Condizioni dei tessuti peri-implantari in impianti trattati con la tecnica del Layer Augmented Sub-periosteo: una serie di casi retrospettiva
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Abstract
Obiettivi: Valutare le condizioni dei tessuti peri-implantari a breve termine in pazienti che ricevono la tecnica dello Strato Augmentato Sub-periostale Peri-implantare (SPAL) e in pazienti con uno spessore adeguato (≥2 mm) della piastra ossea buccale peri-implantare (PBBP) al momento dell'inserimento.
Metodi: I pazienti in cui un difetto di deiscenza o una PBBP sottile al momento dell'inserimento dell'impianto è stata corretta dalla tecnica SPAL (gruppi SPALdehiscence e SPALthin, rispettivamente) e i pazienti con uno spessore residuo di PBBP ≥2 mm al momento dell'inserimento dell'impianto (gruppo di controllo) sono stati selezionati retrospettivamente. Il numero di siti peri-implantari positivi al sanguinamento alla sondaggio (BoP) a 6 mesi dopo il carico protesico è stato l'esito primario. Inoltre, sono stati valutati l'altezza della mucosa cheratinizzata, il livello del tessuto molle marginale, l'Indice di Placca, la profondità di sondaggio peri-implantare, la suppurazione alla sondaggio e il livello osseo radiografico interprossimale (RBL).
Risultati: Trentaquattro pazienti (11 nel gruppo SPALdehiscenza, 11 nel gruppo SPALsottile e 12 nel gruppo di controllo) sono stati inclusi. In ciascun gruppo SPAL, 10 pazienti (90,9%) hanno mostrato uno spessore dei tessuti peri-implantari ≥2 mm nella porzione più coronale dell'impianto al momento della scopertura. La prevalenza (numero) dei siti positivi per BoP è stata di 2, 1 e 0 nei gruppi SPALdehiscenza, SPALsottile e di controllo, rispettivamente. RBL ammontava a 0,3 mm nel gruppo SPALdehiscenza, 0,2 mm nel gruppo SPALsottile e 0 mm nel gruppo di controllo.
Conclusione: Dopo 6 mesi di carico protesico, i pazienti trattati con la tecnica SPAL mostrano un'infiammazione mucosale peri-implantare limitata in associazione con una PD superficiale e un KM adeguato. Negli impianti che ricevono la tecnica SPAL, tuttavia, è stata trovata una RBL interprossimale apicale rispetto alla sua posizione ideale.
Introduzione
Il posizionamento degli impianti guidato protesicamente in una dimensione ossea orizzontale ridotta spesso porta a una deiscenza ossea peri-implantare o a una fenestrazione. Anche in presenza di una piastra corticale buccale intatta ma sottile, il trauma chirurgico e il conseguente rimodellamento osseo dopo il posizionamento dell'impianto possono portare a una perdita ossea verticale con l'esposizione della parte coronale dell'impianto durante la scopertura (Merheb et al., 2017, Monje, et al., 2019, Spray, Black, Morris, 2000). Sebbene la quantità di rimodellamento osseo dopo l'inserimento dell'impianto sia stata dimostrata simile sia in piastre ossee buccali sottili che spesse (Merheb et al., 2017), tale rimodellamento può avere un impatto diverso sull'integrità della piastra ossea buccale peri-implantare (PBBP). A questo proposito, è stato dimostrato in studi preclinici (Monje, et al., 2019) e clinici (Schwarz, Sahm, Becker, 2012, Jung et al., 2017) un aumento del rischio di complicazioni estetiche e biologiche dopo il posizionamento dell'impianto in siti con un difetto di deiscenza o una PBBP sottile rispetto a una PBBP spessa. Complessivamente, questi risultati sottolineano la rilevanza dell'integrità e dello spessore della PBBP al momento del posizionamento dell'impianto per favorire condizioni stabili e sane dei tessuti peri-implantari nel tempo (Sanz-Sánchez et al., 2018).
La procedura più documentata ed efficace per correggere chirurgicamente un difetto di tipo deiscenza si basa sull'uso di membrane barriera combinate con innesti ossei secondo i principi della rigenerazione ossea guidata (GBR) (Sanz-Sánchez, Ortiz-Vigón, Sanz-Martín, Figuero, Sanz, 2015). La riduzione o risoluzione della deiscenza ossea peri-implantare riportata dopo la GBR (Thoma, Bienz, Figuero, Jung, Sanz-Martín, 2019) sembra avere un impatto positivo sulle condizioni a lungo termine degli impianti, in termini di tasso di sopravvivenza degli impianti e stabilità dei tessuti peri-implantari (Sanz-Sánchez et al., 2018). Sfortunatamente, se e in che misura un aumento dello spessore osseo peri-implantare associato a una copertura completa della superficie esposta dell'impianto possa supportare la salute peri-implantare non è stato del tutto chiarito.
Recentemente, è stata descritta una procedura semplificata di aumento osseo, nota come tecnica dello Strato Augmentato Sub-periostale Peri-implantare (SPAL), basata sull'uso del periostio come membrana barriera e di un innesto come "dispositivo" per creare spazio per l'aumento osseo concomitante all'inserimento dell'impianto (Trombelli, Severi, Pramstraller, Farina, 2018). L'efficacia di questa tecnica per correggere una deiscenza ossea peri-implantare e/o per aumentare lo spessore dell'osso peri-implantare è stata precedentemente riportata (Trombelli, Severi, Pramstraller, Farina, 2019), e la sua applicazione è stata esplorata anche nel trattamento dei difetti di peri-implantite (Trombelli et al. 2020). L'obiettivo della presente serie di casi retrospettivi era valutare le condizioni dei tessuti peri-implantari a breve termine in pazienti sottoposti alla tecnica SPAL rispetto a pazienti con uno spessore adeguato (≥2 mm) di PBBP al momento dell'inserimento dell'impianto.
Materiali e metodi
2.1 Progettazione dello studio e aspetti etici
Il presente studio è stato progettato in conformità con le linee guida STROBE Appendice S1. Il protocollo è stato approvato dal Comitato Etico dell'Area Vasta Emilia Centro, Italia (protocollo n. 637/2018/ Oss/UniFe, data di approvazione 12.12.2018). Ogni paziente ha fornito un consenso informato scritto prima del trattamento chirurgico. Tutte le procedure cliniche sono state eseguite in conformità con la Dichiarazione di Helsinki e le Linee Guida di Buona Pratica Clinica (GCP).
2.2 Popolazione dello studio
Le schede cliniche dei pazienti sottoposti a riabilitazione protesica supportata da impianti nel periodo dicembre 2015–luglio 2018 presso il Centro di Ricerca per lo Studio delle Malattie Parodontali e Peri-implantari, Università di Ferrara, e un ufficio dentistico privato a Ferrara sono state esaminate per determinare l'idoneità dei pazienti per lo studio. L'inclusione dei pazienti nello studio era subordinata ai seguenti criteri:
- Non fumatori o fumatori ≤10 sigarette/giorno al momento dell'intervento;
- Non diabetici o diabetici ben controllati (HbA1c ≤ 7%) al momento dell'intervento;
- Disponibilità di parametri clinici ed esami radiografici per lo studio (vedere “Parametri dello studio” per i dettagli).
- Non assumere farmaci che influenzano il metabolismo osseo (ad es., bisfosfonati, corticosteroidi);
- Sottoposti a posizionamento dell'impianto interamente in osso nativo (con uno spessore residuo di PBBP ≥2 mm dopo l'inserimento dell'impianto) o contemporaneamente con la tecnica SPAL.
L'inclusione dell'impianto nello studio era subordinata ai seguenti criteri:
- Posizionamento in cresta guarita (impianti di tipo IV, Hämmerle, Chen, Wilson, 2004);
- Stabilità primaria, come valutata dal torque di inserimento.
Sulla base delle condizioni del PBBP al momento dell'inserimento dell'impianto e sulla sua gestione clinica, i pazienti sono stati categorizzati in tre gruppi:
- Pazienti con impianto/i che presentano uno spessore residuo di PBBP ≥2 mm dopo l'inserimento dell'impianto (gruppo di controllo);
- Pazienti con impianto/i trattati con la tecnica SPAL per correggere una deiscenza ossea peri-impiantare ≥3 mm contemporaneamente all'inserimento dell'impianto (gruppo SPALdehiscence);
- Pazienti con impianto/i trattati con la tecnica SPAL per aumentare un PBBP sottile (≤1 mm) contemporaneamente all'inserimento dell'impianto (gruppo SPALthin).
2.3 Procedure cliniche
Prima dell'inserimento dell'impianto, tutti i pazienti avevano subito una terapia attiva per il trattamento delle lesioni cariose e delle malattie parodontali ed erano stati iscritti a una manutenzione professionale con frequenza di richiami programmata secondo lo strumento di valutazione PerioRisk (Trombelli, Farina, Ferrari, Pasetti, Calura, 2009, Trombelli et al., 2017).
Tutte le procedure chirurgiche sono state eseguite da due periodontisti esperti (L.T. e M.P.). Ai pazienti è stata somministrata una dose di 2 g di amoxicillina + acido clavulanico (Augmentin, GlaxoSmithKline) un'ora prima dell'intervento. L'anestesia locale è stata ottenuta utilizzando articaine con 1:100.000 di epinefrina somministrata per infiltrazione locale.
2.3.1 Procedure chirurgiche—gruppi SPAL
Nei pazienti in cui è stata corretta una deiscenza o una PBBP sottile al momento dell'inserimento mediante la tecnica SPAL (Figure 1 e 2, rispettivamente), l'accesso chirurgico alla cresta ossea è stato eseguito come precedentemente descritto (Trombelli, Severi, Pramstraller, & Farina, 2018). In breve, uno strato mucoso è stato sollevato sul lato buccale mediante dissezione a spessore parziale con una lama 15C, oltre a coltelli per tunneling (KPAX, TKN1X e TKN2X, Hu-Friedy) con bordi affilati angolati variabili a seconda della posizione anatomica. Successivamente, lo strato periosteo è stato elevato dall'osso con un elevatore periosteo (PTROM, Hu-Friedy), creando una tasca che poteva ospitare un innesto. Un lembo a spessore totale è stato sollevato sul lato orale (linguale/palatale).
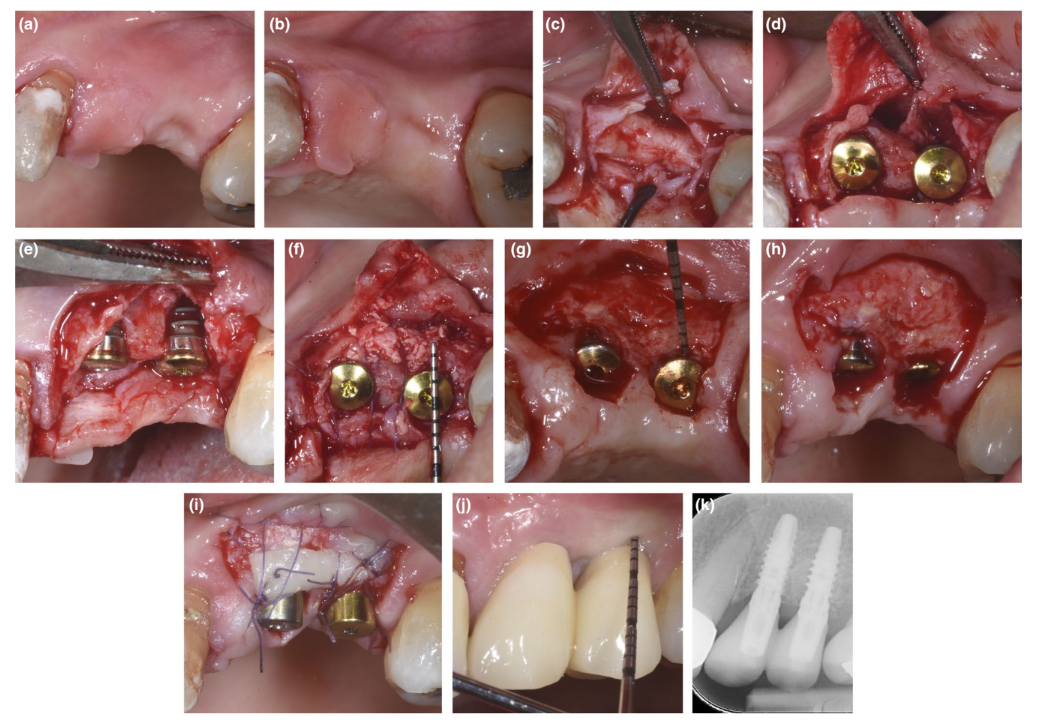
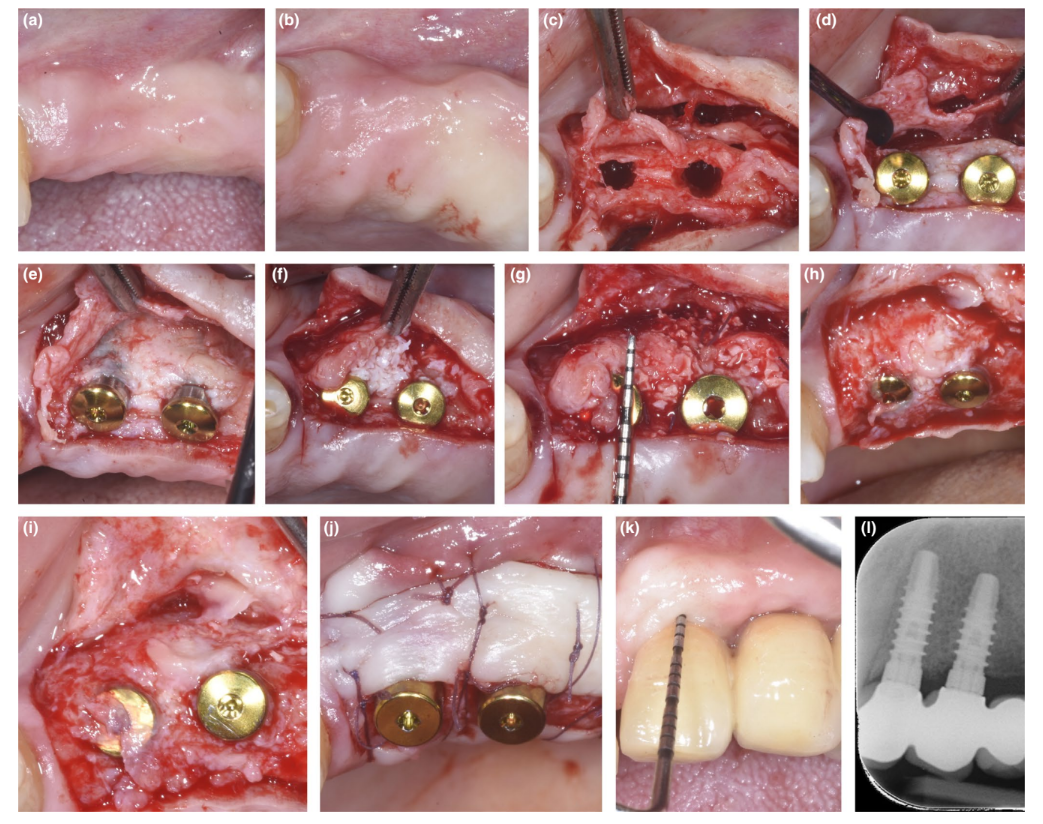
Gli impianti a livello tissutale (SPI Element™; Thommen Medical) sono stati inseriti. È stato utilizzato un xenoinnesto di origine bovina (Bio-Oss® granuli di spongiosa, dimensione delle particelle 0,25–1,0 mm; Geistlich Pharma, AG) da solo o in combinazione con particelle di osso corticale autologo per riempire lo spazio creato chirurgicamente tra il strato periosteo e la sottile piastra ossea buccale o la superficie dell'impianto esposta. In presenza di una deiscenza, è stato eseguito un innesto per correggere completamente il difetto peri-implantare fino al collare lucidato. In tutti i casi, l'innesto sub-periosteo ha fornito almeno 2 mm di spessore nella porzione coronale più alta dell'impianto.
La porzione coronale dello strato periosteo è stata stabilizzata al lembo mucoperiosteo orale mediante suture interne a materasso riassorbibili (Vicryl 6/0, Ethicon). Lo strato mucoso è stato quindi avanzato coronariamente e suturato senza tensione mediante suture interne a materasso orizzontali e suture interrotte per sommergere sia l'innesto che gli impianti.
Durante la procedura di re-inserimento per il rilascio dell'impianto, è stata dissezionata una flap buccale a spessore parziale per posizionare l'abutment di guarigione. Per fornire dimensioni adeguate della mucosa peri-impiantare cheratinizzata, è stata eseguita una flap posizionata apicalmente o un innesto gengivale libero (Trombelli, Severi, Pramstraller, & Farina, 2019).
2.3.2 Procedure chirurgiche—gruppo di controllo
È stata sollevata una flap buccale e linguale/palatale a spessore totale per esporre la cresta ossea. Il sito dell'impianto è stato preparato secondo le istruzioni del produttore, e sono stati inseriti impianti a livello del tessuto (SPI Element™; Thommen Medical). A causa della presenza di uno spessore residuo di PBBP ≥2 mm, non è stata eseguita alcuna procedura di aumento osseo. In tutti i casi, la flap è stata rifilata e posizionata attorno all'abutment di guarigione con suture riassorbibili (Vicryl 6/0, Ethicon). Il design e la manipolazione della flap, così come la tecnica di sutura, sono stati eseguiti per garantire dimensioni adeguate (altezza, spessore) della mucosa peri-impiantare cheratinizzata.
2.3.3 Procedure postoperative
Ai pazienti è stato detto di non indossare protesi rimovibili per evitare compressioni sul sito chirurgico per almeno 4 settimane e di non masticare o spazzolare nell'area trattata per circa 2 settimane.
È stata prescritta l'uso domiciliare di una soluzione di clorexidina allo 0,12% (Curasept ADS Trattamento Rigenerante®; Curaden Healthcare) per il controllo chimico della placca (risciacquo di 1 minuto b.i.d. per 3 settimane). I punti sono stati rimossi 2 settimane dopo l'intervento chirurgico.
2.3.4 Tempistiche della riabilitazione protesica
La riabilitazione protesica è stata avviata 3–4 mesi dopo il posizionamento dell'impianto nel gruppo di controllo, mentre almeno 4 settimane dopo la scopertura dell'impianto nei gruppi SPAL.
2.4 Parametri dello studio
2.4.1 Parametri clinici
Dopo 6 mesi di carico protesico, un esaminatore formato (M.S.) che era stato coinvolto in studi precedenti sulla tecnica SPAL (Trombelli, Severi, Pramstraller, Farina, 2019) ha eseguito le seguenti misurazioni cliniche con una sonda parodontale UNC-15 nella seguente sequenza cronologica:
- Altezza della mucosa cheratinizzata (KM): misurata nell'aspetto medio-buccale dell'impianto come la distanza tra il margine mucoso peri-impiantare buccale e la giunzione mucogengivale, e registrata al millimetro più vicino;
- Livello del tessuto molle marginale (MSTL) (Zitzmann, Schärer, Marinello, 2001): misurato nell'aspetto medio-buccale dell'impianto come la distanza tra il margine mucoso peri-impiantare buccale e la giunzione impianto-abutment, e registrato al millimetro più vicino. MSTL è stato registrato come positivo o negativo quando il margine dell'abutment si trovava sopra o sotto il margine mucoso, rispettivamente;
- Indice di placca (PlI; O'Leary, Drake, Naylor, 1972): registrato negli aspetti mesio-buccale, medio-buccale, disto-buccale, medio-linguale/palatale dell'impianto come placca sopragengivale presente o assente dopo aver esplorato il margine protesico juxtagingivale con la punta della sonda;
- Profondità di sondaggio (PD): misurata dal margine mucoso alla penetrazione più profonda della sonda in sei siti (mesio-buccale, medio-buccale, disto-buccale, disto-linguale, medio-linguale e mesio-linguale) utilizzando una forza di 0,2–0,3 N, e registrata al millimetro più vicino;
- Sanguinamento alla sondaggio (BoP; Ainamo e Bay, 1975): registrato come presente o assente durante la valutazione della PD;
- Suppurazione alla sondaggio (SoP): registrata come presente o assente durante la valutazione della PD.
2.4.2 Livello osseo radiografico
Radiografie periapicali non standardizzate eseguite con la tecnica parallela a cono lungo a 6 mesi dopo il carico protesico sono state digitalizzate e analizzate utilizzando un software appositamente progettato (NIS elements v4.2; Nikon Instruments, Campi Bisenzio). Il livello osseo radiografico (RBL) è stato misurato come la distanza (approssimata al millimetro più vicino) tra il margine apicale del collare lucido dell'impianto e la cresta ossea nell'aspetto mesiale (mRBL) e distale (dRBL) di ciascun impianto utilizzando un ingrandimento di 10x–15x. Un segno di riferimento alto 1 mm presente sulla radiografia digitale è stato utilizzato per la calibrazione.
Un esaminatore (A.S.) ha eseguito le misurazioni radiografiche. L'esaminatore è stato coinvolto in una sessione di calibrazione su un campione di radiografie ottenute da pazienti non selezionati per il presente studio. La sessione di calibrazione consisteva in due sessioni di misurazioni RBL, eseguite a intervalli di 7 giorni, e ha permesso di raggiungere un'eccellente concordanza intra-esaminatore (punteggio k = 0.89), con una differenza media tra misurazioni abbinate di 0.04 ± 0.15 mm.
2.5 Analisi statistica
Il paziente è stato considerato come l'unità statistica. Se due o più impianti nello stesso paziente erano idonei per lo studio, solo un impianto è stato incluso casualmente per l'analisi. I dati sono stati descritti utilizzando media e deviazione standard (SD), mediana e intervallo interquartile (IR), valori minimi-massimi per variabili quantitative e frequenza e percentuale per variabili categoriali.
Il numero mediano di siti positivi al BoP valutato a 6 mesi dopo il carico dell'impianto è stata la variabile principale dello studio. I valori mediani di PD, KM, MSTL, RBL, numero di siti positivi al PlI e numero di siti positivi al SoP erano variabili secondarie.
A causa della dimensione limitata del campione, non sono state eseguite statistiche inferenziali e i risultati sono stati riportati con un approccio narrativo. Tuttavia, la dimensione dell'effetto (ES) è stata calcolata per ciascuna variabile di esito secondo il test non parametrico di Kruskal-Wallis. L'ES è stata classificata come piccola (d = 0.1–0.3), media (d = 0.3–0.5) o grande (d ≥ 0.5) (Cohen, 1988).
Risultati
3.1 Popolazione dello studio
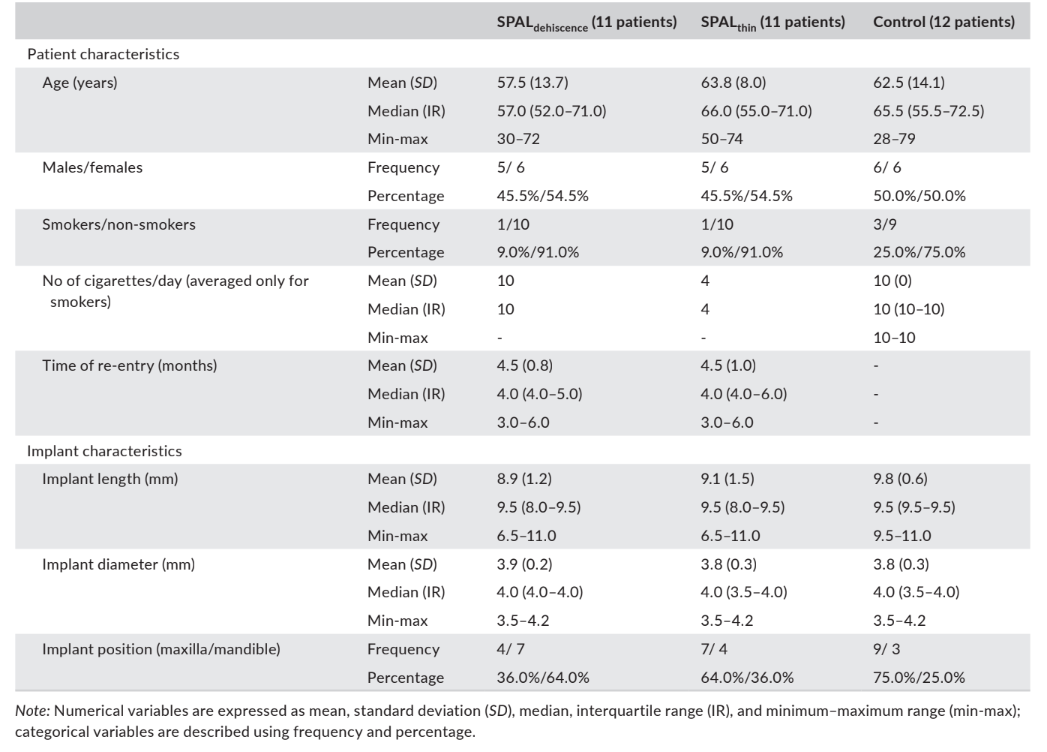
Trentaquattro pazienti con 34 impianti (11 nel gruppo SPALdehiscenza, 11 nel gruppo SPALsottile, e 12 nel gruppo di controllo) sono stati inclusi per l'analisi. La stragrande maggioranza dei pazienti era non fumatrice (90,9% nel gruppo SPALdehiscenza, 90,9% nel gruppo SPALsottile, e 75% nel gruppo di controllo). Gli impianti nel gruppo SPALdehiscenza erano prevalentemente localizzati nella mandibola, mentre gli impianti nei gruppi SPALsottile e di controllo erano prevalentemente posizionati nella mascella (Tabella 1). Nessun paziente o impianto è andato perso durante il periodo di follow-up.
Nel gruppo SPALdeiscenza, 1 paziente ha mostrato deiscenza della ferita dopo 2 settimane, con esposizione parziale dei fili dell'impianto. Il paziente è stato visitato mensilmente fino al re-inserimento, e il sito è stato disinfettato localmente con una soluzione di clorexidina allo 0,12% ad ogni visita di richiamo.
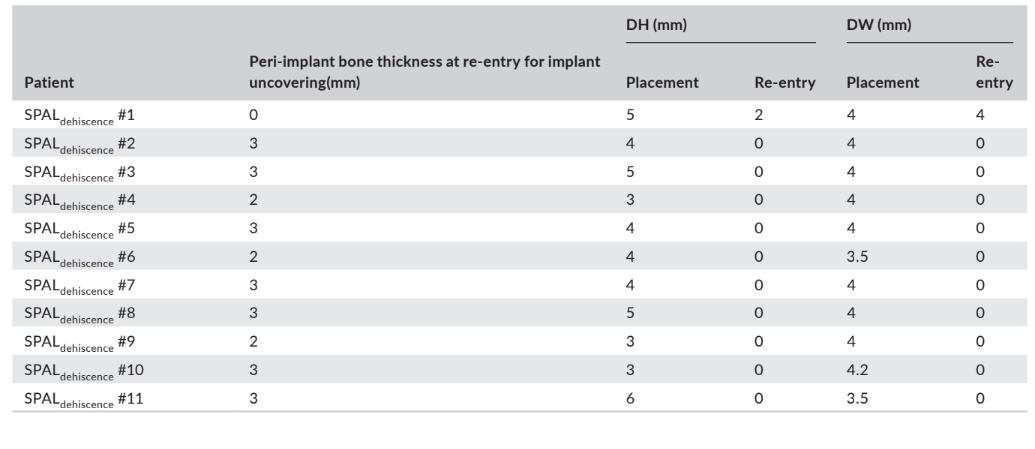
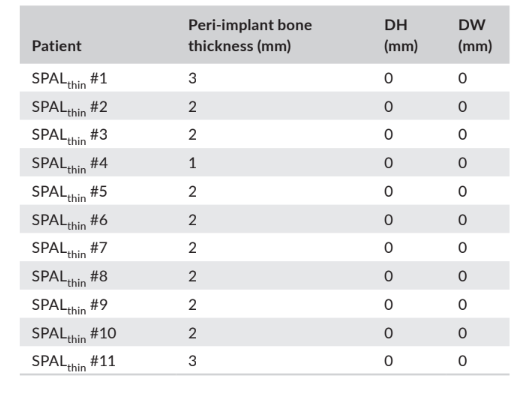
In entrambi i gruppi SPALdeiscenza e SPALsottile, il re-inserimento è stato effettuato a 3–6 mesi dopo il posizionamento dell'impianto (mediana: 4,0 mesi in entrambi i gruppi; p = 1; Tabella 1). Lo spessore dell'osso peri-impiantare e l'altezza e la larghezza della deiscenza ossea peri-impiantare registrati per i gruppi SPALdeiscenza e SPALsottile sono riportati nelle Tabelle 2 e 3, rispettivamente. In ciascun gruppo SPAL, 10 pazienti (90,9%) hanno mostrato assenza di deiscenza peri-impiantare combinata con uno spessore dell'osso peri-impiantare ≥2 mm (Tabelle 2 e 3). Un paziente nel gruppo SPALdeiscenza ha presentato una deiscenza residua di 2 mm (Tabella 2), che è stata coperta con un innesto gengivale libero. Un paziente nel gruppo SPALsottile ha presentato uno spessore dell'osso peri-impiantare di 1 mm senza deiscenza (Tabella 3).
Nel gruppo SPALdehiscence, 8 impianti supportavano una protesi parziale fissa, 2 impianti sono stati restaurati con una corona singola e 1 impianto faceva parte di una protesi mobile. Nel gruppo SPALthin, 9 impianti supportavano una protesi parziale fissa, 2 impianti sono stati restaurati con una corona singola e 1 faceva parte di una protesi mobile. Nel gruppo di controllo, 4 impianti facevano parte di una protesi parziale fissa e 8 impianti sono stati restaurati con una corona singola.
3.2 Risultati dello studio
I dati relativi agli esiti clinici (cioè, PD, BoP, SoP, PlI, MSTL e KM) e RBL valutati a 6 mesi dopo il carico dell'impianto sono riportati nella Tabella 4.
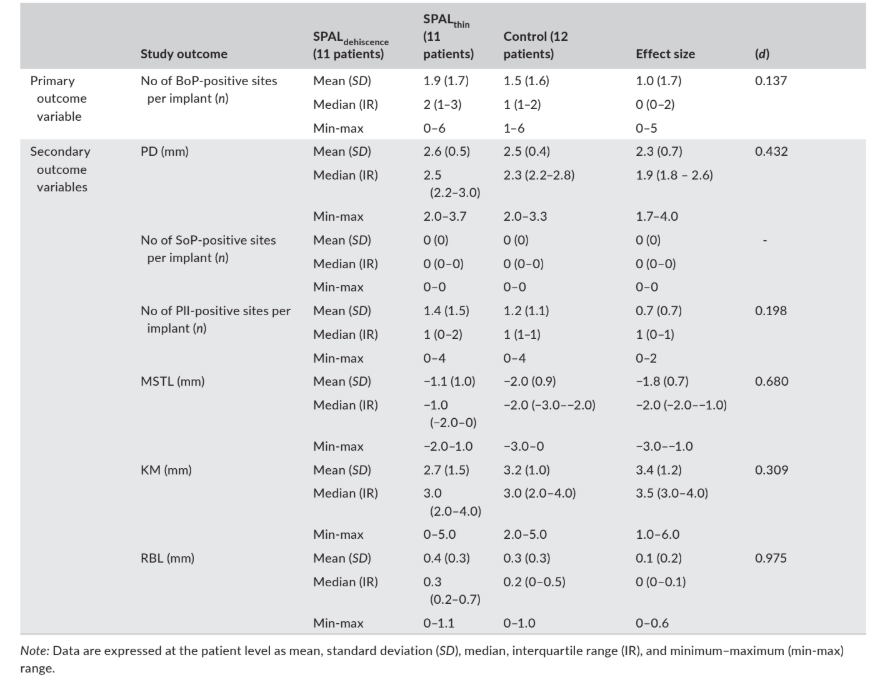
del tessuto molle marginale, MSTL; e larghezza della mucosa cheratinizzata, KM) e livello osseo radiografico (RBL) valutati a 6 mesi dopo il carico dell'impianto.
La prevalenza mediana (numero) dei siti positivi al BoP era di 2, 1 e 0 nei gruppi SPALdehiscenza, SPALsottile e di controllo, rispettivamente.
Il numero mediano di siti positivi al PlI era di 1 in tutti i gruppi. SoP era negativo in tutti i siti implantari.
Il margine mucosale era situato a 1 mm (gruppo SPALdehiscenza) o 2 mm (gruppi SPALsottile e di controllo) sopra la giunzione impianto-abutment in tutti i gruppi, e i gruppi di studio presentavano una KM mediana di almeno 3 mm.
Il livello osseo radiografico ammontava a 0,3 mm nel gruppo SPALdehiscenza, 0,2 mm nel gruppo SPALsottile e 0 mm nel gruppo di controllo.
L'ES era piccolo per il numero di siti BoP + (d = 0,137) e PlI (d = 0,198), medio per KM (d = 0,309), PD (d = 0,432) e MSTL (d = 0,680), e grande per RBL (d = 0,975) (Tabella 4).
Discussione
L'obiettivo della presente serie di casi retrospettivi era valutare le condizioni dei tessuti peri-implantari a breve termine in pazienti sottoposti alla tecnica SPAL e in pazienti con uno spessore adeguato (≥2 mm) di PBBP al momento dell'inserimento dell'impianto. I risultati hanno indicato che i pazienti trattati con la tecnica SPAL hanno mostrato un numero ridotto di siti peri-implantari infiammati e una PD superficiale (<4 mm) a 6 mesi dal carico protesico. Inoltre, il livello osseo interprossimale è stato trovato apicale (sebbene in misura limitata) al collare lucido dell'impianto solo nei gruppi SPAL.
Il sanguinamento alla sondaggio è stato selezionato come esito primario poiché (a) la valutazione del BoP è attualmente identificata come la misura clinica per distinguere tra salute e malattia peri-implantare, essendo un elemento diagnostico invariabile della mucosite peri-implantare e della peri-implantite (Renvert, Persson, Pirih, Camargo, 2018, Berglundh et al., 2018), e (b) la sua assenza è associata alla stabilità delle condizioni dei tessuti peri-implantari (Jepsen, Rühling, Jepsen, Ohlenbusch, Albers, 1996, Luterbacher, Mayfield, Brägger, Lang, 2000). La proporzione di siti peri-implantari infiammati registrata nei gruppi di studio è comparabile con i risultati precedenti che valutano la prevalenza del BoP su 289 impianti (Farina, Filippi, Brazzioli, Tomasi, Trombelli, 2017). Inoltre, condizioni infiammatorie peri-implantari simili sono state riportate a 18 mesi dopo GBR (Jung et al., 2017).
Nel nostro studio, è stata osservata una bassa frequenza di siti mucosali peri-implantari infiammati in tutti i gruppi di studio. Questo può essere in parte dovuto a caratteristiche simili per fattori che influenzano il BoP attorno agli impianti, come la bassa presenza di placca giustagingivale (Pontoriero et al., 1994; Salvi et al., 2012), PD superficiale (Farina, Filippi, Brazzioli, Tomasi, & Trombelli, 2017) e un'adeguata quantità di KM (Chung, Oh, Shotwell, Misch, Wang, 2006, Perussolo et al., 2018). I nostri risultati sono coerenti con quelli derivanti da una recente revisione sistematica sulle complicazioni biologiche degli impianti dentali posizionati sia in siti pristini che in siti aumentati. La meta-analisi ha mostrato una prevalenza simile di mucosite peri-implantare nei pazienti che ricevevano (19,6%; 95% CI: 0%–40%) o non ricevevano (22,4%; 95% CI: 6%–38%) procedure per la preservazione del cresta alveolare e/o l'aumento verticale/laterale della cresta (Salvi, Monje, Tomasi, 2018). Inoltre, condizioni infiammatorie simili sono state riportate per impianti posizionati in osso nativo rispetto a impianti posizionati congiuntamente a una procedura GBR (Benic, Jung, Siegenthaler, Hammerle, 2009; Benic, Bernasconi, Jung, Hammerle, 2017).
È importante considerare che al rientro, la grande maggioranza dei pazienti che hanno ricevuto la tecnica SPAL ha mostrato uno spessore osseo peri-implantare ≥2 mm nella porzione più coronale dell'impianto. Sebbene la misurazione del PBBP non fosse disponibile al rientro per il gruppo di controllo (procedura a una fase), l'integrità del PBBP dopo il rimodellamento osseo peri-implantare post-inserzione può essere assunta sulla base di dati preclinici (Monje et al., 2019) e clinici (Spray, Black, Morris, & Ochi, 2000) sulle dimensioni critiche della piastra ossea buccale. Complessivamente, i dati disponibili sembrano suggerire che dimensioni verticali e orizzontali adeguate dei tessuti peri-implantari ottenute mediante procedure di aumento possano favorire condizioni per limitare l'infiammazione dei tessuti peri-implantari. Tuttavia, l'associazione tra l'integrità del PBBP fino alla porzione più coronale dell'impianto e la gravità dell'infiammazione mucosale peri-implantare non è del tutto chiara (Jung et al., 2017).
A 6 mesi dal carico protesico, è stata osservata una posizione diversa del livello osseo peri-implantare interprossimale tra i gruppi, con una RBL più apicale nei gruppi SPAL. È degno di nota che, nei gruppi SPAL, gli impianti a livello tissutale sono stati posizionati leggermente sottocrestali (Figure 1 e 2). Sebbene ciò possa aver facilitato l'innesto della tasca periostale fino alla parte più coronale dell'impianto, così come la chiusura per prima intenzione, il posizionamento sottocrestale potrebbe anche aver contribuito al rimodellamento osseo interprossimale (Saleh et al., 2018). Inoltre, poiché gli impianti che ricevevano la tecnica SPAL hanno subito un intervento chirurgico aggiuntivo per la scopertura, incluso un lembo posizionato apicalmente o un innesto gengivale libero, il rimodellamento osseo interprossimale nei gruppi SPAL potrebbe essere anche in parte attribuito all'effetto dannoso dell'elevazione del lembo sulla vascolarizzazione locale. Coerentemente, è stata riportata una perdita ossea marginale peri-implantare tra il re-intervento per la scopertura e la consegna della protesi finale da altri autori (Cardaropoli, Lekholm, Wennstrom, 2006, Nader et al., 2016). Si dovrebbe anche considerare che, in alcuni pazienti del gruppo SPALdeiscenza, l'innesto è stato esteso agli aspetti mesiali e/o distali dell'impianto a causa di un'estensione interprossimale del difetto osseo peri-implantare. Nel gruppo SPALdeiscenza, quindi, l'estensione del rimodellamento dell'innesto nei siti interprossimali potrebbe aver avuto un impatto negativo sui valori di RBL. Dati recenti hanno mostrato che anche i biomateriali per innesti a lenta riassorbibilità, come il DBBM, sono associati a una sostanziale riduzione dell'area innestata nella valutazione radiografica a 12 mesi dopo le procedure di aumento endosinussale (Franceschetti et al., 2019). Tuttavia, l'entità della RBL osservata nello studio presente è limitata rispetto a quella riportata per impianti posizionati con GBR concomitante o in osso nativo (Urban et al., 2019) e impianti che presentano una deiscenza buccale non trattata (Jung et al., 2017).
È stata osservata una KM e MSTL leggermente inferiori per il gruppo SPALdehiscenza. Questo è avvenuto nonostante la manipolazione dei tessuti molli peri-implantari fosse stata adeguatamente eseguita per fornire dimensioni adeguate della mucosa peri-implantare cheratinizzata e una posizione sottogengivale dei margini protesici. Questo risultato potrebbe essere in qualche modo correlato con l'aumento del rimodellamento osseo (RBL) osservato nel gruppo SPALdehiscenza, che potrebbe aver coinvolto anche la piastra ossea buccale rigenerata. Una recente revisione sistematica ha correlato il rimodellamento dell'osso buccale con l'insorgenza della recessione dei tessuti molli peri-implantari (Aizcorbe-Vicente, Peñarrocha-Oltra, Canullo, Soto-Peñaloza, & Peñarrocha-Diago, 2020). Nel gruppo SPALdehiscenza, 1 paziente (9,1%) ha sperimentato una deiscenza della ferita a 2 settimane che ha portato a un'esposizione parziale dei fili dell'impianto al riesame. Questo risultato è paragonabile all'incidenza di deiscenza della ferita e conseguente esposizione della membrana dopo procedure GBR per correggere la deiscenza ossea peri-implantare al momento dell'inserimento, come riportato in una recente meta-analisi condotta su studi sia prospettici che retrospettivi (Garcia et al., 2018). In particolare, l'esposizione della membrana si è verificata con un'incidenza che variava dal 16,7% (Tawil, El-Ghoule, & Mawla, 2001) al 62,8% (Gher, Quintero, Assad, Monaco, & Richardson, 1994), ed era associata a una copertura della deiscenza significativamente inferiore (Garcia et al., 2018). Le limitazioni di questo rapporto preliminare includono il design retrospettivo, la piccola dimensione del campione e il breve tempo di follow-up di 6 mesi dopo il ripristino degli impianti. Inoltre, l'impatto di fattori correlati al paziente (ad es., spessore dei tessuti molli nell'area edentula, abitudine al fumo, diabete) e complicazioni correlate alla chirurgia (ad es., perforazioni del periostio e/o dello strato mucoso) sugli esiti clinici non è stato analizzato in modo completo. Inoltre, condizioni cliniche specifiche (cioè, PBBP sottile o deiscenza ossea peri-implantare di dimensione verticale limitata) sono state selezionate per il trattamento SPAL. Sono necessari ulteriori studi per valutare quali condizioni/lesioni cliniche possano essere trattate efficacemente con la tecnica SPAL o se un trattamento più convenzionale (ad es., GBR) debba essere preferito.
In conclusione, i risultati del presente studio hanno mostrato che, dopo 6 mesi di carico protesico, i pazienti trattati con la tecnica SPAL mostrano un'infiammazione mucosale peri-implantare limitata in associazione con una PD superficiale e un KM adeguato. Tuttavia, negli impianti che ricevono la tecnica SPAL, è stata trovata una RBL interprossimale apicale rispetto alla sua posizione ideale. Se e in che misura i favorevoli risultati a breve termine osservati dopo la tecnica SPAL possano essere benefici per le condizioni di salute a lungo termine dei tessuti peri-implantari e la stabilità del profilo mucosale buccale deve essere valutato.
Leonardo Trombelli, Mattia Pramstraller, Mattia Severi, Anna Simonelli, Roberto Farina
Riferimenti
- Ainamo, J., & Bay, I. (1975). Problemi e proposte per la registrazione della gengivite e della placca. International Dental Journal, 25, 229–235.
- Aizcorbe-Vicente, J., Peñarrocha-Oltra, D., Canullo, L., Soto-Peñaloza, D., & Peñarrocha-Diago, M. (2020). Influenza dello spessore osseo facciale dopo il posizionamento dell'impianto nelle creste guarite sull'osso facciale rimodellato e considerando la recessione dei tessuti molli: Una revisione sistematica. International Journal of Oral and Maxillofacial Implants, 35, 107–119. https://doi.org/10.11607/jomi.7259
- Benic, G. I., Bernasconi, M., Jung, R. E., & Hammerle, C. H. F. (2017). Confronto clinico e radiografico intra-soggetto di impianti posizionati con o senza rigenerazione ossea guidata: risultati a 15 anni. Journal of Clinical Periodontology, 44, 315–325. https://doi.org/10.1111/jcpe.12665
- Benić, G. I., Jung, R. E., Siegenthaler, D. W., & Hämmerle, C. H. F. (2009). Confronto clinico e radiografico di impianti in osso rigenerato o nativo: risultati a 5 anni. Clinical Oral Implant Research, 20, 507–513. https://doi.org/10.1111/j.1600-0501.2008.01583.x
- Berglundh, T., Armitage, G., Araujo, M. G., Avila-Ortiz, G., Blanco, J., Camargo, P. M., Zitzmann, N. (2018). Malattie e condizioni peri-implantari: rapporto di consenso del gruppo di lavoro 4 del World Workshop 2017 sulla classificazione delle malattie e condizioni parodontali e peri-implantari. Journal of Clinical Periodontology, 45(Suppl 20), S286–S291. https://doi.org/10.1034/j.1600-0501.1994.050409.x
- Cardaropoli, G., Lekholm, U., & Wennstrom, J. L. (2006). Alterazioni tissutali nei sostituti di denti singoli supportati da impianti: uno studio clinico prospettico di 1 anno. Clinical Oral Implant Research, 17, 165–171. https://doi.org/10.1111/j.1600-0501.2005.01210.x
- Chung, D. M., Oh, T. J., Shotwell, J. L., Misch, C. E., & Wang, H. L. (2006). Significato della mucosa cheratinizzata nel mantenimento degli impianti dentali con superfici diverse. Journal of Periodontology, 77, 1410–1420. https://doi.org/10.1902/jop.2006.050393
- Cohen, J. (1988). Analisi della potenza statistica per le scienze comportamentali, 2a ed. Mahwah, NJ: Lawrence Erlbaum Associated Publishers.
- Farina, R., Filippi, M., Brazzioli, J., Tomasi, C., & Trombelli, L. (2017). Emorragia alla sondatura attorno agli impianti dentali: uno studio retrospettivo dei fattori associati. Journal of Clinical Periodontology, 44, 115–122. https://doi.org/10.1111/jcpe.12647
- Franceschetti, G., Farina, R., Minenna, L., Riccardi, O., Stacchi, C., Di Raimondo, R., … Trombelli, L. (2019). L'impatto del rimodellamento del innesto sul supporto osseo peri-implantare in impianti posizionati concomitantemente con l'elevazione del pavimento del seno trascrestale: una serie di casi retrospettiva multicentrica. Clinical Oral Implant Research, 31(2), 1–16. https://doi.org/10.1111/clr.13541
- Garcia, J., Dodge, A., Luepke, P., Wang, H. L., Kapila, Y., & Lin, G. H. (2018). Effetto dell'esposizione della membrana sulla rigenerazione ossea guidata: una revisione sistematica e meta-analisi. Clinical Oral Implants Research, 29, 328–338. https://doi.org/10.1111/clr.13121
- Gher, M. E., Quintero, G., Assad, D., Monaco, E., & Richardson, A. C. (1994). Innesto osseo e rigenerazione ossea guidata per impianti dentali immediati negli esseri umani. Journal of Periodontology, 65, 881–891. https://doi.org/10.1902/jop.1994.65.9.881
- Hämmerle, C. H., Chen, S. T., & Wilson, T. G. Jr (2004). Dichiarazioni di consenso e procedure cliniche raccomandate riguardo al posizionamento di impianti in siti di estrazione. International Journal of Oral and Maxillofacial Implants, 19(suppl), 26–28.
- Jepsen, S., Rühling, A., Jepsen, K., Ohlenbusch, B., & Albers, H. K. (1996). Peri-implantite progressiva. Incidenza e previsione della perdita di attacco peri-implantare. Clinical Oral Implants Research, 7, 133–142. https://doi.org/10.1034/j.1600-0501.1996.070207.x
- Jung, R. E., Herzog, M., Wolleb, K., Ramel, C. F., Thoma, D. S., & Hammerle, C. H. F. (2017). Uno studio clinico controllato randomizzato che confronta piccoli difetti di deiscenza buccale attorno agli impianti dentali trattati con rigenerazione ossea guidata o lasciati per guarigione spontanea. Clinical Oral Implants Research, 28, 348–354. https://doi.org/10.1111/clr.12806
- Luterbacher, S., Mayfield, L., Brägger, U., & Lang, N. P. (2000). Caratteristiche diagnostiche di test clinici e microbiologici per il monitoraggio delle condizioni dei tessuti mucosali parodontali e peri-implantari durante la terapia parodontale di supporto (SPT). Clinical Oral Implants Research, 11, 521–529. https://doi.org/10.1034/j.1600-0501.2000.011006521.x
- Merheb, J., Vercruyssen, M., Coucke, W., Beckers, L., Teughels, W., & Quirynen, M. (2017). Il destino dell'osso buccale attorno agli impianti dentali. Uno studio di follow-up di 12 mesi dopo il carico. Clinical Oral Implants Research, 28, 103–108. https://doi.org/10.1111/clr.12767
- Monje, A., Chappuis, V., Monje, F., Muñoz, F., Wang, H. L., Urban, I. A., & Buser, D. (2019). Lo spessore critico della parete ossea buccale peri-implantare rivisitato: uno studio sperimentale nel cane Beagle. Int J Oral Maxillofac Implants, 34, 1328–1336. https://doi.org/10.11607/jomi.7657
- Nader, N., Aboulhosn, M., Berberi, A., Manal, C., & Younes, R. (2016). Rimodellamento osseo marginale attorno all'elemento di guarigione rispetto al posizionamento dell'elemento finale nella chirurgia di secondo stadio: uno studio clinico randomizzato di 12 mesi. Journal of Contemporary Dental Practice, 17, 7–15. https://doi.org/10.5005/jp-journals-10024
- O'Leary, T. J., Drake, R. B., & Naylor, J. E. (1972). Il registro di controllo della placca. Journal of Periodontology, 43, 38. https://doi.org/10.1902/jop.1972.43.1.38
- Perussolo, J., Souza, A. B., Matarazzo, F., Oliveira, R. P., & Araújo, M. G. (2018). Influenza della mucosa cheratinizzata sulla stabilità dei tessuti peri-implantari e sul disagio durante lo spazzolamento: uno studio di follow-up di 4 anni. Clinical Oral Implant Research. Journal of Clinical Periodontology, 29, 1177–1185. https://doi.org/10.1111/clr.13381
- Pontoriero, R., Tonelli, M. P., Carnevale, G., Mombelli, A., Nyman, S. R., & Lang, N. P. (1994). Mucositi peri-implantari indotte sperimentalmente. Uno studio clinico negli esseri umani. Clinical Oral Implants Research, 5, 254–259. https://doi.org/10.1034/j.1600-0501.1994.050409.x
- Renvert, S., Persson, G. R., Pirih, F. Q., & Camargo, P. M. (2018). Salute peri-implantare, mucosite peri-implantare e peri-implantite: definizioni dei casi e considerazioni diagnostiche. Journal of Clinical Periodontology, 45(Suppl 20), S278–S285. https://doi.org/10.1111/jcpe.12956
- Saleh, M. H. A., Ravidà, A., Suárez-López Del Amo, F., Lin, G.-H., Asa'ad, F., & Wang, H.-L. (2018). L'effetto della posizione della giunzione impianto-abutment sulla perdita ossea crestal: una revisione sistematica e meta-analisi. Clinical Implant Dentistry and Related Research, 20, 617–633. https://doi.org/10.1111/cid.12600
- Salvi, G. E., Aglietta, M., Eick, S., Sculean, A., Lang, N. P., & Ramseier, C. A. (2012). Reversibilità della mucosite peri-implantare sperimentale rispetto alla gengivite sperimentale negli esseri umani. Clinical Oral Implants Research, 23, 182–190. https://doi.org/10.1111/j.1600-0501.2011.02220.x
- Salvi, G. E., Monje, A., & Tomasi, C. (2018). Complicazioni biologiche a lungo termine degli impianti dentali posizionati in siti pristini o aumentati: una revisione sistematica e meta-analisi. Clinical Oral Implant Research, 29(Suppl. 16), 294–310. https://doi.org/10.1111/clr.13123
- Sanz-Sánchez, I., Carrillo de Albornoz, A., Figuero, E., Schwarz, F., Jung, R., Sanz, M., & Thoma, D. (2018). Effetti delle procedure di aumento osseo laterale sulla salute o malattia peri-implantare: una revisione sistematica e meta-analisi. Clinical Oral Implants Research, 29, 18–31. https://doi.org/10.1111/clr.13126
- Sanz-Sánchez, I., Ortiz-Vigón, A., Sanz-Martín, I., Figuero, E., & Sanz, M. (2015). Efficacia dell'aumento osseo laterale sulla dimensione della cresta alveolare: una revisione sistematica e meta-analisi. Journal of Dental Research, 94, 1s–15s. https://doi.org/10.1177/0022034515594780
- Schwarz, F., Sahm, N., & Becker, J. (2012). Impatto del risultato della rigenerazione ossea guidata in difetti di tipo deiscenza sulla stabilità a lungo termine della salute peri-implantare: osservazioni cliniche a 4 anni. Clinical Oral Implants Research, 23, 191–196. https://doi.org/10.1111/j.1600-0501.2011.02214.x
- Spray, J. R., Black, C. G., Morris, H. F., & Ochi, S. (2000). L'influenza dello spessore osseo sulla risposta ossea marginale facciale: posizionamento di fase 1 attraverso la scopertura di fase 2. Annals of Periodontology, 5, 119–128. https://doi.org/10.1902/annals.2000.5.1.119
- Tawil, G., El-Ghoule, G., & Mawla, M. (2001). Valutazione clinica di una membrana di collagene bilayer (bio-gide) supportata da innesti autologhi nel trattamento dei difetti ossei attorno agli impianti. The International Journal of Oral & Maxillofacial Implants, 16, 857–863.
- Thoma, D. S., Bienz, S. P., Figuero, E., Jung, R. E., & Sanz-Martín, I. (2019). Effetti delle procedure di aumento dei tessuti molli sulla salute o malattia peri-implantare: una revisione sistematica e meta-analisi. Journal Clinical Periodontology, 46(Suppl 21), 257–276. https://doi.org/10.1111/jcpe.13050
- Trombelli, L., Farina, R., Ferrari, S., Pasetti, P., & Calura, G. (2009). Confronto tra due metodi per la valutazione del rischio parodontale. Minerva Stomatologica, 58, 277–287.
- Trombelli, L., Minenna, L., Toselli, L., Zaetta, A., Checchi, L., Checchi, V., … Farina, R. (2017). Valore prognostico di un metodo semplificato per la valutazione del rischio parodontale durante la terapia parodontale di supporto. Journal of Clinical Periodontology, 44, 51–57. https://doi.org/10.1111/jcpe.12645
- Trombelli, L., Severi, M., Farina, R., & Simonelli, A. (2020). Tecnica del Layer Augmented Sub-periostale peri-implantare per trattare le lesioni di peri-implantite. Clinical Advances in Periodontics. https://doi.org/10.1002/ cap.10107. [Epub ahead of print].
- Trombelli, L., Severi, M., Pramstraller, M., & Farina, R. (2018). Tecnica del Layer Augmented Sub-periostale peri-implantare per l'aumento osseo orizzontale al posizionamento dell'impianto. Minerva Stomatologica, 67, 217–224. https://doi.org/10.23736/S0026-4970.18.04161-4
- Trombelli, L., Severi, M., Pramstraller, M., & Farina, R. (2019). Una gestione semplificata dei tessuti molli per l'aumento osseo peri-implantare. International Journal of Oral and Maxillofacial Implants, 34, 197–204. https://doi.org/10.11607/jomi.6959
- Urban, I. A., Wessing, B., Alández, N., Meloni, S., González-Martin, O., Polizzi, G., … Zechner, W. (2019). Uno studio controllato randomizzato multicentrico che utilizza una nuova membrana di collagene per la rigenerazione ossea guidata in siti di impianto deiscente: risultato alla consegna protesica e a 1 anno di follow-up. Clinical Oral Implant Research, 30, 487–497. https://doi.org/10.1111/clr.13426
- Zitzmann, N. U., Schärer, P., & Marinello, C. P. (2001). Risultati a lungo termine di impianti trattati con rigenerazione ossea guidata: uno studio prospettico di 5 anni. International Journal of Oral and Maxillofacial Implants, 16, 355–366.