L'uso del trattamento superficiale al plasma a vuoto per migliorare la guarigione e la rigenerazione ossea nella preservazione dell'alveolo e GBR: una serie di casi con analisi istologica
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Abstract
Scopo: Valutare i risultati clinici e istologici dei pazienti che ricevono corone supportate da impianti dopo il trattamento della superficie al plasma in vuoto (VPST) dei biomateriali utilizzati nella preservazione dell'alveolo (SP) e nella rigenerazione ossea guidata (GBR).
Materiali e metodi: Questo studio è stato progettato come una serie di casi. Sono stati arruolati pazienti che necessitavano di estrazione dentale e preservazione dell'alveolo o rigenerazione ossea guidata. La tecnica di preservazione dell'alveolo è stata eseguita dopo l'estrazione del dente utilizzando un innesto osseo in collagene eterologo e una xenomatrice in collagene, entrambi attivati con plasma in vuoto. Nel frattempo, è stata eseguita un'augmentazione orizzontale a due fasi utilizzando una rete in titanio personalizzata e un mix di innesti ossei autologhi (non trattati) e eterologhi (trattati), insieme a una membrana in collagene trattata. ACTILINK Reborn con Universal Vortex Holder (Plasmapp Co., Ltd., Daejeon, Repubblica di Corea) è stato utilizzato per trattare tutti i biomateriali. Le misure di esito erano i fallimenti degli impianti e delle protesi, le complicazioni e l'esame istologico. Campioni di tessuti molli e duri sono stati raccolti al momento dell'inserimento dell'impianto solo nei pazienti trattati con SP.
Risultati: Un totale di sei pazienti è stato trattato: tre con preservazione dell'alveolo e posizionamento dell'impianto ritardato, e tre con GBR a fasi. Nessun impianto o protesi è fallito. Una rete di titanio personalizzata si è rotta dopo il trattamento al plasma, richiedendo la sostituzione con una membrana pericardica. Non si sono verificate altre complicazioni. L'analisi istologica a tre mesi dall'intervento ha rivelato osso neoformato ben vascolarizzato in diverse fasi di maturazione con particelle di innesto osseo integrate, mentre il tessuto molle appariva strutturato fisiologicamente.
Conclusione: Il VPST può migliorare l'idrofobicità dei biomateriali, supportando risultati di guarigione favorevoli in SP e GBR. Sono necessari ulteriori studi controllati randomizzati con calcoli appropriati della dimensione del campione per confermare questi risultati preliminari.
Introduzione
L'implantologia orale è riconosciuta come una metodologia clinica sicura ed efficace in grado di garantire il successo a lungo termine nella riabilitazione orale. Le origini di questo campo medico risalgono ai primi anni '50, quando il Dr. Per-Ingvar Brånemark, un chirurgo ortopedico svedese, fece scoperte rivoluzionarie mentre conduceva esperimenti ortopedici sulle gambe dei conigli. Da allora, il campo è rapidamente evoluto, guidato dai progressi nei biomateriali e nelle tecniche chirurgiche, portando a risultati migliorati e a una maggiore soddisfazione dei pazienti.
Attualmente, un impianto è considerato osseointegrato quando non c'è movimento relativo progressivo tra l'impianto e l'osso circostante, indicando contatto diretto e stabilità. La stabilità primaria è ampiamente influenzata dall'interblocco meccanico tra la superficie dell'impianto e l'osso ospite, che dipende da fattori come la densità ossea, il design dell'impianto e la tecnica chirurgica.
Raggiungere e mantenere l'osseointegrazione a lungo termine è complesso e può essere influenzato da vari fattori biologici e meccanici. Questi includono la salute sistemica del paziente, la qualità locale dell'osso, le condizioni di carico dell'impianto e le caratteristiche superficiali dell'impianto. Studi recenti suggeriscono che modificare le superfici degli impianti per migliorare la loro compatibilità biologica può migliorare significativamente i risultati dell'osseointegrazione. Numerosi metodi di trattamento superficiale sono stati studiati e implementati per migliorare le caratteristiche superficiali biologiche degli impianti, supportando il processo di osseointegrazione per il successo sia a breve che a lungo termine. Tra questi, la rugosità superficiale e l'idrofilicità sono particolarmente significative per raggiungere un alto contatto osso-impianto (BIC). Queste caratteristiche superficiali sono progettate per fornire una migliore stabilità durante il processo di guarigione e consentire un caricamento più rapido dell'impianto accelerando il meccanismo di osseointegrazione e promuovendo una formazione ossea più forte e veloce.
Per migliorare l'osteoconduttività e l'osteoinduttività dei biomateriali per la rigenerazione ossea, è stata dimostrata la modifica della loro superficie per promuovere l'adesione cellulare, la proliferazione e la formazione di nuovo osso. Questi trattamenti includono modifiche additive come rivestimenti o modifiche sottrattive come incisioni, sabbiatura e altre. Tra i vari trattamenti dei biomateriali volti a migliorare l'osseointegrazione, il trattamento al plasma ha dimostrato significativi miglioramenti nell'adesione cellulare modificando la rugosità superficiale e la bagnabilità. L'attivazione al plasma modifica la superficie incorporando gruppi funzionali, aumentando l'energia superficiale e migliorando l'idrofilicità. Questo porta a una riduzione dell'angolo di contatto tra i fluidi biologici e la superficie dell'impianto, facilitando la diffusione delle cellule osteoblastiche senza lasciare residui dopo il trattamento. Inoltre, il trattamento al plasma induce cambiamenti nelle proprietà fisico-chimiche, inclusa l'energia libera superficiale, il contenuto di idrocarburi e la presenza di gruppi idrossilici funzionali. I recenti progressi nella tecnologia del plasma hanno reso possibile lo sviluppo di sistemi di plasma a bassa pressione in grado di trattare uniformemente geometrie di impianto complesse. Questi sistemi offrono un controllo preciso sui parametri di trattamento come potenza, composizione del gas e tempo di esposizione, consentendo modifiche superficiali su misura per migliorare la biocompatibilità. Tuttavia, nonostante i risultati promettenti in vitro, le evidenze cliniche sui biomateriali trattati al plasma rimangono limitate, necessitando ulteriori indagini. Nonostante i risultati promettenti degli studi in vitro, le evidenze cliniche sull'efficacia dei biomateriali trattati al plasma rimangono limitate, necessitando ulteriori indagini.
L'obiettivo di questo audit clinico è valutare i risultati clinici e istologici dei pazienti che ricevono corone supportate da impianti dopo VPST di biomateriali utilizzati nella preservazione dell'alveolo (SP) e nella rigenerazione ossea guidata (GBR). I risultati di questa ricerca sono destinati a informare e potenzialmente affinare i protocolli clinici esistenti, contribuendo a un approccio più accurato e prevedibile nella riabilitazione orale. Pertanto, questo audit clinico può servire come studio di prova di concetto.
Materiali e Metodi
Questo studio è stato progettato come uno studio di casi di fase IV, con materiali e dispositivi approvati CE utilizzati come parte della pratica professionale abituale e senza rischi aggiuntivi. Tutti i casi sono stati eseguiti in una clinica privata a Roma, Italia, e i dati sono stati valutati presso il Dipartimento di Medicina, Chirurgia e Farmacia, Università di Sassari, Italia. Lo studio ha rispettato i principi della Dichiarazione di Helsinki del 2013 e i principi di Buona Pratica Medica. I dati medici sono stati anonimizzati in modo che i pazienti non potessero essere identificati, e il nulla osta del comitato etico per il consenso per una serie di casi è stato ottenuto (Numero di rapporto 41/1.6; rilasciato il 21 maggio 2025).
I pazienti che necessitano di un'estrazione atraumatica di un dente senza speranza e di una procedura di preservazione dell'alveolo, così come i pazienti che necessitano di una procedura di rigenerazione ossea guidata prima dell'inserimento dell'impianto, sono stati arruolati in questa ricerca.
Criteri di inclusione:
- Pazienti con almeno un dente senza speranza nella mandibola o nel mascellare, con alveolo post-estrattivo intatto, in grado di comprendere e fornire consenso informato sono stati considerati idonei per l'inclusione per la preservazione dell'alveolo; oppure qualsiasi paziente che necessitava di una restaurazione supportata da impianto singolo e rigenerazione ossea guidata orizzontale in fasi (difetto di classe IV secondo Cawed e Howell) sia nella mandibola che nel mascellare. Un dente senza speranza è stato definito come un dente con grave danno strutturale, parodontale o endodontico che non poteva essere trattato o mantenuto in modo prevedibile ed era raccomandato per l'estrazione. I criteri comuni per classificare un dente come senza speranza includono: grave malattia parodontale con ≥75% di perdita ossea, mobilità (Grado III) o coinvolgimento della furcazione di classe III; carie estese o fratture che rendono il dente non restaurabile; trattamento endodontico non riuscito con infezione persistente; e trauma che porta a radici non vitali o grave dislocazione.
- Avere 18 anni o più e in grado di fornire consenso informato.
- I fumatori sono stati classificati come: (1) non fumatori; (2) fumatori moderati (fino a 10 sigarette/giorno); e (3) fumatori pesanti (più di 11 sigarette/giorno). I fumatori pesanti sono stati esclusi, solo le categorie 1 e 2 sono state incluse in questo studio.
- Il biotipo è stato classificato come: sottile (≤1 mm), medio (>1–<2 mm) o spesso (≥2 mm). Criteri di esclusione:
- Controindicazioni generali alla chirurgia implantare
- Pazienti irradiati nell'area della testa e del collo.
- Pazienti immunosoppressi o immunocompromessi.
- Pazienti trattati o in trattamento con amino-bisfosfonati per via endovenosa.
- Pazienti con parodontite non trattata.
- Pazienti con scarsa igiene orale e motivazione.
- Diabete non controllato.
- Fumatori pesanti (più di 11 sigarette/giorno).
- Gravidanza o allattamento.
- Abusatori di sostanze.
- Problemi psichiatrici o aspettative irrealistiche.
- Mancanza di dentizione antagonista occludente nell'area destinata all'inserimento dell'impianto.
- Pazienti con infezione e/o infiammazione nell'area destinata all'inserimento dell'impianto.
- Pazienti che partecipano ad altri studi se il presente protocollo non può essere rispettato correttamente.
- Pazienti riferiti solo per l'inserimento dell'impianto e che non possono essere seguiti presso il centro di trattamento.
- Pazienti non in grado di essere seguiti per 5 anni.
2.1. Procedura di Preservazione dell'Alveolo
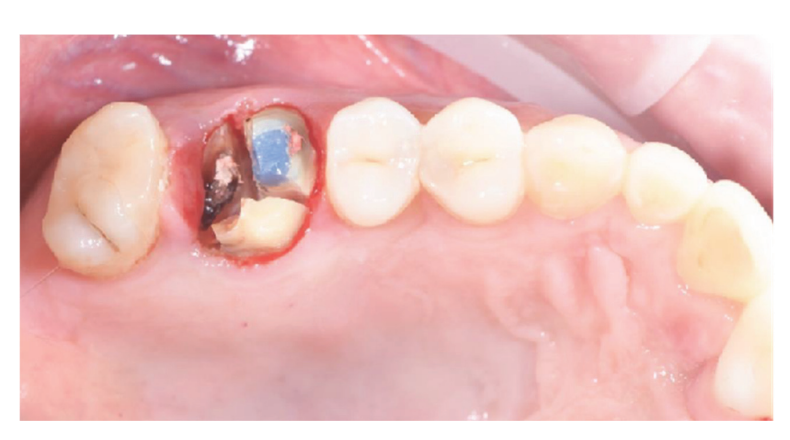
I pazienti che soddisfacevano i criteri di inclusione/esclusione (Figura 1) sono stati esaminati clinicamente in modo approfondito per la valutazione della carie dentale e della salute parodontale. Prima della procedura di preservazione dell'alveolo, i pazienti hanno subito una scansione CBCT preoperatoria per quantificare il volume osseo. Una volta confermata l'idoneità e ottenuto il consenso informato, è stata condotta un'esame orale completo per valutare la salute orale generale e identificare eventuali patologie che richiedevano trattamento prima della preservazione dell'alveolo e della riabilitazione implantare. Circa 10 giorni prima della preservazione dell'alveolo e dell'inserimento dell'impianto, tutti i pazienti hanno ricevuto un'igiene orale professionale, inclusa la detersione, se necessario. L'amministrazione di antibiotici profilattici includeva 2 g di amoxicillina un'ora prima dell'intervento chirurgico, o 600 mg di clindamicina in caso di allergia alla penicillina. I pazienti hanno anche sciacquato con collutorio al 0,2% di clorexidina per un minuto prima di qualsiasi procedura chirurgica. Tutti gli interventi chirurgici sono stati eseguiti in anestesia locale con articaina e adrenalina (1:100.000). La sedazione endovenosa era facoltativa. È stata eseguita un'estrazione dentale atraumatica senza elevazione del lembo, seguita da curettage dell'alveolo, valutazione dell'integrità alveolare e preservazione dell'alveolo (Figura 2). Gli alveoli post-estrazione sono stati riempiti con un sostituto osseo eterologo utilizzando granuli di osso equino naturale (Bioactiva, Arcugnano, Italia) e coperti con XC Collagen Xenomatrix (Bioteck S.p.A, Vicenza, Italia). Il trattamento della superficie al plasma in vuoto è stato eseguito utilizzando la macchina ACTILINK reborn (Activelink reborn, Plasmapp Co., Ltd., Daejeon, Repubblica di Corea) con un supporto personalizzato (Figura 3), secondo un protocollo pubblicato. Il tempo di ciclo del trattamento della superficie al plasma in vuoto, denominato modalità Vortex Plasma, era di 30 s.
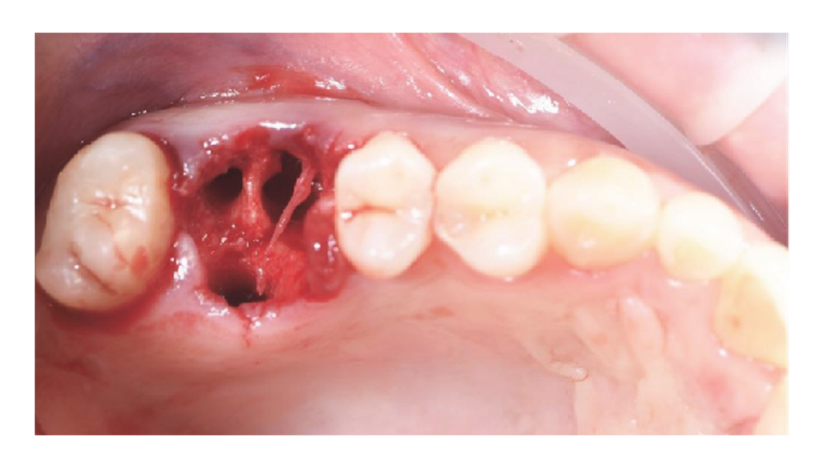

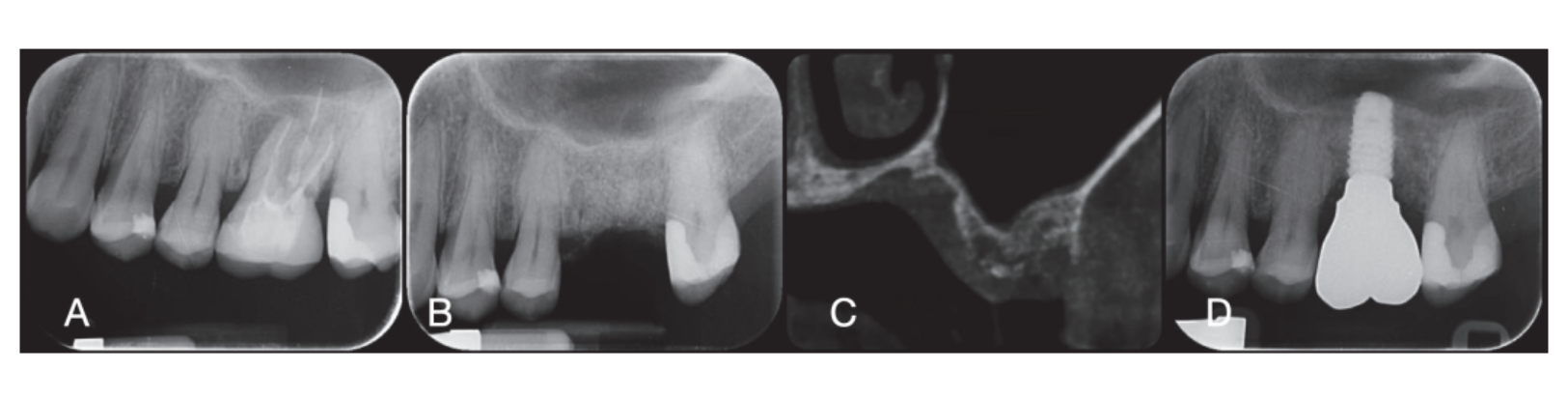
I siti chirurgici sono stati quindi chiusi con suture semplici in Vicryl 4.0 (Revello S.p.A, Verona, Italia) (Figura 4). Dopo un periodo di guarigione di tre mesi, è stata eseguita l'inserzione dell'impianto (Osstem Implant, Seoul, Repubblica di Corea) secondo le istruzioni del produttore. Campioni di tessuto istologico sono stati raccolti immediatamente prima della preparazione del sito per l'impianto (vedi Sezioni 2.3 e 2.4). I siti per l'impianto sono stati preparati a mano libera, senza un template chirurgico, utilizzando punte di diametro crescente. La qualità dell'osso è stata soggettivamente categorizzata come dura, media o morbida. La coppia motore è stata impostata a 35 Ncm durante l'inserimento dell'impianto. Gli impianti sono stati posizionati 1,5 mm al di sotto dell'osso buccale intatto, e è stato adottato un protocollo di carico immediato con una coppia di inserimento minima di 35 Ncm. È stato prescritto un trattamento analgesico post-chirurgico con ibuprofene 600 mg secondo necessità. Tutti i pazienti sono stati seguiti rigorosamente per valutare la completa guarigione. Tre o quattro mesi dopo il carico immediato, sono state prese le impronte definitive e, entro un mese, è stata consegnata una corona metal-free sostenuta da impianti e trattenuta da vite. Radiografie periapicali sono state ottenute al momento dell'inserimento dell'impianto (Figura 5).
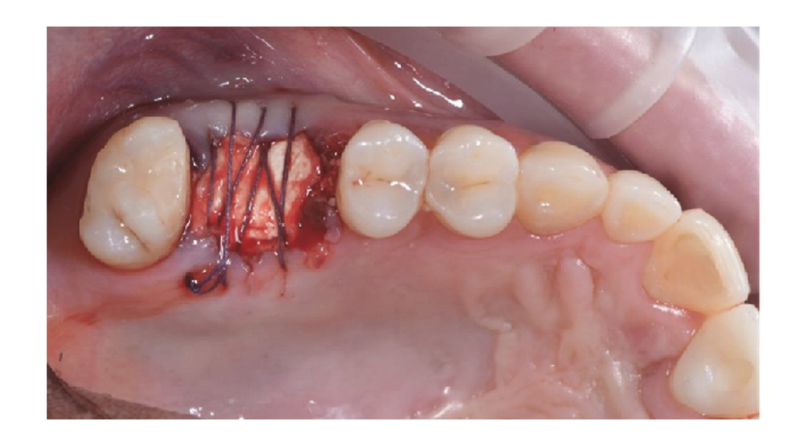
2.2. Istruzioni Post-Chirurgiche e Fase Protesica Dopo la Preservazione dell'Alveolo
È stata raccomandata una dieta morbida per 30 giorni in caso di carico immediato. È stato prescritto ibuprofene (400 mg) da assumere 2–4 volte al giorno durante i pasti, ma ai pazienti è stato detto di non assumerlo in assenza di dolore (in caso di allergia o problemi gastrici, è stato prescritto 1 g di paracetamolo invece). Inoltre, è stato raccomandato un collutorio a base di clorexidina allo 0,2% per 1 minuto due volte al giorno per 14 giorni. Non era consentito ai pazienti indossare alcuna protesi rimovibile che potesse caricare gli impianti in studio. I punti sono stati rimossi dopo 7-10 giorni e sono state fornite istruzioni per l'igiene orale.
Al momento dell'inserimento dell'impianto, sono state consegnate le restaurazioni temporanee a carico immediato. Dopo l'osseointegrazione (8 settimane), le restaurazioni temporanee sono state modificate in base alla gestione dei tessuti molli. Dopo 3-4 mesi, è stata presa un'impronta definitiva, digitale o analogica. Le restaurazioni definitive sono state consegnate entro un mese dopo aver testato la stabilità degli impianti individuali. La superficie occlusale era in leggero contatto con la dentizione opposta. Sono state effettuate radiografie periapicali e fotografie cliniche degli impianti in studio (Figura 5). Se i livelli ossei marginali peri-impiantari non erano leggibili, è stata effettuata una nuova radiografia e sono state fornite istruzioni per l'igiene orale.
2.3. Recupero della Biopsia
Dopo tre mesi, è stata eseguita l'installazione dell'impianto (Osstem Implant, Seoul, Repubblica di Corea) secondo le istruzioni del produttore. Durante la preparazione del sito dell'impianto, sono state ottenute biopsie di tessuti molli e duri utilizzando un mucotomo da 5 mm (diametro esterno) per i tessuti molli e un trapano trepanatore da 3,0 mm (diametro esterno) per i campioni ossei. I campioni di tessuto duro sono stati fissati in formalina tamponata neutra al 10% e i tessuti molli in formalina tamponata neutra al 4% per l'esame istologico.
2.4. Elaborazione dei Campioni e Analisi Istologica
I campioni di tessuto duro sono stati disidratati utilizzando una serie di etanolo in aumento. Dopo la disidratazione, i campioni sono stati infiltrati con resina metacrilica e successivamente incorporati. I blocchi sono stati sezionati utilizzando una lama di diamante e ulteriormente ridotti a uno spessore di circa 100 µm. Le sezioni sono state montate su vetrini di plastica, incollate e colorate con Blu di Toluidina e Pironina Gialla.
I campioni di tessuto molle fissati in formalina sono stati inclusi in paraffina. Sono state ottenute sezioni istologiche e colorate con ematossilina ed eosina, tricromia di Mallory e rosso di Sirius. Le sezioni sono state esaminate qualitativamente sotto un microscopio ottico a campo chiaro (Nikon Eclipse 80i, Nikon, Tokyo, Giappone) e uno scanner ad alta risoluzione a diverse ingrandimenti (Hamamatzu NanoZoomer Series S60, Hamamatzu Photonics, Hamamatsu, Giappone). Inoltre, i campioni colorati con rosso di Sirius sono stati osservati sotto luce polarizzata per valutare l'organizzazione delle fibre di collagene (Nikon Eclipse 80i, Nikon, Tokyo, Giappone).
2.5. Procedura GBR
I pazienti sono stati valutati per l'idoneità allo studio. È stata ottenuta una scansione CBCT preoperatoria per ciascun paziente per quantificare il volume osseo. I pazienti privi di un volume osseo sufficiente per il posizionamento dell'impianto sono stati informati sui dettagli dello studio e hanno firmato il modulo di consenso informato alla ricerca. Una volta confermata l'idoneità e ottenuto il consenso informato, è stata condotta un'accurata visita orale per valutare la salute generale e identificare eventuali patologie orali che richiedevano trattamento prima della rigenerazione ossea guidata (GBR) e della riabilitazione implantare. Dieci giorni prima della GBR e del posizionamento dell'impianto, tutti i pazienti hanno subito procedure professionali di igiene orale, inclusa la detersione, se necessario. I denti compromessi nei siti operatori sono stati estratti otto settimane prima della GBR e del posizionamento dell'impianto. I pazienti hanno ricevuto 2 g di amoxicillina (Zimox, Pfizer, Roma, Italia) un'ora prima dell'intervento, seguiti da 1 g due volte al giorno per due settimane. In caso di allergia alla penicillina, sono stati somministrati 600 mg di clindamicina con lo stesso regime postoperatorio. Immediatamente prima dell'intervento, i pazienti hanno sciacquato con una soluzione di clorexidina allo 0,2% (Curasept, Curaden Healthcare, Saronno, Italia) per un minuto. La procedura chirurgica è stata eseguita sotto sedazione cosciente (Diazepam, Hoffmann-La Roche, Basilea, Svizzera) e anestesia locale (Septanest con adrenalina 1/100.000, Septodont, Saint-Maur-des-Fossés, Francia). È stata effettuata un'incisione mid-crestale (leggermente avanzata buccalmente) nel tessuto keratinizzato residuo utilizzando una lama chirurgica n. 15, seguita da due incisioni verticali bilaterali a uno o due denti di distanza. È stato elevato un lembo a pieno spessore oltre il giunzione mucogengivale, almeno 5 mm oltre il difetto osseo, e il sito ricevente è stato accuratamente liberato da residui di tessuto molle. L'osso autologo è stato prelevato dal sito dell'impianto pianificato o dalla regione retro-molare mandibolare utilizzando un raccoglitore di osso corticale minimamente invasivo (Micross, Meta, Reggio Emilia, Italia). Il difetto osseo è stato quindi riempito con una miscela 50:50 di osso autologo e sostituto osseo eterologo (granuli di osso equino naturale, Bioactiva, Arcugnano, Italia), pre-trattati con Vortex Plasma utilizzando il supporto del materiale. Una rete di titanio progettata CAD/CAM, trattata al plasma (Exocad DentalCAD, Exocad, Darmstadt, Germania), personalizzata in base al contorno e alla forma della regione controlaterale (New Ancorvis Srl, Bargellino, Calderara di Reno, Italia), è stata quindi posizionata per coprire e proteggere il sito innestato. La rete di titanio personalizzata è stata fissata con due o tre viti ossee pre-pianificate e coperta con una membrana pericardica trattata al plasma (Bioactiva, Arcugnano, Italia) (Figure 6 e 7). La chiusura del lembo senza tensione è stata ottenuta utilizzando suture Vicryl 4.0. Postoperatoriamente, i pazienti hanno ricevuto 80 mg di ketoprofene (Oki, Dompé, Milano, Italia) e 4 mg/giorno di betametasone (Bentelan, Glaxo, Verona, Italia) per due giorni. È stato consigliato loro di sciacquare con clorexidina allo 0,2% (Curasept) tre volte al giorno per due settimane e consumare solo cibi morbidi per 30 giorni. Le suture sono state rimosse dopo 14-21 giorni. Radiografie periapicali di base sono state eseguite al termine della procedura, durante la riapertura, alla consegna della protesi e annualmente successivamente. L'ACTILINK Reborn con Universal Vortex Holder (Plasmapp Co., Ltd., Repubblica di Corea) è stato utilizzato per trattare tutti i biomateriali, come riportato in precedenza.

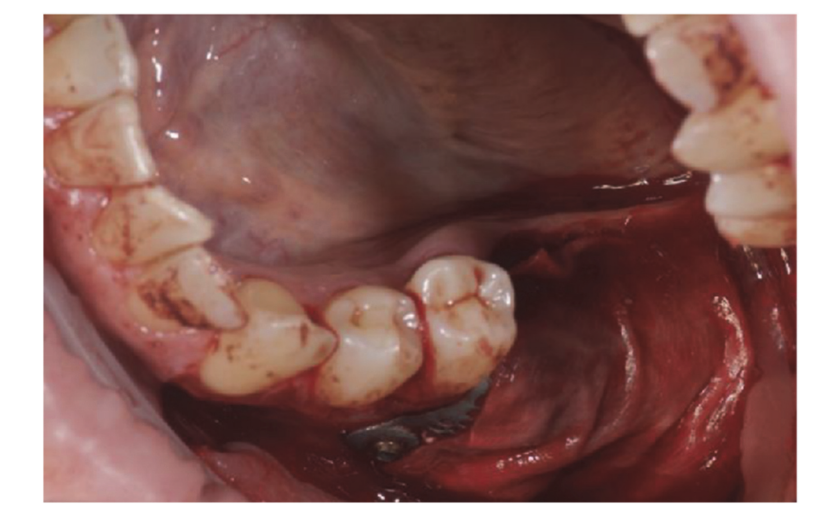
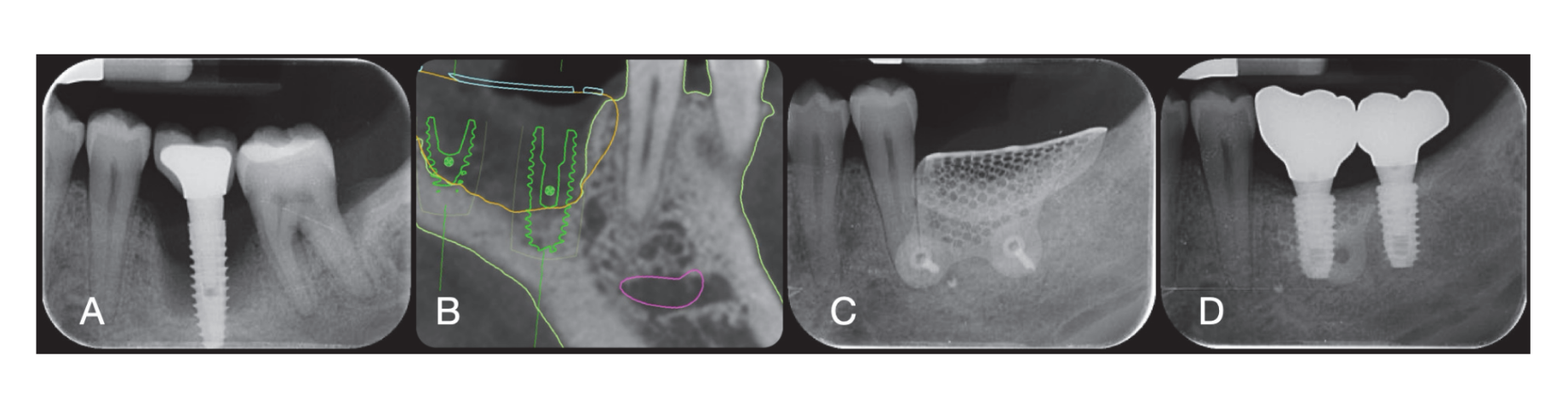
Sei mesi dopo la GBR, gli impianti sono stati posizionati seguendo il protocollo standard del produttore. Dopo l'elevazione del lembo, i siti per gli impianti sono stati preparati utilizzando punte di diametro crescente, con la qualità dell'osso categorizzata soggettivamente come dura, media o morbida. La coppia del motore è stata impostata a 25 Ncm durante l'inserimento degli impianti. Gli impianti (Osstem TSIII SOI, Osstem Implant CO., LTD., Seoul, Repubblica di Corea) sono stati posizionati in posizioni pianificate protesicamente. Poiché gli impianti avevano una superficie attivata, non è stato eseguito alcun trattamento aggiuntivo con Vortex Plasma. Gli impianti sono stati posizionati a livello crestale o leggermente al di sotto, sia a mano libera che utilizzando un template chirurgico CAD/CAM. Quattro mesi dopo il posizionamento degli impianti, gli impianti sono stati esposti e i tessuti molli sono stati gestiti secondo necessità. Sono state quindi prese impronte digitali o analogiche, e le restaurazioni temporanee sono state consegnate in base ai requisiti di gestione dei tessuti molli. Due a quattro mesi dopo, le corone definitive monolitiche in zirconia legate su Ti-link sono state consegnate dopo aver confermato la stabilità individuale degli impianti. Le superfici occlusali sono state progettate per essere in leggero contatto con la dentizione opposta. Radiografie periapicali e immagini cliniche sono state scattate durante la procedura GBR, il posizionamento degli impianti, le fasi di restauro temporaneo e definitivo (Figura 8). Sono state fornite istruzioni per l'igiene orale ad ogni visita di follow-up. La manutenzione igienica professionale è stata programmata ogni sei mesi dopo il carico definitivo e secondo necessità durante le fasi protesiche. L'occlusione dentale è stata valutata ad ogni appuntamento di follow-up.
2.6. Misure di Risultato
I risultati primari erano:
- Fallimento dell'impianto definito come mobilità, infezione, frattura e/o qualsiasi altro problema meccanico o biologico che ne ha determinato la rimozione.
- Il fallimento della protesi è stato considerato ogni volta che doveva essere sostituita.
- Qualsiasi complicazione biologica (ad es., dolore resistente ai farmaci, gonfiore, eccessivo MBL, suppurazione, ecc.) e/o tecnica (ad es., frattura del materiale di rivestimento e/o della struttura, allentamento della vite, ecc.) è stata registrata durante il follow-up.
L'obiettivo secondario era valutare la rigenerazione ossea attraverso un'analisi istologica qualitativa valutando il grado di mineralizzazione ossea.
Risultati
3.1. Risultati Clinici
Un totale di sei pazienti è stato trattato. Tre pazienti con denti compromessi e alveoli intatti dopo l'estrazione dentale hanno ricevuto una procedura di preservazione dell'alveolo e un posizionamento dell'impianto ritardato (tre mesi), mentre gli altri tre pazienti con difetti orizzontali di classe IV hanno ricevuto il posizionamento dell'impianto in combinazione con la rigenerazione ossea guidata. Sei campioni istologici in tre pazienti sono stati raccolti al momento del posizionamento dell'impianto nel gruppo di preservazione dell'alveolo. Da ciascun paziente, tessuti molli e duri sono stati prelevati tre mesi dopo la procedura di preservazione dell'alveolo, nello stesso momento dell'intervento chirurgico per l'impianto, come descritto. Un totale di sei campioni è stato raccolto e inviato per analisi istologica (tre campioni di tessuto molle e tre campioni ossei).
Un totale di sei pazienti è stato trattato. Tutti i pazienti erano donne con un'età media di 50 anni (intervallo 37-63). Nessuno dei pazienti era fumatore e tutti i pazienti erano in buona salute (ASA 1). Tutti i pazienti sono stati seguiti per almeno 1 anno dopo la consegna della protesi, senza abbandoni.
Nessun impianto o protesi è fallito fino a un anno dopo l'inserimento dell'impianto. In un paziente che ha subito una rigenerazione ossea guidata, la rete di titanio si è rotta dopo il trattamento al plasma. In questo paziente, è stata utilizzata una membrana pericardica fissata con dei tag. Non si sono verificate altre complicazioni biologiche o tecniche.
In un paziente del gruppo di preservazione del socket, al momento dell'inserimento dell'impianto, la stabilità primaria era di circa 15–20 Ncm. Tuttavia, l'impianto si è osseointegrato e la corona finale è stata consegnata.
3.2. Valutazione Istologica
Tre mesi dopo l'intervento di preservazione del socket, nessun campione istologico ha mostrato segni di infiammazione o necrosi.
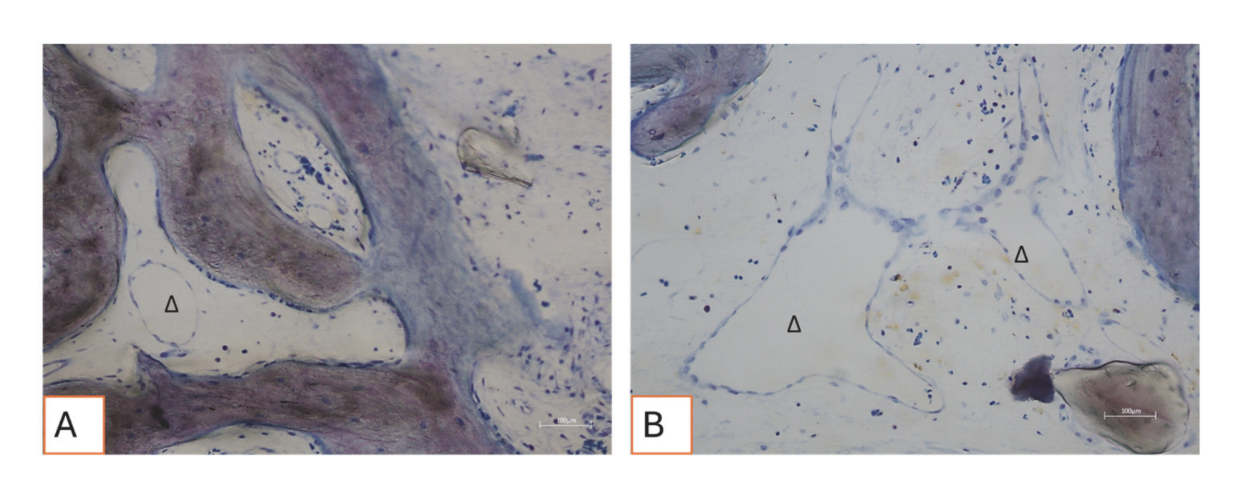
Tutti i campioni di tessuto duro hanno evidenziato nuovo osso in fase di mineralizzazione a diversi stadi (Figura 9) che circondava diverse particelle di innesto osseo, caratterizzate da numerose lacune superficiali coerenti con le lacune di riassorbimento degli osteoclasti (Figura 10). Il nuovo osso appariva ricco di cellule ossee attive, in particolare cellule simili agli osteoblasti, allineate in linee di deposizione e che secernono matrice osteoide, e cellule immature simili agli osteociti che abitano le lacune del tessuto osseo intrecciato (Figura 9). È stato osservato tessuto connettivo lasso attorno alle aree di tessuto duro, apparendo ricco di cellule e vasi sanguigni (Figura 11).
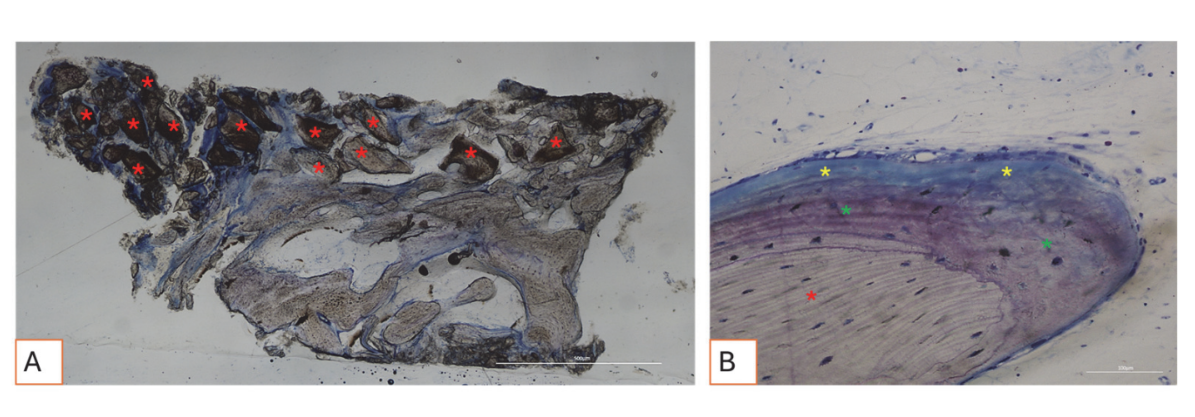
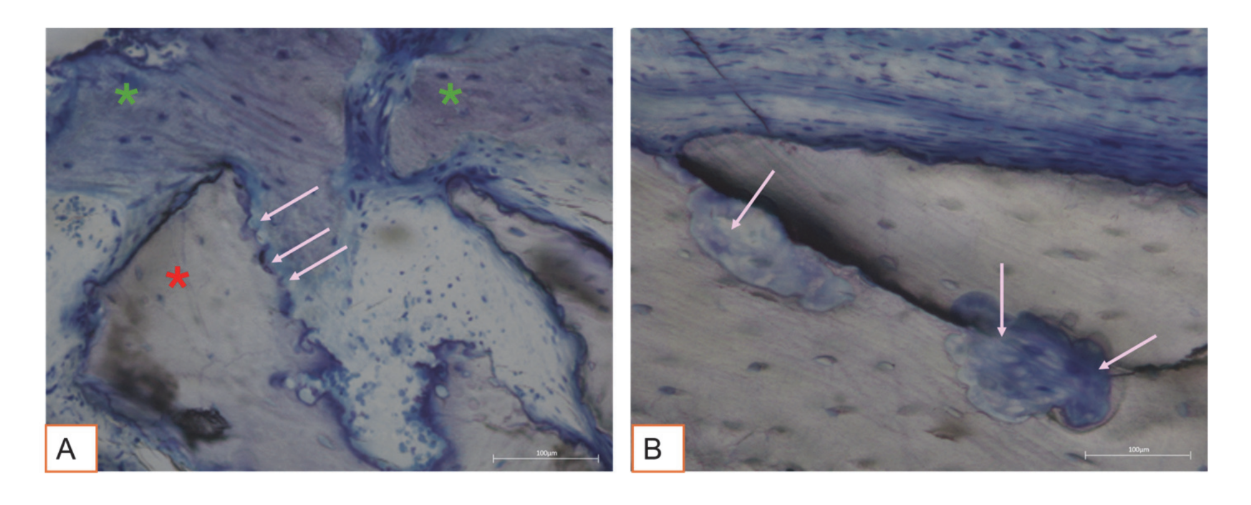
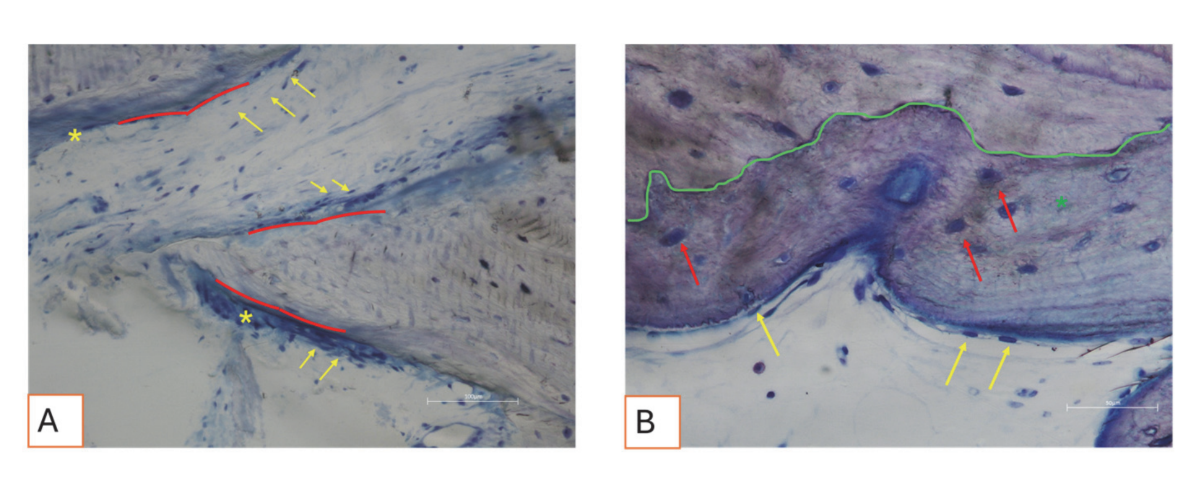
I tessuti molli hanno mostrato una morfologia fisiologica. Il componente connettivo era leggermente fibrotico, coerente con la guarigione post-chirurgica (Figure 12 e 13).

Discussione
Questo studio ha investigato l'impatto della VPST sui biomateriali utilizzati nelle procedure di SP e GBR, valutando la sua influenza sull'idrofobicità superficiale e sui risultati di guarigione. I risultati indicano che il trattamento al plasma migliora la compatibilità biologica dei biomateriali, promuovendo una efficace osteointegrazione e risposte di guarigione favorevoli.
L'analisi istologica a tre mesi non ha mostrato segni di necrosi, infiammazione o cicatrici. Sia i tessuti molli che quelli duri hanno mostrato architetture fisiologiche con buona vascolarizzazione. I tessuti duri rigenerati post-chirurgia hanno rivelato la presenza di cellule ossee attive che secernono matrice osteoide e nuovo tessuto osseo, coerente con il tempo di guarigione previsto. Questi risultati sono in linea con studi precedenti che riportano che la formazione ossea precoce è caratterizzata dalla deposizione di una matrice osteoide, che si mineralizza progressivamente nel tempo. Le particelle di innesto osseo erano ben integrate nel nuovo osso formato. Interessantemente, molte di queste particelle mostrano lacune superficiali compatibili con la riassorbimento osteoclastico. Gli osteoclasti umani coltivati per 21 giorni sulla superficie di granuli di osso equino deproteinizzato (DEBGs) e granuli di osso bovino deproteinizzato (DBBGs) hanno riassorbito i biomateriali, mostrando marcatori osteoclastici tipici e caratteristiche morfologiche più attive sui DEBGs rispetto ai DBBGs. Questi risultati suggeriscono che i DEBGs supportano la differenziazione degli osteoclasti e l'attività resorptiva. Inoltre, Di Stefano et al., in uno studio clinico e istomorfometrico condotto sei mesi dopo l'innesto del sito, hanno riportato che i DEBGs erano associati a una quantità significativamente maggiore di nuovo osso formato e a una percentuale inferiore di biomateriale residuo rispetto ai DBBGs. Alla luce dei nostri risultati, la presenza di lacune di riassorbimento osservate sulla superficie dei DEBGs potrebbe essere attribuita alle proprietà intrinseche del materiale stesso, che sembrano essere ulteriormente potenziate dal trattamento VPST. Inoltre, la VPST migliora la rugosità superficiale e la bagnabilità, promuovendo una migliore differenziazione cellulare e formazione di apatite, che sono cruciali per una rigenerazione ossea di successo. L'analisi del tessuto duro, infatti, ha rivelato numerose linee di deposizione ossea, caratterizzate dalla presenza di cellule simili agli osteoblasti che secernono attivamente matrice osteoide. L'attività secretoria degli osteoblasti gioca un ruolo critico nella formazione di nuovo osso e nell'integrazione di successo del biomateriale all'interno del tessuto ospite. Questi risultati hanno confermato che il trattamento VPST non ha compromesso le proprietà osteoconduttive dell'innesto DEBG, supportando così la sua compatibilità con i processi fisiologici di rigenerazione ossea. Inoltre, l'azione simultanea della deposizione di matrice mediata dagli osteoblasti e del riassorbimento mediato dagli osteoclasti forma la base del rimodellamento osseo fisiologico.
Questo processo dinamico è strettamente regolato attraverso un complesso dialogo cellulare tra questi due tipi di cellule.
Per quanto riguarda il tessuto molle, l'analisi istologica ha evidenziato un'architettura fisiologica con un componente connettivo leggermente fibrotico, coerente con la guarigione post-chirurgica. Questi risultati sono in linea con quelli di Pellegrini et al. che hanno descritto la progressione della guarigione del tessuto molle dopo procedure di innesto osseo nelle tecniche di preservazione dell'alveolo. La presenza di leggera fibrosi nel tessuto connettivo può essere interpretata come parte della fase normale di rimodellamento, in cui i fibroblasti contribuiscono alla deposizione della matrice extracellulare e alla maturazione del tessuto.
Clinicamente, non sono stati registrati fallimenti di impianti o protesi fino a un anno dopo il posizionamento dell'impianto, sottolineando l'affidabilità clinica dei biomateriali trattati al plasma. Questo è coerente con studi precedenti che hanno riportato un miglioramento della stabilità degli impianti e dei tassi di sopravvivenza associati a superfici attivate al plasma. L'assenza di complicazioni biologiche o tecniche, ad eccezione della rottura isolata della rete di titanio, supporta ulteriormente la sicurezza clinica e l'efficacia del protocollo di trattamento proposto. L'interazione del plasma in vuoto con oggetti biologici può anche avere effetti avversi che devono essere considerati. Una possibile spiegazione per la rottura della rete di titanio è che la rete di titanio sia stata trattata immediatamente dopo essere stata testata sul difetto osseo. La presenza di fluidi biologici potrebbe aver causato un'iperattivazione della superficie.
Per quanto a conoscenza degli autori, questo è il primo studio a valutare il VPST sui biomateriali. Nonostante questi risultati promettenti, questo studio presenta alcune limitazioni. La piccola dimensione del campione e la natura di un audit clinico limitano la generalizzabilità dei risultati. Inoltre, la mancanza di un gruppo di controllo impedisce un confronto diretto tra biomateriali trattati al plasma e non trattati. Studi futuri dovrebbero includere trial controllati randomizzati più ampi con follow-up a lungo termine per convalidare questi risultati preliminari e stabilire linee guida cliniche robuste.
Conclusioni
Considerando la dimensione limitata del campione, questa serie di casi preliminari dimostra che il VPST può migliorare la compatibilità biologica dei biomateriali utilizzati nelle procedure di SP e GBR. Questi risultati preliminari possono suggerire che il trattamento al plasma potrebbe essere integrato in modo sicuro nei protocolli clinici per migliorare potenzialmente i risultati della riabilitazione orale. Sono necessari ulteriori trial controllati randomizzati con calcolo della dimensione del campione per confermare questi risultati preliminari e per esplorare l'impatto a lungo termine sulla sopravvivenza degli impianti e sulla soddisfazione del paziente.
Marco Tallarico, Michele Troia, Milena Pisano, Silvio Mario Meloni, Dario Melodia, Claudia Della Via, Dolaji Henin, Francesco Mattia Ceruso, Carlotta Cacciò e Aurea Immacolata Lumbau
Riferimenti
- Busenlechner, D.; Fürhauser, R.; Haas, R.; Watzek, G.; Mailath, G.; Pommer, B. Successo a lungo termine degli impianti presso l'Accademia di Implantologia Orale: follow-up di 8 anni e analisi dei fattori di rischio. J. Periodontal Implant. Sci. 2014, 44, 102–108. [CrossRef] [PubMed]
- Kim, T.I. Un tributo al Dr. Per-Ingvar Brånemark. J. Periodontal Implant. Sci. 2014, 44, 265. [CrossRef] [PubMed]
- Mavrogenis, A.F.; Dimitriou, R.; Parvizi, J.; Babis, G.C. Biologia dell'osseointegrazione degli impianti. J. Musculoskelet. Neuronal Interact. 2009, 9, 61–71.
- Gallucci, G.O.; Hamilton, A.; Zhou, W.; Buser, D.; Chen, S. Protocolli di posizionamento e carico degli impianti in pazienti parzialmente edentuli: una revisione sistematica. Clin. Oral Implant. Res. 2018, 29 (Suppl. S16), 106–134. [CrossRef]
- Wong, M.; Eulenberger, J.; Schenk, R.; Hunziker, E. Effetto della topologia superficiale sull'osseointegrazione dei materiali impiantari nell'osso trabecolare. J. Biomed. Mater. Res. 1995, 29, 1567–1575. [CrossRef]
- Wennerberg, A.; Albrektsson, T. Sulle superfici degli impianti: una revisione delle conoscenze e opinioni attuali. Int. J. Oral Maxillofac. Implant. 2010, 25, 63–74.
- Wennerberg, A.; Albrektsson, T. Effetti della topografia superficiale del titanio sull'integrazione ossea: una revisione sistematica. Clin. Oral Implant. Res. 2009, 20 (Suppl. S4), 172–184. [CrossRef]
- Kazimierczak, P.; Przekora, A. Modifiche superficiali osteoconduttive e osteoinduttive dei biomateriali per la rigenerazione ossea: una revisione concisa. Coatings 2020, 10, 971. [CrossRef]
- Canullo, L.; Genova, T.; Chinigò, G.; Iacono, R.; Pesce, P.; Menini, M.; Mussano, F. Dispositivo di trattamento al plasma sotto vuoto per migliorare l'attività dei fibroblasti su superfici di titanio lavorate e ruvide. Dent. J. 2024, 12, 71. [CrossRef] [PubMed]
- Shibata, Y.; Hosaka, M.; Kawai, H.; Miyazaki, T. Il trattamento al plasma a scarica luminosa delle lastre di titanio migliora l'adesione delle cellule simili agli osteoblasti alle lastre attraverso un meccanismo mediato dagli integrini. Int. J. Oral Maxillofac. Implant. 2002, 17, 771–777.
- Noro, A.; Kaneko, M.; Murata, I.; Yoshinari, M. Influenza della topografia superficiale e della fisico-chimica superficiale sulla bagnabilità della zirconia (zirconia poliacristallina tetragonale). J. Biomed. Mater. Res. Part B Appl. Biomater. 2013, 101, 355–363. [CrossRef] [PubMed]
- Tallarico, M.; Meloni, S.M.; Troia, M.; Cacciò, C.; Lumbau, A.I.; Gendviliene, I.; Ceruso, F.M.; Pisano, M. L'uso del trattamento superficiale al plasma sotto vuoto per migliorare l'idrofilicità e la bagnabilità dei biomateriali: uno studio in vitro. Dent. J. 2025, 13, 141. [CrossRef] [PubMed]
- Canullo, L.; Pellegrini, G.; Canciani, E.; Heinemann, F.; Galliera, E.; Dellavia, C. Tecnica di preservazione dell'alveolo: effetto del biomateriale sul modello rigenerativo osseo. Ann. Anat. Anat. Anz. 2016, 206, 73–79. [CrossRef] [PubMed]
- Lorusso, F.; Alla, I.; Gehrke, S.A.; Carmine, M.D.; Tari, S.R.; Scarano, A. Effetto di diversi giunti protesici per impianti dentali sulla perdita ossea marginale: risultati emergenti da un'analisi di rete bayesiana (NMA) e revisione sistematica. Prosthesis 2024, 6, 186–205. [CrossRef]
- Udeabor, S.E.; Heselich, A.; Al-Maawi, S.; Alqahtani, A.F.; Sader, R.; Ghanaati, S. Conoscenze attuali sulla guarigione dell'alveolo estrattivo: una revisione narrativa. Bioengineering 2023, 10, 1145. [CrossRef]
- Perrotti, V.; Nicholls, B.M.; Piattelli, A. Formazione e attività degli osteoclasti umani su un sostituto osseo spongioso equino. Clin. Oral Implant. Res. 2009, 20, 17–23. [CrossRef]
- Di Stefano, D.A.; Zaniol, T.; Cinci, L.; Pieri, L. Confronto chimico, clinico e istomorfometrico tra osso equino prodotto attraverso eliminazione enzimatica degli antigeni e osso bovino reso non antigenico utilizzando un processo ad alta temperatura in innesti di alveolo post-estrattivo. Uno studio clinico retrospettivo comparativo. Dent. J. 2019, 7, 70. [CrossRef]
- Le, P.T.M.; Shintani, S.A.; Takadama, H.; Ito, M.; Kakutani, T.; Kitagaki, H.; Terauchi, S.; Ueno, T.; Nakano, H.; Nakajima, Y.; et al. Trattamento di bioattivazione con acido misto e calore su impianti in titanio fabbricati mediante fusione laser selettiva migliora la differenziazione delle cellule preosteoblastiche. Nanomaterials 2021, 11, 987. [CrossRef]
- Pellegrini, G.; Rasperini, G.; Obot, G.; Farronato, D.; Dellavia, C. Guarigione dei tessuti molli nella tecnica di preservazione dell'alveolo: valutazioni istologiche. Int. J. Periodontics Restor. Dent. 2014, 34, 531–539. [CrossRef]
- Kahm, S.H.; Lee, S.H.; Lim, Y.; Jeon, H.J.; Yun, K.I. Osseointegrazione degli impianti dentali dopo trattamento superficiale al plasma sotto vuoto in vivo. J. Funct. Biomater. 2024, 15, 278. [CrossRef]
- Pesce, P.; Menini, M.; Santori, G.; Giovanni, E.; Bagnasco, F.; Canullo, L. Attivazione foto e plasma delle superfici in titanio degli impianti dentali. Una revisione sistematica con meta-analisi di studi preclinici. J. Clin. Med. 2020, 9, 2817. [CrossRef] [PubMed]
- Scribante, A.; Ghizzoni, M.; Pellegrini, M.; Pulicari, F.; Manfredini, M.; Poli, P.P.; Maiorana, C.; Spadari, F. Maglie personalizzate completamente digitali nelle procedure di rigenerazione ossea guidata: una revisione esplorativa. Prosthesis 2023, 5, 480–495. [CrossRef]
- Berger, M.B.; Bosh, K.B.; Cohen, D.J.; Boyan, B.D.; Schwartz, Z. Trattamento al plasma da banco delle superfici in titanio migliora la risposta cellulare. Dent. Mater. 2021, 37, 690–700. [CrossRef] [PubMed]