Polietereeterchetone nella Protesi Implantare: Una Revisione Scoping
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Scopo: Condurre una revisione della letteratura disponibile sull'applicazione del polietere eterechetone (PEEK) nella protesi implantare, mappare la letteratura disponibile per evidenziare possibili lacune nella conoscenza e, se possibile, estrarre linee guida cliniche.
Materiali e Metodi: La letteratura sul PEEK nella protesi implantare pubblicata fino ad agosto 2018 è stata identificata tramite una ricerca online nei database MEDLINE (tramite PubMed), Science Direct, Embase (tramite Ovid) e Google Scholar. Sono state effettuate sintesi qualitative e quantitative per studi di ricerca originali.
Risultati: È stato riscontrato che il numero di studi di ricerca originali pubblicati era limitato. È stato trovato che il PEEK veniva applicato come materiale nella fabbricazione di strutture di protesi dentale fisse supportate da impianti (IFDP) (43%), abutment protesici per impianti (35%), viti per abutment di impianti (15%) e clip di ritenzione su barre implantari (7%). Solo il 38% degli studi erano studi clinici, mentre il 15% erano osservazionali e il 47% erano in vitro. Gli studi identificati non hanno permesso di stimare la sopravvivenza a lungo termine né i tassi di successo per nessuno dei componenti protesici. I risultati hanno consentito solo una valutazione preliminare a breve termine delle strutture IFDP in PEEK, che hanno presentato una sopravvivenza soddisfacente ma tassi di successo allarmanti nel primo anno di servizio.
Conclusione: Alla luce della scarsità di prove sulla validità del PEEK come materiale implantoprotesico, il suo utilizzo non può ancora essere approvato. I clinici dovrebbero prestare attenzione ai protocolli suggeriti per migliorare le prestazioni meccaniche e ridurre l'incidenza delle complicazioni protesiche. È necessaria ulteriore ricerca di alta qualità per una migliore comprensione della validità del materiale.
I materiali plastici hanno un'ampia gamma di applicazioni oggi, e ci sono molte diverse categorie di polimeri disponibili. I polimeri ad alte prestazioni sono plastiche che soddisfano requisiti rigorosi per stabilità termica, resistenza chimica e proprietà meccaniche. Poiché le loro formulazioni possono essere modificate secondo necessità, questi materiali possono essere progettati favorendo una di queste caratteristiche rispetto alle altre per raggiungere obiettivi specifici. I polimeri ad alte prestazioni trovano molte applicazioni in molti campi diversi, come ingegneria, industria e medicina (cioè, dispositivi medici).
Il polietereeterchetone (PEEK) è un polimero termoplastico semi-cristallino poliaromatico con proprietà meccaniche favorevoli per applicazioni biomediche. Incorporando particelle di idrossiapatite in una matrice di PEEK, alcuni autori hanno ottenuto un polimero composito che ha mostrato una resistenza a trazione compresa tra 49,0 e 83,3 MPa, che corrisponde ai limiti inferiori dell'osso corticale (50-150 MPa). Grazie al suo comportamento elastico, simile a quello dell'osso umano, il PEEK è ampiamente utilizzato nella chirurgia spinale, nella chirurgia ortopedica e nella chirurgia maxillo-facciale come sostituto dell'osso e della cartilagine.
Il PEEK è stato introdotto per la prima volta in tre forme di versioni non riempite: PEEK-LT1, PEEK-LT2 e PEEK-LT3. Successivamente, sono stati aggiunti riempitivi come ceramiche, idrossiapatite, fosfato di calcio beta e fibre di carbonio alla formula del PEEK per aumentarne la bioattività e migliorare le sue proprietà meccaniche, portando a materiali come BioHPP (Bredent). Molte versioni di PEEK riempito sono ora utilizzate per la produzione di impianti biomedici. Grazie alle sue favorevoli proprietà meccaniche, il PEEK ha raggiunto anche il campo dell'odontoiatria, dove è stato implementato in diverse aree. Combinando le sue proprietà con la diffusione in corso della tecnologia CAD/CAM, i componenti in PEEK possono ora essere progettati digitalmente e successivamente stampati in 3D, raggiungendo un'alta precisione per soddisfare i requisiti clinici.
Una varietà di recensioni ha discusso le applicazioni del PEEK nell'implantologia orale e nella protesi dentale supportata da denti, che includono componenti per protesi dentali fisse supportate da denti (FDP), protesi dentali rimovibili supportate da denti (RDP), nanocompositi bioattivi e impianti dentali.
Il PEEK è stato inizialmente introdotto nel campo della protesi implantare come materiale per la fabbricazione di componenti di restauro temporaneo come i monconi implantari, grazie alla sua fattibilità di fabbricazione con CAD/CAM, al suo prezzo accessibile e alle sue migliori prestazioni meccaniche rispetto ai materiali in resina comuni. Tuttavia, non sono stati identificati articoli di revisione che si concentrino esclusivamente sul ruolo del PEEK nella protesi implantare. È stato riportato da diversi autori che le evidenze riguardanti il PEEK in odontoiatria sono ancora limitate in quantità; pertanto, una revisione esplorativa sembra essere il tipo di articolo di revisione più appropriato da condurre su questo argomento per valutare se sia indicato condurre una ulteriore revisione sistematica sull'applicazione di questo polimero nella protesi implantare. Pertanto, la presente revisione esplorativa è stata condotta per mappare sistematicamente la ricerca effettuata in quest'area, così come per identificare eventuali lacune esistenti nella conoscenza riguardante il comportamento del materiale PEEK quando applicato come componente protesico implantare. È stata formulata la seguente domanda di ricerca: Cosa è noto dalla letteratura riguardo all'applicazione del PEEK nella protesi implantare?
Materiali e metodi
È stata effettuata una ricerca della letteratura nelle seguenti banche dati: MEDLINE tramite PubMed, Science Direct e Google Scholar.
È stata applicata la seguente strategia di ricerca per parole chiave: PEEK O polietereterechetone O polietere-etere-chetone O polimero ad alte prestazioni O polimero ad alte prestazioni O BioHPP E (odontoiatria O implantoprotesi). Come filtro di ricerca, sono stati considerati solo articoli pubblicati fino al 31 agosto 2018. Inoltre, sono state esaminate anche le liste di riferimento e gli articoli di revisione precedenti per articoli pertinenti. Per quanto riguarda il database di Google Scholar, sono stati considerati solo i primi 300 risultati, come suggerito da Haddaway et al. Non è stato registrato alcun protocollo di revisione per questo lavoro.
È stata seguita la checklist PRISMA Extension for Scoping Reviews (PRISMA-ScR) come linea guida per la corretta segnalazione degli elementi richiesti per questo tipo di revisione. È stata effettuata una valutazione iniziale dell'idoneità degli articoli esaminando titoli e abstract, seguita da un'analisi del testo completo. I titoli e gli abstract dei risultati della ricerca sono stati inizialmente esaminati da due revisori (A.P. e G.P.) per una possibile inclusione. Per evitare di escludere articoli potenzialmente pertinenti, sono stati inclusi abstract che fornivano un risultato poco chiaro nell'analisi del testo completo. I testi completi di tutti gli studi potenzialmente pertinenti sono stati ottenuti per una valutazione indipendente da parte dei due revisori rispetto ai criteri di inclusione dichiarati.
I disaccordi sono stati portati a un revisore indipendente (M.G.) e risolti attraverso discussioni.
Per essere inclusi nella valutazione preliminare, i seguenti criteri dovevano essere soddisfatti dall'articolo: abstract presente; relativo al PEEK nelle sue presentazioni non riempite e riempite; e relativo all'odontoiatria.
Per essere inclusi nelle sintesi qualitative e quantitative, i seguenti criteri dovevano essere soddisfatti: articoli che discutono le applicazioni del PEEK nella protesi implantare che registravano variabili collegate al componente protesico pertinente.
Non sono state fatte discriminazioni riguardo al processo di fabbricazione del materiale, alla sua composizione, alla sua modifica superficiale o alle sue procedure di rivestimento. Solo articoli di ricerca originali e relazioni di casi sono stati considerati per le analisi qualitative e quantitative. Le revisioni storiche e sistematiche, i capitoli di libri e le lettere al direttore sono state escluse dalle analisi; tuttavia, se ritenute pertinenti, sono state utilizzate per contestualizzare il background del materiale.
Un autore indipendente ha effettuato la raccolta dei dati, con l'obiettivo di estrarre informazioni riguardanti la dimensione del campione, il periodo di follow-up, il tasso di sopravvivenza, il tasso di successo, la resistenza alla frattura della restaurazione, la resistenza alla frattura del componente protesico e le complicazioni. È stata eseguita un'analisi statistica descrittiva per i dati ritenuti idonei. Per gli studi umani e animali che riportavano le informazioni necessarie, sono stati calcolati i mezzi aritmetici ponderati per i tassi di sopravvivenza e di successo. La sopravvivenza è stata considerata come la presenza del componente protesico all'interno della bocca al momento dell'osservazione. Il successo è stato considerato come l'assenza di complicazioni al momento dell'osservazione. Nel caso in cui i tassi di sopravvivenza e di successo riguardanti la stessa applicazione del materiale fossero disponibili da più studi, i dati umani e animali sono stati aggregati separatamente. L'accordo inter-esaminatore è stato calcolato utilizzando le statistiche κ.
Risultati
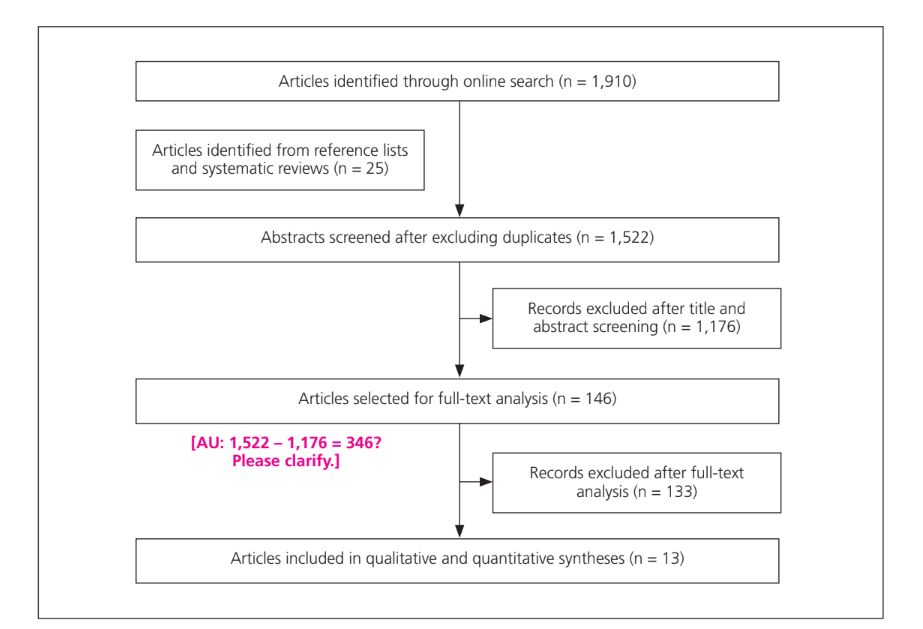
Un totale di 1.910 articoli è stato identificato dalle tre banche dati cercate (MEDLINE, Science Direct e Google Scholar) (Fig 1). Dopo aver controllato i duplicati, i titoli e gli abstract di 1.522 articoli sono stati esaminati. Di questi articoli, 146 sono stati selezionati per una valutazione del testo completo; di questi, 13 sono stati inclusi nei riassunti qualitativi e quantitativi dopo una revisione del testo completo (Tabella 1). Durante lo screening degli abstract, è stato calcolato un valore κ di 0,91 per l'accordo inter-esaminatore, e durante l'analisi del testo completo, è stato osservato un valore κ di 0,83. Le discrepanze sono state risolte attraverso discussioni tra i revisori. Sono stati identificati diversi disegni di studio. Gli studi clinici in vivo costituivano il 38% (5 studi) del totale, ma solo 2 avevano un disegno controllato e solo 1 era randomizzato. Gli studi osservazionali in vivo costituivano il 15% (2 studi) del totale, mentre la ricerca in vitro costituiva il 47% (6 studi) del totale.
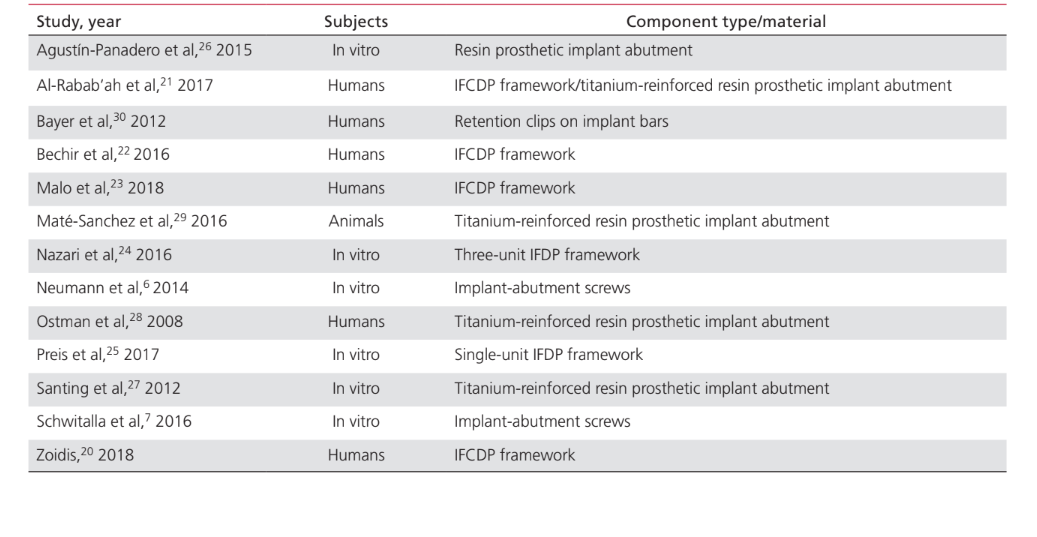
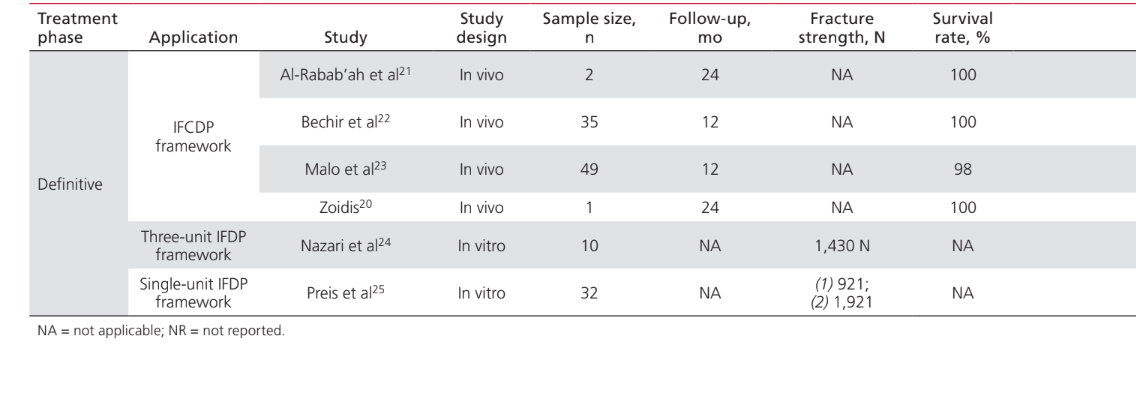
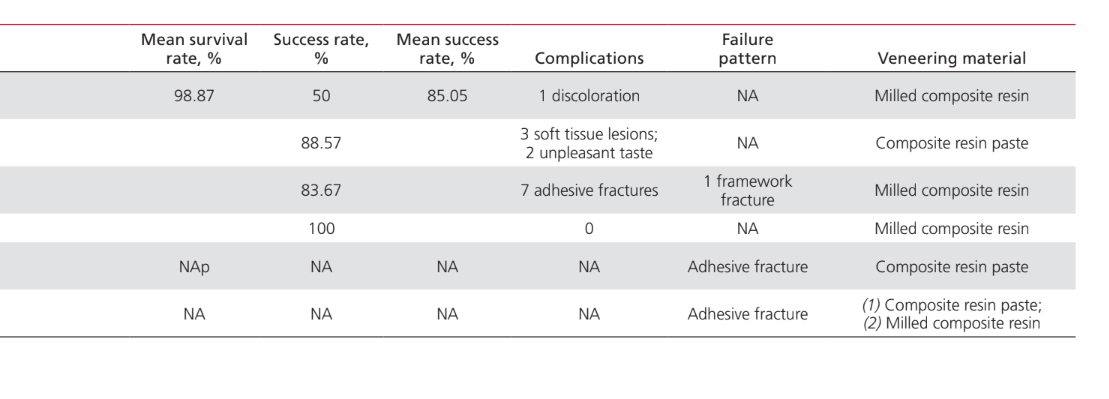
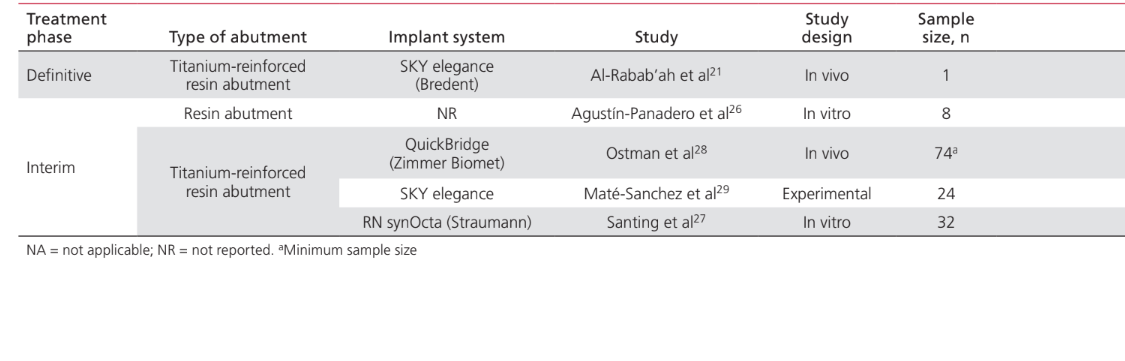
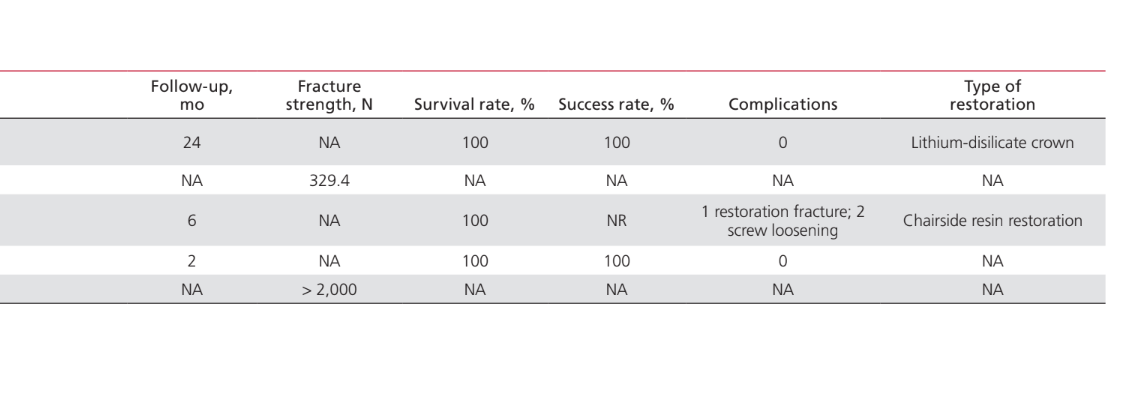
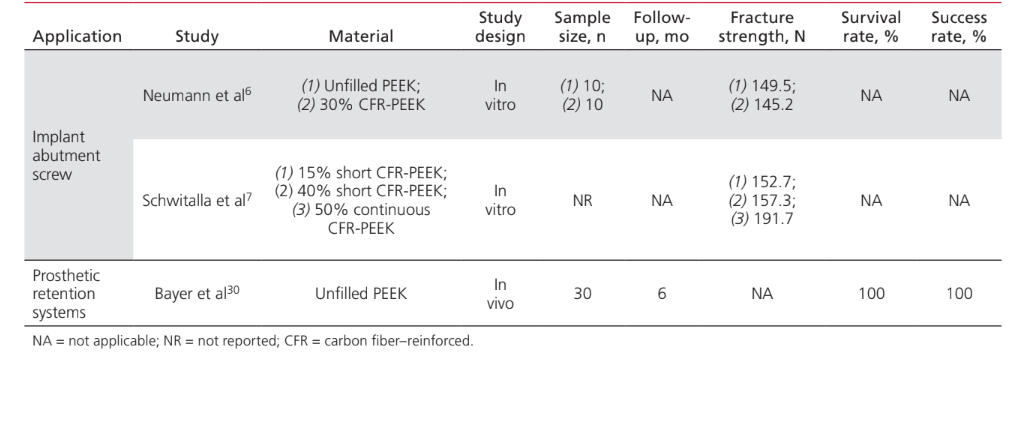
Le applicazioni del PEEK come materiale per la fabbricazione di componenti coinvolti nelle procedure di riabilitazione implantoprotesica erano: telai IFDP (43%); abutment protesici per impianti (35%); viti per abutment di impianti (15%); e clip di ritenzione per attaccare le protesi dentali alle barre implantari (7%). Gli studi sull'applicazione del PEEK come materiale per la fabbricazione di abutment di guarigione per impianti non sono stati inclusi in questo documento, poiché sono stati considerati più strettamente correlati all'aspetto chirurgico piuttosto che a quello protesico del trattamento. La Tabella 2 elenca gli studi che coinvolgono il PEEK come materiale per telai per IFDP. Non sono stati trovati studi in vivo che fornissero un gruppo di controllo; solo 2 serie di casi. Sono stati identificati due studi clinici non controllati e 2 studi in vitro. Le unità di design protesico identificate erano protesi dentali fisse complete supportate da impianti (IFCDP); IFDP a tre unità; e IFDP a singola unità. Gli IFDP a singola unità e a tre unità situati posteriormente fornivano informazioni riguardanti solo la resistenza alla frattura, mentre nessuna informazione sulla resistenza alla frattura è stata registrata per gli elementi situati anteriormente, né per gli IFCDP. Negli IFDP parziali, il modello di fallimento è stato trovato essere da frattura adesiva tra il telaio e i materiali di rivestimento in tutti i campioni testati per la resistenza alla frattura. Dei quattro studi in vivo che riportano informazioni sugli IFCDP, sono state identificate 87 protesi. Le medie aritmetiche ponderate hanno mostrato che, nei primi 12 mesi dopo la riabilitazione protesica, gli IFCDP avevano un tasso medio di sopravvivenza del 98,87% e un tasso medio di successo dell'85,05%. È stato identificato un tasso di incidenza del 16% per l'insorgenza di complicazioni nei primi 12 mesi. Di quelle complicazioni, il 64,28% si è rivelato di natura meccanica, mentre il 35,72% erano biologiche. Tra le complicazioni meccaniche, il 77,8% riguardava fratture adesive tra il telaio e i materiali di rivestimento, l'11,1% riguardava la frattura del materiale del telaio e l'11,1% erano segnalazioni di scolorimento della protesi. Tra le complicazioni biologiche c'erano l'insorgenza di lesioni dei tessuti molli e un sapore sgradevole. La Tabella 3 elenca gli studi che discutono le applicazioni del PEEK come materiale per abutment protesici per impianti. È stato identificato un rapporto di caso per l'applicazione del PEEK come abutment protesico definitivo per impianti, mentre sono stati identificati due studi in vitro e due studi clinici per abutment protesici temporanei in PEEK. L'uso del PEEK in un abutment protesico definitivo in resina rinforzata con titanio ha avuto solo un rapporto di caso, che ha mostrato tassi di sopravvivenza e successo del 100% per 24 mesi. Uno studio animale controllato in vivo, che includeva 24 soggetti, ha riportato un tasso di sopravvivenza del 100% in un periodo di 2 mesi in cui è stato utilizzato il PEEK in un abutment protesico temporaneo in resina rinforzata con titanio. Gli studi che coinvolgono il PEEK come materiale per la fabbricazione di viti per abutment di impianti e clip rotonde per la ritenzione delle protesi sulle barre implantari sono elencati nella Tabella 4. Sono stati trovati solo due studi in vitro riguardanti il PEEK come materiale per viti per abutment di impianti. L'uso del PEEK per clip di ritenzione per attaccare la protesi a barre implantari rotonde è stato discusso in un solo studio clinico randomizzato, che ha mostrato tassi di successo e sopravvivenza del 100% nei primi 6 mesi.
Discussione
Le limitazioni di questa revisione includono la strategia di ricerca selezionata per i database analizzati, che è stata intenzionalmente progettata per essere più generale, poiché uno degli obiettivi era identificare tutte le possibili applicazioni del materiale nel campo di interesse. Per lo stesso motivo, un'altra limitazione relativa alla riproducibilità della ricerca online può essere l'inclusione di Google Scholar tra i database analizzati. I suoi algoritmi di ricerca portano spesso a un'ampia quantità di risultati; tuttavia, questo ha reso possibile mappare la letteratura non indicizzata negli altri database cercati in questa revisione.
Secondo le evidenze ottenute, le applicazioni del PEEK nella protesi implantare possono essere riassunte come segue.
Materiale IFDP
Il ruolo del PEEK come componente IFDP è stato quello riportato più frequentemente. Tutti gli studi che hanno discusso il PEEK come materiale IFDP definitivo hanno applicato il polimero per la fabbricazione di strutture, che sono state successivamente rivestite con materiali in resina.
La resistenza alla frattura degli IFDP in PEEK è stata descritta come inferiore a quella del nichel-cromo e della zirconia, ma clinicamente accettabile. Tuttavia, va menzionato che le informazioni riportate dagli studi in vitro inclusi in questa revisione si riferiscono a carichi di fatica statici, e non sono state fornite informazioni sulle loro prestazioni sotto stress da fatica ciclica, che è un indicatore più rilevante per il comportamento delle riabilitazioni orali. Il design di fabbricazione e il tipo di rivestimento in resina hanno anche influenzato la resistenza alla frattura, favorendo le restaurazioni cementate rispetto a quelle trattenute da vite e il rivestimento con resina composita fresata rispetto alla pasta composita.
Pertanto, in situazioni in cui la scelta tra design a vite o cementati è ugualmente indicata, si ritiene che le restaurazioni cementate offrano una migliore prestazione meccanica, e per quanto riguarda la scelta della procedura e del materiale di rivestimento, si dovrebbe preferire la resina composita fresata. Diversi procedimenti di fabbricazione hanno anche dimostrato di influenzare le proprietà meccaniche della protesi. Le restaurazioni realizzate utilizzando PEEK fresato con CAD/CAM sembrano essere più resistenti alla frattura rispetto agli elementi realizzati con altri metodi di fabbricazione.
Gli IFCDP hanno dimostrato di fornire un trattamento altamente efficace per i pazienti con edentulismo. Gli IFCDP in PEEK possono offrire un punto d'incontro ragionevole tra l'accessibilità e la facilità di riparazione degli IFDP in metallo-acrilico e la migliore prestazione meccanica degli IFCDP in zirconia e metallo-porcellana.
Nonostante il numero limitato di casi riportati, basandosi sui risultati discussi in questa revisione, gli IFCDP in PEEK sembrano avere tassi di sopravvivenza soddisfacenti (98,87%) a 12 mesi. Oltre al fatto che questa affermazione si basa su soli quattro studi, va anche notato che tutti gli studi inclusi presentano brevi periodi di follow-up; tuttavia, i risultati sono comparabili a quelli ottenuti da IFCDP in metallo-acrilico, metallo-porcellana e zirconia. D'altra parte, i tassi di successo per gli IFCDP in PEEK hanno mostrato dati più allarmanti, poiché è stata osservata un'incidenza del 16% per l'insorgenza di complicazioni a 12 mesi. Gli IFCDP rivestiti in resina di polimetilmetacrilato (PMMA) e in ceramica rivestiti in zirconia sono stati riportati con tassi di complicazione annuali del 6,6% con un tasso di sopravvivenza del 90,6%, libero da complicazioni, a 12 mesi. Questi dati suggeriscono che gli IFCDP in PEEK comportano un rischio maggiore. Tuttavia, l'incidenza delle complicazioni riportate qui dovrebbe essere interpretata considerando alcune limitazioni: in particolare, sono stati identificati solo 87 IFCDP in PEEK, con un follow-up a 12 mesi per 84 protesi e a 24 mesi per 3 protesi. Oltre al numero limitato di casi, il periodo di follow-up di 12 mesi fornisce una significatività clinica limitata nel caso di protesi definitive.
Le complicazioni biologiche, che includevano un sapore sgradevole e lesioni dei tessuti molli, costituivano il 35,72% dei casi totali osservati. Tuttavia, va notato che gli autori dello studio che riportava le alterazioni del gusto affermavano che alcuni dei pazienti soffrivano anche di condizioni sistemiche al momento della valutazione, aggiungendo così un ulteriore livello di bias al tasso di incidenza delle complicazioni. Il PEEK è stato precedentemente designato come un materiale bioinerte; tuttavia, Trindade et al hanno recentemente osservato che questo materiale provoca una maggiore attivazione immunitaria rispetto al titanio durante il processo di osseointegrazione. Gli autori hanno suggerito che la conoscenza dell'inerzia chimica del materiale fosse probabilmente basata su studi in vitro, poiché non erano disponibili informazioni riguardo al ruolo del sistema immunitario nella downregulation del processo infiammatorio durante l'interazione PEEK-ospite. Non è ancora chiaro se le lesioni dei tessuti molli osservate in questa revisione possano essere correlate all'interazione del PEEK con i tessuti ospiti o a fattori confondenti dei disegni degli studi inclusi; tuttavia, alla luce dei risultati sopra menzionati, questo potrebbe meritare ulteriori indagini.
Per quanto riguarda i guasti meccanici, il 77,8% consisteva in fratture adesive tra il telaio e i materiali di rivestimento. I modelli di guasto negli IFDP singoli e multi-unità consistevano anch'essi principalmente in fratture adesive tra il telaio e il materiale di rivestimento, il che conferma i risultati osservati per gli IFCDP. Questo dovrebbe indicare una resistenza soddisfacente per il telaio, anche se, fino ad oggi, non è stata trovata una strategia di adesione durevole e prevedibile tra un telaio in PEEK e un rivestimento composito. Le indagini future dovrebbero concentrarsi sulla ricerca del giusto equilibrio tra l'integrazione della formula PEEK con riempitivi e la scelta del giusto protocollo di condizionamento della superficie e della procedura di rivestimento per ottenere prestazioni meccaniche ottimali.
Materiale dell'Abutment Implantare
Numerosi studi in vitro e in vivo hanno riportato l'uso di abutment implantari protesici composti interamente o parzialmente di PEEK. Tuttavia, solo cinque studi hanno discusso variabili relative all'abutment che erano di interesse per questo documento.
In termini di prestazioni meccaniche, gli abutment in resina PEEK per impianti sono stati descritti come significativamente meno resistenti alla frattura rispetto agli abutment in titanio. La loro maggiore capacità di assorbimento degli urti non influisce negativamente sulla distribuzione dello stress nell'impianto o nell'osso periferico rispetto ad altri materiali di restauro e abutment. Tuttavia, questi abutment hanno mostrato una maggiore concentrazione di stress nelle corone di restauro, il che è particolarmente rilevante nel caso degli incisivi centrali dove il restauro è più sottile, suggerendo così che gli abutment in resina PEEK per impianti potrebbero richiedere precauzioni specifiche per quanto riguarda il design di un restauro della corona.
Gli abutment in resina PEEK rinforzata in titanio sono stati utilizzati in casi di carico immediato da diversi autori. Questi sistemi sono composti da un nucleo in titanio e una manica in PEEK sovrastante, che può essere rimovibile o meno, a seconda del design dell'elemento. Più recentemente, è stato introdotto sul mercato un abutment composto da un nucleo in titanio con una manica in PEEK rinforzata in ceramica. Anche se supportato da solo uno studio animale, le evidenze sembrano indicare che questo abutment è superiore al titanio in termini di adattamento ai tessuti molli. Questo abutment è anche adatto al concetto di “un abutment—una volta”, il che significa che gli abutment in PEEK rinforzati in titanio potrebbero essere utilizzati sia come abutment provvisori che definitivi.
Uno studio in vitro condotto da Santing et al ha riportato che le corone in resina composita supportate da monconi in PEEK rinforzati con titanio sono in grado di sopportare carichi statici fino a 2.000 N.
Tra le limitazioni di questo articolo c'era l'impossibilità di stimare i tassi di successo e di sopravvivenza per i monconi protesici in PEEK a causa della scarsità di informazioni in vivo e dell'eterogeneità dei sistemi identificati. Tuttavia, si può dedurre dai risultati che i monconi impiantari in PEEK rinforzati con titanio potrebbero fornire risultati superiori in termini di resistenza meccanica quando applicati come moncone temporaneo o definitivo. Pertanto, l'uso di un nucleo in titanio è preferito rispetto alla versione del componente solo in resina. Lo spessore e il processo di fabbricazione della restaurazione temporanea potrebbero essere più significativi per l'esito del trattamento con monconi in PEEK rispetto a quanto non lo siano per i monconi in titanio. La ricerca futura dovrebbe concentrarsi sulla resistenza meccanica dei monconi in PEEK rinforzati con titanio, così come sugli esiti a lungo termine in vivo.
Viti di Abutment per Impianti
I vantaggi proporzionali offerti dalle viti di abutment in PEEK sono legati alle loro proprietà di assorbimento degli urti, così come alla loro più facile rimozione in caso di frattura grazie ai loro coefficienti di attrito più bassi. Quando testate per la resistenza alla frattura rispetto al titanio, le viti in PEEK si sono dimostrate 5 volte meno resistenti, e non sono state trovate differenze tra le versioni non riempite e quelle riempite con fibra di carbonio del materiale. Tuttavia, gli autori non hanno fornito alcuna descrizione del design in fibra di carbonio. In uno studio più recente, Schwitalla et al hanno riportato che le viti in PEEK riempite con fibre di carbonio corte (con una composizione fino al 40%) mostravano un comportamento meccanico simile a quello riportato da Neumann et al. e hanno anche osservato un aumento del 20% della resistenza alla trazione quando il PEEK era riempito con una composizione di fibra di carbonio continua di almeno il 50%.
È stato dimostrato che l'aggiunta di cemento PMMA migliora la resistenza meccanica delle viti in PEEK rinforzate con fibra di carbonio.
Il design della connessione tra l'impianto e la restaurazione è un altro fattore che potrebbe influenzare le prestazioni meccaniche della vite di abutment. Poiché le viti di abutment in PEEK hanno una maggiore tendenza a subire deformazioni plastiche rispetto al titanio, le relazioni tra le diverse connessioni degli impianti e i design delle viti dovrebbero essere ulteriormente investigate.
La prossima sfida per le viti di abutment in PEEK consisterà nel trovare il giusto equilibrio nella composizione del riempitivo in termini di quantità e struttura, nel materiale dell'abutment e nel design della connessione dell'impianto. Ad oggi, le evidenze scientifiche mancano della coerenza necessaria per raccomandarle per uso clinico.
Sistemi di Ritenzione Protesica
I clip di ritenzione in plastica sono stati studiati in diversi scenari per indagare la loro ritenzione delle RDP supportate da denti. Sono stati descritti come meno ritenitivi rispetto ai materiali comunemente usati come il cobalto-cromo, ma comunque sufficientemente ritenitivi per servire al loro scopo clinico. I clip in resina PEEK si sono dimostrati potenzialmente affidabili come ganci di ritenzione per ancorare RDP supportate da denti con una vita utile di 10 anni; tuttavia, sembra necessario aumentare il loro diametro a doppio rispetto a quello dei ganci metallici per ottenere una ritenzione a lungo termine sufficiente. Nei casi di protesi supportate da impianti, ci sono poche evidenze sull'uso del PEEK per i clip di ritenzione. Bayer et al hanno riportato in uno studio clinico randomizzato su esseri umani che i clip in PEEK applicati come dispositivi di ritenzione su barre di impianto rotonde avevano una forza di ritenzione sufficiente, con una perdita di ritenzione clinicamente accettabile del 20% dopo 6 mesi.
Un polimero ad alte prestazioni più recente chiamato polieterechetonechetone (PEKK) è stato dichiarato in grado di fornire prestazioni meccaniche promettenti rispetto ad altri membri della famiglia dei poliarileterechetone (PAEK). Le sue favorevoli proprietà meccaniche sono date da una maggiore resistenza alla compressione, un modulo elastico simile a quello dell'osso umano e una maggiore capacità di lucidatura. In termini di adesione batterica, è stato anche dimostrato che il PEKK fornisce risultati comparabili a quelli del PEEK convenzionale. Attualmente, il PEKK è indicato per la produzione di dispositivi di ritenzione per protesi su impianti. Sono necessarie ulteriori indagini per ottenere una migliore comprensione della biocompatibilità di questo materiale e della sua fattibilità per i trattamenti protesici implantari.
È necessaria anche ulteriore ricerca per chiarire le specifiche relative al diametro e alla forma per i diversi design delle barre implantari, così come la loro capacità di ritenzione a lungo termine, poiché, ad oggi, questi parametri sono ancora sconosciuti.
Conclusioni
Nonostante il PEEK venga utilizzato per la fabbricazione di diversi componenti coinvolti nella riabilitazione protesica implantare, le evidenze scientifiche disponibili sono limitate in quantità e qualità. La mancanza di evidenze significa che intraprendere una revisione sistematica non è appropriato o necessario, ma sostiene ulteriori ricerche cliniche meglio progettate. L'uso del PEEK nella protesi implantare non dovrebbe ancora essere sostenuto; tuttavia, se utilizzato, i clinici dovrebbero prestare attenzione ai protocolli suggeriti riguardo a questa scelta di componente protesico, così come alla sua procedura di fabbricazione e al materiale di rivestimento o alla restaurazione sovrastante, tenendo presente che i risultati a lungo termine sono ancora incerti.
Autori: Andrea Paratelli, Giammarco Perrone, Rocío Ortega, Miguel Gómez-Polo
Riferimenti
- Kurtz SM, Devine JN. Biomateriali PEEK in traumi, ortopedia e impianti spinali. Biomaterials 2007;28:4845–4869.
- Panayotov IV, Orti V, Cuisinier F, Yachouh J. Polietereeterchetone (PEEK) per applicazioni mediche. J Mater Sci Mater Med 2016;27:118.
- Abu Bakar K, Cheang P, Khor K. Proprietà meccaniche dei biocompositi di idrossiapatite polietereeterchetone stampati a iniezione. Composites Sci Technol 2003;65:421-425.
- Almasi D, Iqbal N, Sadeghi M, Sudin I, Abdul Kadir MR, Kamarul T. Metodi di preparazione per migliorare la bioattività del PEEK per applicazioni ortopediche e dentali: Una revisione. Int J Biomater 2016;2016:8202653.
- Suess O, Schomaker M, Cabraja M, Danne M, Kombos T, Hanna M. Gabbie vuote in polietereeterchetone (PEEK) in discectomia cervicale anteriore e fusione (ACDF) mostrano una lenta fusione radiografica che riduce il miglioramento clinico: Risultati dello studio multicentrico prospettico “PIERCE-PEEK”. Patient Saf Surg 2017;11:12.
- Neumann EAF, Villar CC, França FM. Resistenza alla frattura delle viti di supporto realizzate in titanio, polietereeterchetone e polietereeterchetone rinforzato con fibra di carbonio. Braz Oral Res 2014;28:S1806-83242014000100239.
- Schwitalla AD, Abou-Emara M, Zimmermann T, et al. L'applicabilità delle viti di supporto in PEEK. J Mech Behav Biomed Mater 2016;63:244–251.
- Wiesli MG, Özcan M. Polimeri ad alte prestazioni e la loro potenziale applicazione come materiali per impianti medici e orali: Una revisione. Implant Dent 2015;24:448–457.
- Skirbutis D, Dzinguté A, Masiliénaité V, Sulcaite G, Žilinskas J. Una revisione delle proprietà del polimero PEEK e del suo utilizzo in protesi dentarie. Stomatologija 2017;19:19–23.
- Najeeb S, Zafar MS, Khurshid Z, Siddiqui F. Applicazioni della polietereeterchetone (PEEK) in implantologia orale e protesi dentarie. J Prosthodont Res 2016;60:12–19.
- Najeeb S, Bds ZK, Bds SZ, Bds MS. La bioattività e l'osseointegrazione del PEEK sono inferiori a quelle del titanio: Una revisione sistematica. J Oral Implantol 2016;42:512–516.
- Manolea HO, Ob dan F, Popescu SM, Rîcé R, Méréescu P, Iliescu AA, et al. Opzioni attuali per realizzare restauri protesici supportati da impianti per mitigare l'impatto delle forze occlusali. Defect and Diffusion Forum 2017;376:66–77.
- Georgiev J, Vlahova A, Kissov H, Aleksandrov S, Kazakova R. Possibile applicazione di BioHPP in odontoiatria protesica: Una revisione della letteratura. J IMAB 2018;24:1896–1898.
- Schwitalla A, Müller WD. Impianti dentali PEEK: Una revisione della letteratura. J Oral Implantol 2013;39:743–749.
- Schwitalla AD, Spintig T, Kallage I, Müller WD. Comportamento alla pressione di diversi materiali PEEK per impianti dentali. J Mech Behav Biomed Mater 2016;54:295–304.
- Zoidis P, Papathanasiou I. Protesi dentale fissa incollata in resina PEEK modificata come restauro provvisorio dopo l'inserimento dell'impianto. J Prosthet Dent 2016;116:637–641.
- Haddaway NR, Collins AM, Coughlin D, Kirk S. Il ruolo di Google Scholar nelle revisioni delle evidenze e la sua applicabilità alla ricerca nella letteratura grigia. PLoS One 2015;10:e0138237.
- Tricco AC, Lillie E, Zarin W, et al. PRISMA Extension for Scoping Reviews (PRISMA-ScR): Checklist e spiegazione. Ann Intern Med 2018;169:467–473.
- Pjetursson BE, Brägger U, Lang NP, Zwahlen M. Confronto dei tassi di sopravvivenza e complicazione per protesi dentali fisse supportate da denti (FDP) e FDP supportate da impianti e corone singole (SC). Clin Oral Implant Res 2007;18(suppl 3):97–113.
- Zoidis P. L'approccio terapeutico all'all-on-4 con polietereeterchetone modificata: Un rapporto clinico. J Prosthet Dent 2018;119:516–521.
- Al-Rabab’ah M, Hamadneh W, Alsalem I, Khraisat A, Abu Karaky A. Utilizzo di polimeri ad alte prestazioni come abutment e strutture per impianti dentali: Un rapporto di casi. J Prosthodont 2019;28:365–372.
- Bechir ES, Bechir A, Gioga C, Manu R, Burcea A, Dascalu IT. I vantaggi del polimero BioHPP come materiale per superstrutture in implantologia orale. Mater Plast 2016;53:394–398.
- Malo P, de Araújo Nobre M, Moura Guedes C, et al. Rapporto a breve termine di uno studio di coorte prospettico in corso che valuta l'esito di protesi ibride fisse in resina acrilica supportate da impianti a pieno arco e il concetto All-on-Four. Clin Implant Dent Relat Res 2018;20:692–702.
- Nazari V, Ghodsi S, Alikhasi M, Sahebi M, Shamshiri AR. Resistenza alla frattura di protesi parziali fisse supportate da impianti a tre unità con altezza della corona eccessiva realizzate in diversi materiali. J Dent (Tehran) 2016;13:400–406.
- Preis V, Hahnel S, Behr M, Bein L, Rosentritt M. Test di fatica e frattura in vitro di materiali CAD/CAM in corone molari supportate da impianti. Dent Mater 2017;33:427–433.
- Agustín-Panadero R, Serra-Pastor B, Roig-Vanaclocha A, Román-Rodriguez JL, Fons-Font A. Comportamento meccanico di abutment protesici provvisori per impianti. Med Oral Patol Oral Cir Bucal 2015;20:e94–e102.
- Santing HJ, Meijer HJ, Raghoebar GM, Özcan M. Resistenza alla frattura e modalità di rottura di corone singole provvisorie supportate da impianti mascellari: Un confronto tra corone in resina composita realizzate direttamente su abutment PEEK e abutment in titanio solido. Clin Implant Dent Relat Res 2012;14:882–889.
- Ostman PO, Hellman M, Sennerby L, Wennerberg A. Protesi temporanea supportata da impianti per carico immediato secondo un concetto chair-side: Nota tecnica e risultati da 37 casi consecutivi. Clin Implant Dent Relat Res 2008;10:71–77.
- Maté Sánchez de Val JE, Gómez-Moreno G, Pérez-Albacete Martínez C, et al. Comportamento dei tessuti peri-impianto attorno a materiali non in titanio: Studio sperimentale in cani. Ann Anat 2016;206:104–109.
- Bayer S, Komor N, Kramer A, Albrecht D, Mericske-Stern R, Enkling N. Forza di ritenzione di clip in plastica su barre di impianto: Uno studio controllato randomizzato. Clin Oral Implants Res 2012;23:1377–1384.
- Taufall S, Eichberger M, Schmidlin PR, Stawarczyk B. Carico di frattura e tipi di rottura di diverse protesi dentali fisse in polietereeterchetone rivestite. Clin Oral Investig 2016;20:2493–2500.
- Stawarczyk B, Eichberger M, Uhrenbacher J, Wimmer T, Edelhoff D, Schmidlin PR. FDP in composito rinforzato in polietereeterchetone a tre unità: Influenza del metodo di fabbricazione sulla capacità portante e sui tipi di rottura. Dent Mater J 2015;34:7–12.
- Papaspyridakos P, Mokti M, Chen CJ, Benic GI, Gallucci GO, Chronopoulos V. Tassi di sopravvivenza di impianti e protesi con impianti fissi completi in pazienti edentuli dopo almeno 5 anni: Una revisione sistematica. Clin Implant Dent Relat Res 2014;16:705–717.
- Bozini H, Petridis H, Garefis K, Garefis P. Una meta-analisi dei tassi di complicazione protesica delle protesi dentali fisse supportate da impianti in pazienti edentuli dopo un periodo di osservazione di almeno 5 anni. Int J Oral Maxillofac Implants 2011;26:304–318.
- Bidra AS, Tischler M, Patch C. Sopravvivenza di 2039 protesi in zirconia fisse a pieno arco supportate da impianti: Uno studio retrospettivo. J Prosthet Dent 2018;119:220–224.
- Wimmer T, Huffmann AM, Eichberger M, Schmidlin PR, Stawarczyk B. Tasso di usura a due corpi di PEEK, composito in resina CAD/CAM e PMMA: Effetto delle geometrie dei campioni, dei materiali antagonisti e della configurazione del set-up di prova. Dent Mater 2016;32:127–136.
- Tartaglia GM, Maiorana C, Gallo M, Codari M, Sforza C. Riabilitazioni a pieno arco supportate da impianti caricate immediatamente: Confronto dei risultati clinici tra resina e zirconia in uno studio di follow-up retrospettivo di 5 anni. Implant Dent 2016;25:74–82.
- Johansson P, Jimbo R, Kjellin P, Currie F, Chrcanovic BR, Wennerberg A. Valutazione biomeccanica e caratterizzazione della superficie di una superficie nano-modificata su impianti PEEK: Uno studio nella tibia del coniglio. Int J Nanomedicine 2014;9:3903–3911.
- Trindade R, Albrektsson T, Galli S, Prgomet Z, Tengvall P, Wennerberg A. Risposta immunitaria ossea ai materiali, Parte I: Titanio, PEEK e rame in confronto a sham a 10 giorni nella tibia del coniglio. J Clin Med 2018;7:526.
- Trindade R, Albrektsson T, Galli S, Prgomet Z, Tengvall P, Wennerberg A. Risposta immunitaria ossea ai materiali, Parte II: Rame e polietereeterchetone (PEEK) confrontati con titanio a 10 e 28 giorni nella tibia del coniglio. J Clin Med 2019;8:814.
- Etxeberria M, López-Jiménez L, Merlos A, Escuín T, Viñas M. Efficienza di adesione batterica sugli abutment per impianti: Uno studio comparativo. Int Microbiol 2013;16:235–242.
- Tetelman ED, Babbush CA. Un nuovo abutment transitorio per estetica e funzione immediate. Implant Dent 2008;17:51–58.
- Zafiropoulos GG, Deli G, Bartee BK, Hoffmann O. Posizionamento e carico di impianti a singolo dente in alveoli di estrazione freschi e rigenerati. Risultati a cinque anni: Una serie di casi utilizzando due diversi design di impianto. J Periodontol 2010;81:604–615.
- Kaleli N, Sarac D, Külünk S, Özturk Ö. Effetto di diversi materiali per corone restaurative e abutment personalizzati sulla distribuzione dello stress in impianti singoli e osso periferico: Uno studio di analisi agli elementi finiti tridimensionale. J Prosthet Dent 2018;119:437–445.
- Hahnel S, Wieser A, Lang R, Rosentritt M. Formazione di biofilm sulla superficie di materiali moderni per abutment di impianti. Clin Oral Implants Res 2015;26:1297–1301.
- Bressan E, Stocchero M, Jimbo R, et al. Perdita microbica alla connessione protesica conico-morse: Un'indagine in vitro. Implant Dent 2017;26:756–761.
- Amato F, Polara G, Spedicato GA. Cambiamenti dimensionali dei tessuti nell'inserimento immediato di impianti in zona estetica: Uno studio clinico retrospettivo. Int J Oral Maxillofac Implants 2018;33:439–447.
- Maté-Sánchez de Val J, Guirado JC, Ramirez Fernandez M, et al. Studio clinico ed esperimentale di un nuovo abutment ibrido in ceramica rinforzata PEEK-titanio posizionato in alveoli post-estrazione con restauro immediato. Clin Oral Implants Res 2015;26(suppl 12):356.
- Stoppie N, Van Oosterwyck H, Jansen J, Wolke J, Wevers M, Naert I. L'influenza del modulo di Young degli impianti caricati sul rimodellamento osseo: Uno studio sperimentale e numerico nel ginocchio di capra. J Biomed Mater Res A 2009;90:792–803.
- Tannous F, Steiner M, Shahin R, Kern M. Forze di ritenzione e resistenza alla fatica di ganci in resina termoplastica. Dent Mater 2012;28:273–278.
- Keilig L, Stark H, Bourauel C. La rigidità del materiale dei nuovi polimeri ad alte prestazioni per protesi parziali fisse influenza il loro comportamento biomeccanico? Int J Prosthodont 2016;30:595–597.
- Fuhrmann G, Steiner M, Freitag-Wolf S, Kern M. Legame della resina a tre tipi di polietere chetonici aromatici (PAEK): Durabilità e influenza della preparazione della superficie. Dent Mater 2014;30:357–363.
- Wang M, Bhardwaj G, Webster TJ. Proprietà antibatteriche del PEKK per applicazioni ortopediche. Int J Nanomedicine 2017;12:6471–6476.
- Srinivasan M, Kalberer N, Maniewicz S, Müller F. Protesi overdenture mantenute da impianti utilizzando un attacco con correzione di allineamento vero: Una serie di casi.
