Somministrazione locale ripetuta di gel di acido ialuronico come trattamento aggiuntivo delle tasche residue in pazienti con parodontite sottoposti a cure parodontali di supporto. Uno studio clinico controllato randomizzato.
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Abstract
Obiettivi Valutare l'effetto dell'applicazione di acido ialuronico (HyA) come complemento alla reinstrumentazione delle tasche residue in pazienti sottoposti a regolare assistenza parodontale di supporto (SPC).
Metodi Pazienti con parodontite cronica (stadio III e IV, grado B e C) con 4 tasche residue interprossimali sono stati assegnati casualmente al gruppo di test (gel HyA) o al gruppo di controllo (soluzione salina). Dopo l'instrumentazione sottogengivale, la sostanza di test o di controllo è stata applicata sottogengivalmente, quindi quotidianamente sovragengivalmente per 3 mesi, e se necessario una seconda volta dopo la reinstrumentazione sottogengivale dopo 3 mesi. I parametri clinici e i risultati riportati dai pazienti sono stati registrati ogni 3 mesi per 12 mesi. La chiusura della tasca [profondità di sondaggio della tasca (PPD) ≤ 4mm con assenza di sanguinamento alla sondatura (BoP) a PPD = 4mm] era il principale parametro di esito.
Risultati Cinquantasei pazienti (221 siti sperimentali) sono stati analizzati. La chiusura della tasca è stata raggiunta nel 56,8 e nel 46,6% dei siti sperimentali nel gruppo di test e nel gruppo di controllo, rispettivamente (p > 0,05), mentre la PPD mediana e la distribuzione della PPD (< 5mm/5mm/ > 5mm) differivano significativamente tra i gruppi a favore del gruppo di test, a 12 mesi. Inoltre, significativamente meno siti nel gruppo HyA hanno richiesto reinstrumentazione a 3 mesi, e i siti nel gruppo HyA hanno mostrato una tendenza a presentare minori probabilità di rimanere malati rispetto al gruppo di controllo (OR 0.48, 95%CI 0.22–1.06). Le probabilità che un sito rimanesse malato dopo 12 mesi sono aumentate significativamente in presenza di placca (OR 7.94, 95%CI 4.12–15.28), ma in generale, sono diminuite significativamente nel tempo (OR 0.48, 95%CI 0.28–0.81).
Conclusione La reinstrumentazione delle tasche residue nei pazienti SPC, di per sé, porta a un significativo aumento della chiusura delle tasche nel tempo; ciò è stato ostacolato da un cattivo controllo della placca. L'applicazione locale ripetuta di HyA porta a meno siti che richiedono reinstrumentazione e potrebbe migliorare leggermente il tasso di chiusura delle tasche. (registrazione clinicaltrials.gov nr. NCT04792541).
Rilevanza clinica Il gel di HyA è facile da applicare, ben accettato dai pazienti e potrebbe avere un effetto positivo in termini di meno siti che richiedono reinstrumentazione a 3 mesi e un tasso di chiusura delle tasche più elevato a 12 mesi.
Introduzione
L'instrumentazione subgengivale non chirurgica iniziale (cioè, secondo passo della terapia), sia manuale che con strumenti (ultra)sonici (o una combinazione di essi), è un approccio terapeutico molto efficace nei pazienti con parodontite; in media, una profondità di sondaggio delle tasche (PPD) superficiale può essere raggiunta in 3 tasche su 4. Recentemente, il World Workshop on the Classification of Periodontal and Peri‐Implant Diseases and Conditions e le linee guida cliniche EFP S3 hanno definito l'obiettivo del trattamento parodontale. A livello del sito, la chiusura della tasca è definita come PPD ≤ 4 mm e nessun sanguinamento alla sondatura (BoP), mentre a livello del paziente, un paziente con parodontite trattato con successo è caratterizzato da 1) PPD di ≤ 4 mm, 2) nessun PPD = 4 mm con BoP, e 3) BoP totale < 10%. Sebbene questo obiettivo sia difficile da raggiungere in ogni paziente, è stato dimostrato che i pazienti che raggiungono questi endpoint clinici presentano un tasso ridotto di progressione/recidiva della malattia e perdita di denti a causa della parodontite durante la cura parodontale di supporto a lungo termine (SPC). Pertanto, l'uso di prodotti aggiuntivi (somministrati localmente o sistemicamente) durante il secondo passo della terapia è frequentemente discusso, con l'obiettivo di 1) migliorare ulteriormente il tasso di chiusura delle tasche, 2) ridurre la necessità di ulteriore terapia chirurgica, e/o 3) migliorare il tasso di raggiungimento di un paziente con parodontite trattato con successo e stabile. Questo, a sua volta, dovrebbe non solo migliorare la stabilità a lungo termine del trattamento e ridurre la perdita di denti, ma anche minimizzare la morbidità del paziente e, infine, i costi di trattamento. Le varie opzioni e l'efficacia degli ausili somministrati localmente (cioè, modulatori dell'ospite o antimicrobici) durante il secondo passo della terapia sono state valutate ampiamente nell'ambito delle linee guida cliniche EFP S3. È stato infine suggerito che solo la clorexidina a rilascio prolungato e gli antibiotici applicati localmente possano essere considerati opzioni valide. In questo contesto, ci sono informazioni limitate riguardo al “miglior” momento di somministrazione degli ausili applicati localmente, in termini di (costo-)efficienza, cioè se debbano essere applicati durante il secondo passo della terapia o durante il terzo o quarto passo della terapia in caso di reinstrumentazione delle tasche residue/recidivanti, rispettivamente. Considerando gli impatti sui pazienti, sulla società e/o i possibili impatti biologici dell'uso non necessario di qualsiasi misura ausiliaria, quest'ultimo approccio consentirebbe di limitare il loro uso a quei pazienti/siti che non guariscono dopo l'instrumentazione subgengivale iniziale. Due recenti revisioni sistematiche hanno trattato l'efficacia degli ausili per i pazienti con parodontite con tasche residue/recidivanti durante la SPC. In particolare, tra gli antimicrobici somministrati localmente, la clorexidina a rilascio prolungato e le fibre di tetraciclina si sono classificate al primo posto con una riduzione aggiuntiva di PPD statisticamente e clinicamente significativa di circa 0,6-0,7 mm, mentre sono disponibili prove insufficienti per qualsiasi altra opzione di trattamento ausiliario (cioè, diversa dagli antimicrobici).
Un altro ausiliario somministrato localmente, tuttavia, che non è stato incluso in nessuna delle revisioni sistematiche sopra menzionate né nelle Linee Guida Cliniche di Livello S3 dell'EFP, è l'acido ialuronico (HyA). Vari gel contenenti HyA in diverse concentrazioni sono stati, da diversi anni, testati come ausiliari all'istrumentazione meccanica subgengivale non chirurgica e la loro efficacia è stata persino riassunta in alcune revisioni sistematiche. Queste revisioni hanno avuto conclusioni ben comparabili, cioè, la maggior parte degli studi clinici inclusi ha riportato un effetto positivo, sebbene moderato, a favore di HyA in termini di riduzione della PPD e del BoP. Tuttavia, c'era una grande variazione nei modi e nella frequenza di applicazione negli studi originali, e tutte le revisioni hanno sottolineato la necessità di ulteriori studi clinici controllati randomizzati (RCT) ben progettati, che includano un'adeguata segnalazione dei dettagli del prodotto. In questo contesto, attualmente non è chiaro se l'applicazione ripetuta di un ausiliario somministrato localmente sia, in generale, vantaggiosa rispetto all'applicazione singola, cioè, solo subito dopo l'istrumentazione. Tuttavia, 2 recenti RCT hanno valutato l'applicazione di HyA in ufficio specificamente nella re-istrumentazione di tasche residue/ricadenti. Ogni studio ha testato un diverso prodotto HyA e frequenza di applicazione; in uno degli studi HyA è stato applicato subgengivalmente, una volta, mentre nell'altro studio HyA è stato applicato subgengivalmente in 2 appuntamenti consecutivi, ma entrambi hanno mostrato una tendenza a favore dell'applicazione di HyA.
Pertanto, sembra ragionevole valutare se l'applicazione locale combinata di HyA, cioè subgingivale in ufficio, dopo l'istruzione meccanica, e ripetuta sovragengivale, da parte del paziente, una volta al giorno per 3 mesi, abbia il potenziale di migliorare il tasso di chiusura delle tasche rispetto alla re-istruzione da sola nel trattamento delle tasche residue nei pazienti con parodontite che seguono un SPC regolare.
Materiali e metodi
Progetto dello studio e partecipanti
Il presente studio è stato un trial clinico randomizzato, in doppio cieco (paziente e osservatore), controllato con placebo, a gruppi paralleli con follow-up di 12 mesi ed è riportato in conformità agli standard di reporting degli studi clinici (Dichiarazione CONSORT; Appendice 1). Il protocollo è stato approvato dal comitato etico regionale (Dnr. 2016/468) e registrato su clinicaltrials.gov (NCT04792541); eventuali modifiche al protocollo dopo la sua pubblicazione sono elencate nell'Appendice 2. Il reclutamento dei pazienti è stato effettuato tra dicembre 2016 e gennaio 2020, cioè, il reclutamento dei pazienti è iniziato prima del World Workshop sulla Classificazione delle Malattie e Condizioni Parodontali e Peri-Implantari nel 2017. Tutti i pazienti con parodontite, che avevano completato la fase di trattamento attivo da ≥ 6 mesi e erano stati arruolati in un programma SPC regolare (cioè, passo 4 del trattamento) in una Clinica Specializzata per la Parodontologia (Servizio Dentistico Pubblico, Värmland, Svezia), soddisfacendo i seguenti criteri di inclusione sono stati inclusi consecutivamente: (i) età compresa tra 35 e 75 anni, (ii) diagnosi di parodontite cronica, (iii) almeno 10 denti rimanenti, e (iv) 4-8 siti interprossimali con PPD di ≥ 5 a < 8 mm e presenza di BoP al momento dell'inclusione. Inoltre, sono stati definiti i seguenti criteri di esclusione: (i) molari con coinvolgimento della furcazione di classe II o III, (ii) mobilità dentale di classe II o III, (iii) > 2 mm di PPD più profondo in un altro sito nello stesso spazio interprossimale (iv) terapia antibiotica nei 6 mesi precedenti o durante la partecipazione allo studio, (v) necessità di profilassi antibiotica prima dell'esame parodontale e/o trattamento, (vi) uso a lungo termine di farmaci anti-infiammatori e immunosoppressori, (vii) diabete non controllato o recentemente diagnosticato prima o durante la partecipazione allo studio, (viii) gravidanza o allattamento, (ix) grave disfunzione occlusale, (x) trattamento ortodontico in corso, e (xi) lesioni endodontiche. Età, sesso, stato di fumatore (cioè, mai / ex / attuale fumatore) e presenza/assenza di diabete mellito ben controllato sono stati registrati per ciascun partecipante.
Prodotto test e placebo
Il prodotto utilizzato nel gruppo “test/HyA” per l'applicazione sub- e supragingivale era un gel contenente acido ialuronico (0,3%, non reticolato, peso molecolare medio; Afta Clear™ Gel; Sunstar Europe SA, Etoy, Svizzera), mentre il “gruppo di controllo/placebo” riceveva una piccola bottiglia di soluzione salina fisiologica. Entrambi i prodotti erano mascherati con nastro bianco, in modo che il paziente non fosse a conoscenza dell'assegnazione al gruppo.
Intervento, randomizzazione e cieco
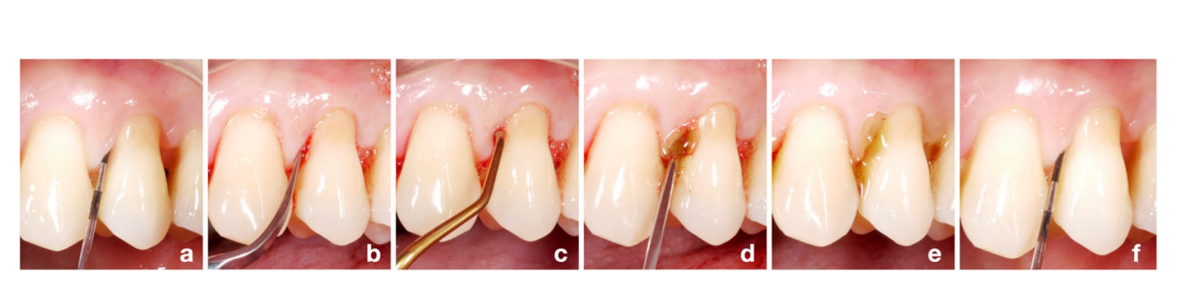
Prima dell'inizio dello studio, un elenco di sequenze casuali per l'assegnazione ai gruppi è stato generato al computer (rapporto 1:1 per il gruppo test/HyA e il gruppo di controllo/placebo) da un parodontologo non incluso nel processo di reclutamento (KB). Tutti i partecipanti sono stati reclutati da uno dei 3 igienisti dentali esperti (LG, AS, MSS). Quattro siti interprossimali di ciascun partecipante sono stati definiti come siti sperimentali (cioè, mesio-buccale, mesio-palatale/-linguale, disto-buccale o disto-palatale/-linguale); se possibile, è stato scelto 1 sito per quadrante, altrimenti i siti sperimentali dovevano trovarsi in spazi interprossimali diversi. Tutti i partecipanti hanno ricevuto all'inizio una sessione standard di SPC che includeva la reinstrumentazione con un dispositivo ultrasonico (E.M.S. Electro Medical Systems S.A., Nyon, Svizzera) e/o strumenti manuali (HuFriedyGroup, Chicago, USA) di tutte le tasche residue da uno dei 3 igienisti dentali sopra menzionati; ciascun paziente è stato trattato dallo stesso igienista dentale per tutto il periodo dello studio. L'assegnazione ai gruppi è stata nascosta fino dopo la reinstrumentazione delle tasche residue. Dopo la reinstrumentazione, un parodontologo (AZ) si è unito alla sessione di trattamento, rivelando l'assegnazione al gruppo solo a se stesso aprendo una nota nascosta nella busta con il modulo di rapporto del caso del paziente, e ha applicato il prodotto test o placebo subgingivalmente in tutti i siti sperimentali. Per l'applicazione subgingivale, il prodotto test e placebo sono stati trasferiti in una siringa sterile con un ago smussato e i siti sperimentali sono stati riempiti fino a quando il prodotto non traboccava dalla tasca (Fig. 1). Lo stesso parodontologo ha eseguito questa procedura su tutti i partecipanti, mentre gli igienisti dentali e i pazienti sono rimasti all'oscuro dell'assegnazione ai gruppi. Ciascun paziente ha ricevuto un volantino con un riepilogo delle istruzioni pertinenti e un disegno che indicava i 4 siti sperimentali, compresa la dimensione corretta delle spazzole interdentali (TePe Munhygienprodukter AB, Malmö, Svezia) per lo specifico spazio interprossimale e il prodotto test o placebo. I pazienti dovevano applicare il prodotto una volta al giorno supragingivalmente con una spazzola interdentale dopo lo spazzolamento dei denti, solo nei siti sperimentali, e per i successivi 3 mesi fino al secondo appuntamento SPC (cioè, follow-up di 3 mesi). Inoltre, ai pazienti è stato detto di evitare di spazzolare i denti o mangiare per 3 ore dopo l'applicazione e di non utilizzare alcuna soluzione per il risciacquo orale o altri gel durante la partecipazione allo studio attuale. Le sessioni di SPC sono state ripetute dopo 3, 6, 9 e 12 mesi, tuttavia, il paziente ha smesso di applicare il prodotto test o placebo dopo i primi 3 mesi. Infine, tutti i siti sperimentali con PPD = 5 mm e BoP o PPD > 5 mm al follow-up di 3 mesi hanno ricevuto nuovamente reinstrumentazione e una seconda applicazione subgingivale del prodotto assegnato, come descritto sopra. In generale, tutti i siti con PPD= 5 mm e BoP o PPD>5 mm in qualsiasi delle sessioni SPC hanno ricevuto come standard di cura reinstrumentazione subgingivale.
Valutazione dei risultati e cieco
Il campionamento microbiologico subgengivale dai 4 siti sperimentali è stato effettuato all'inizio e dopo 3, 6 e 12 mesi. I risultati del campionamento microbiologico saranno riportati altrove. Inoltre, dopo il campionamento microbiologico e ad ogni SPC (cioè, all'inizio e dopo 3, 6, 9 e 12 mesi) lo stesso igienista dentale cieco e calibrato (LG, AS, MSS) ha registrato PPD, livello di attacco clinico (CAL), presenza/assenza di BoP e presenza/assenza di placca in ciascun sito sperimentale. Come standard di cura, il parodontologo (AZ) di questa specifica Clinica Specialistica controlla le misurazioni PPD di ciascun igienista circa 2-3 volte all'anno, il che è stato considerato come calibrazione. Inoltre, ad ogni follow-up i pazienti sono stati interrogati su eventuali cambiamenti nella loro storia medica e su eventuali assunzioni di antibiotici nei 3 mesi precedenti. Al secondo SPC (cioè, follow-up di 3 mesi), i pazienti hanno ricevuto inoltre un breve questionario sulla loro opinione riguardo al prodotto testato. Il questionario chiedeva la presenza e l'intensità del dolore durante l'applicazione e l'opinione dei pazienti sulla consistenza e sul gusto del prodotto durante l'uso domestico, utilizzando una scala da 1 a 10. Un esito di trattamento riuscito (cioè, chiusura della tasca) è stato definito come PPD≤ 4 mm con assenza di BoP a PPD = 4 mm; se questi criteri non erano soddisfatti, il sito sperimentale rimaneva classificato come "malato". Questo esito composito è stato definito come parametro di esito primario e valutato ad ogni SPC.
Criteri di idoneità per il follow-up
I pazienti erano programmati ogni 3 mesi per SPC, tuttavia, era consentito un intervallo di 2,5-5 mesi tra 2 sessioni di SPC; se il tempo tra 2 sessioni di SPC superava i 5 mesi, l'appuntamento SPC era considerato perso. Inoltre, il periodo totale dal primo al quinto appuntamento SPC non doveva superare i 18 mesi, altrimenti il paziente veniva escluso. Poiché erano stati inclusi diversi pazienti prima dell'epidemia della pandemia di Covid-19, ai pazienti era consentito saltare l'appuntamento di 6 o 9 mesi senza essere esclusi dallo studio. Tuttavia, i pazienti che saltavano 2 sessioni di SPC o l'appuntamento di 3 o 12 mesi venivano anch'essi esclusi.
Calcolo della dimensione del campione
Per il calcolo della dimensione del campione, si presumeva che il 75% e il 25% dei siti nel gruppo test/HyA e nel gruppo controllo/placebo, rispettivamente, avrebbero raggiunto la chiusura della tasca, cioè PPD ≤ 4 mm con assenza di BoP a PPD = 4 mm. In presenza di questi parametri clinici, il rischio di progressione della malattia è considerato basso e il trattamento è considerato efficace. Sulla base del set di dati di una pubblicazione precedente, si presume un coefficiente di correlazione intra-individuale di 0,42 per la presenza di BoP. Basandosi su questo coefficiente di correlazione, una potenza di 0,80 e un valore alpha di 0,05, è stata calcolata una dimensione del campione di 30 partecipanti per gruppo (cioè una popolazione totale di studio di 60). Per compensare le rinunce, sono stati reclutati consecutivamente un totale di 80 pazienti (40 pazienti per gruppo).
Analisi statistica
La distribuzione di frequenza per variabili categoriali (come genere, stato di fumatore, distribuzione PPD, ecc.) e le medie (deviazioni standard) o mediane e intervalli interquartili per variabili continue (come età, PPD, ecc.) sono riportate separatamente per il gruppo test/HyA e il gruppo di controllo/placebo. Per testare eventuali differenze tra il gruppo test/HyA e il gruppo di controllo/placebo è stato applicato il test esatto di Fisher o il test del chi-quadrato per parametri categoriali (cioè, il test del chi-quadrato è stato applicato se ogni cella presentava una frequenza > 5) e per variabili continue è stato utilizzato un test t indipendente (per dati distribuiti normalmente) o un test di Mann Whitney-U (per dati non distribuiti normalmente). La normalità dei dati è stata controllata tramite il test di Shapiro-Wilk. Lo “stato di salute del sito sperimentale” è stato definito come il parametro di esito primario [dichotomico; “malato” (cioè, PPD > 4 mm o PPD = 4 mm con BoP) contro “trattato con successo/chiusura della tasca” (cioè, PPD ≤4 mm con assenza di BoP a PPD = 4 mm). Sono stati calcolati due modelli di regressione logistica a effetti misti multivariati con l'assegnazione del gruppo come principale predittore e i seguenti confondenti a priori: 1) tipo di dente (anteriore / premolare / molare), 2) sito interprossimale (buccale / palatale/linguale), 3) PPD al basale presso il sito sperimentale (5 mm / 6–7 mm), 4) placca presso il sito sperimentale ad ogni appuntamento (assente / presente), 5) stato di fumatore (mai / ex / attuale), 6) genere (femminile / maschile), 7) tempo trascorso tra gli appuntamenti (mesi), e 8) età (anni). Il primo modello includeva solo i dati a 3 mesi, mentre il secondo modello includeva tutti i dati raccolti su un periodo di 12 mesi; in quest'ultimo modello è stato aggiunto un ulteriore confondente, cioè, il punto temporale (follow-up a 3- / 6- / 9- / 12 mesi). L'analisi statistica è stata eseguita con STATA/IC 17.0 per Mac (Lakeway Drive, Texas, USA) e un valore p ≤ 0.05 è stato considerato statisticamente significativo.
Risultati
Caratteristiche della popolazione al basale (livello paziente)
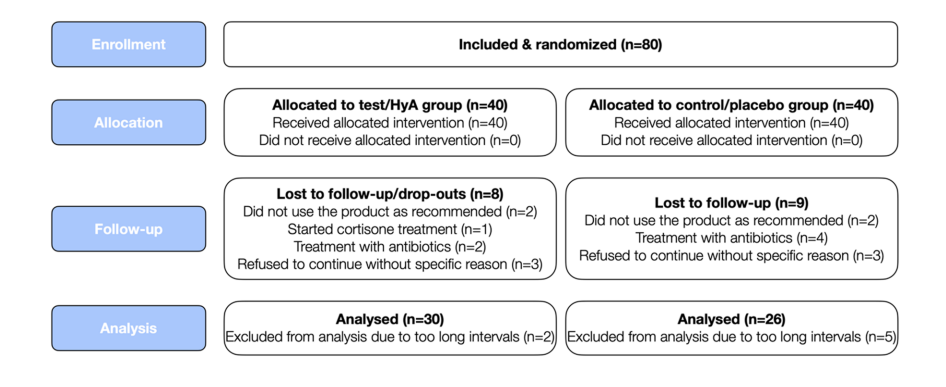
Ottanta pazienti con parodontite cronica (corrispondenti a pazienti con parodontite di stadio III e IV e grado B e C) sottoposti a SPC regolari sono stati reclutati e randomizzati. In totale, 24 partecipanti hanno abbandonato o non potevano essere inclusi nell'analisi per vari motivi (per dettagli vedere Fig. 2). Le caratteristiche dei 56 pazienti (cioè, 30 e 26 pazienti nel gruppo test/HyA e nel gruppo controllo/placebo, rispettivamente), che contribuiscono all'analisi, sono riportate nella Tabella 1; nessuna delle caratteristiche basali a livello paziente differiva significativamente tra i 2 gruppi. In breve, il campione 1) era composto da circa il 66% di femmine, 2) aveva un'età media di 58 anni, 3) includeva circa il 46% di fumatori attuali e 4) aveva 3 diabetici ben controllati.
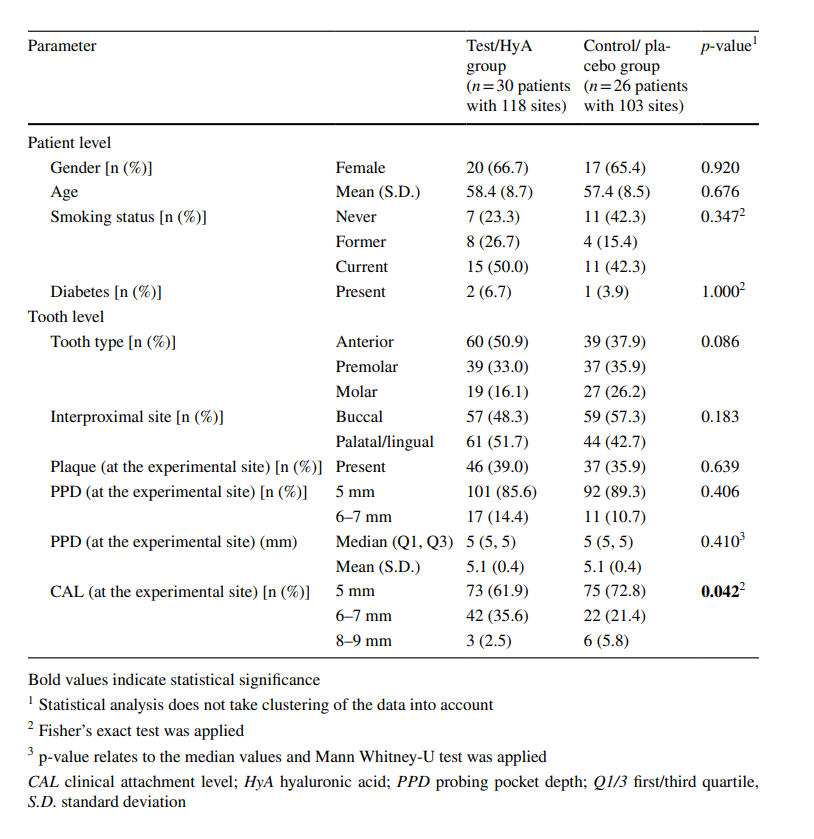
Caratteristiche dei siti sperimentali al basale (livello dentale)
Il campione includeva 221 siti sperimentali, tutti giudicati “malati” in base ai criteri di idoneità con presenza di BoP al basale. Ad eccezione di 3 pazienti, ogni paziente ha contribuito con 4 siti sperimentali. Tre siti sperimentali (uno per ciascuno di 2 pazienti test/HyA e 1 paziente di controllo/placebo) sono stati esclusi a causa di riabilitazione con una nuova restaurazione protesica sul dente sperimentale o su un dente adiacente (n = 2) e a causa di un paziente che ha applicato per errore il prodotto sul dente controlaterale, cioè su quello sbagliato (n = 1). Le caratteristiche basali dei siti sperimentali del gruppo test/HyA e del gruppo controllo/placebo sono riportate nella Tabella 1. Il tipo di dente, i siti interprossimali, la placca e il PPD erano ben distribuiti tra i 2 gruppi, mentre il gruppo test/HyA ha contribuito con significativamente più siti che mostrano un CAL ≥ 6 mm rispetto al gruppo controllo/placebo (p = 0.042). La maggior parte dei siti presentava un PPD = 5 mm al basale, mentre il 14.4 e il 10.7% del gruppo test/HyA e del gruppo controllo/placebo, rispettivamente, avevano un PPD di 6-7 mm al basale.
Caratteristiche dei siti sperimentali dopo 3 mesi (a livello dentale)
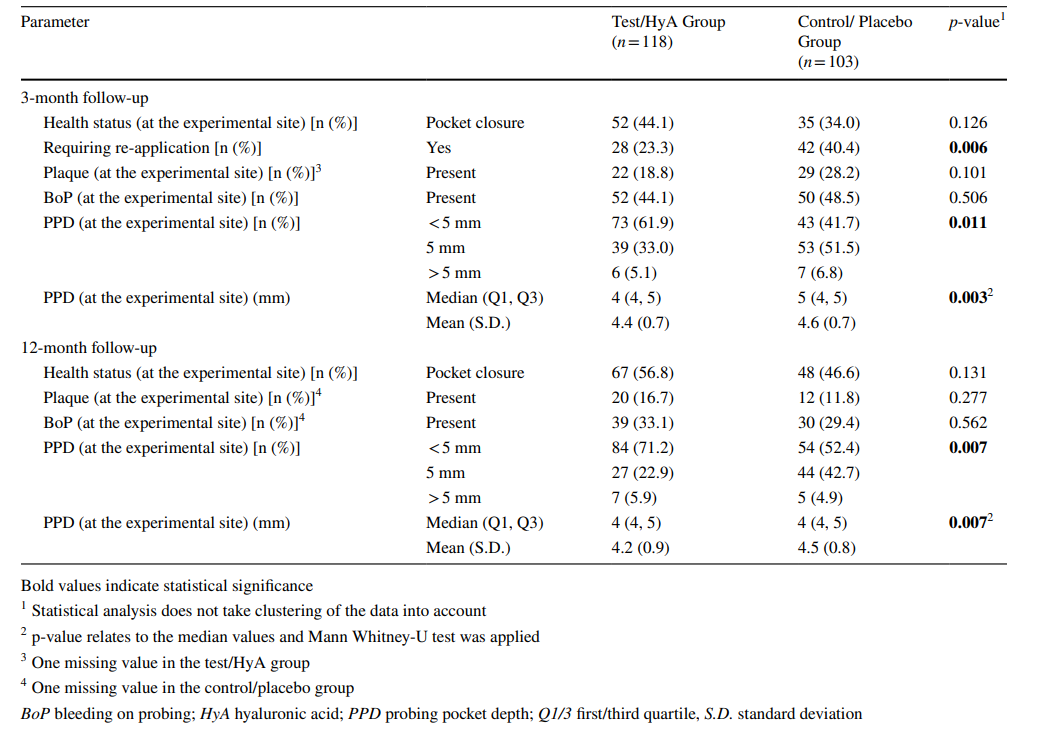
Le caratteristiche dei siti sperimentali dopo 3 mesi sono riportate nella Tabella 2. Dopo 3 mesi, il 44,1% e il 34,0% dei siti sperimentali del gruppo test/HyA e del gruppo controllo/placebo, rispettivamente, hanno raggiunto la chiusura della tasca senza una differenza significativa tra i gruppi. Allo stesso modo, la presenza di placca e BoP era comparabile tra i 2 gruppi. Tuttavia, la mediana PPD (p = 0.003) e la distribuzione della PPD (< 5mm / 5 mm / > 5mm; p = 0.011) differivano significativamente tra i gruppi a favore del gruppo test/HyA. In particolare, il 61,9% e il 41,7% dei siti sperimentali del gruppo test/HyA e del gruppo controllo/placebo, rispettivamente, presentavano PPD < 5 mm. Inoltre, significativamente meno siti nel gruppo test/HyA (p = 0.006) rispetto al gruppo controllo/placebo, 23,3% e 40,4%, rispettivamente, richiedevano una riapplicazione subgingivale al follow-up di 3 mesi.
Valutazione del risultato del trattamento dopo 3 mesi
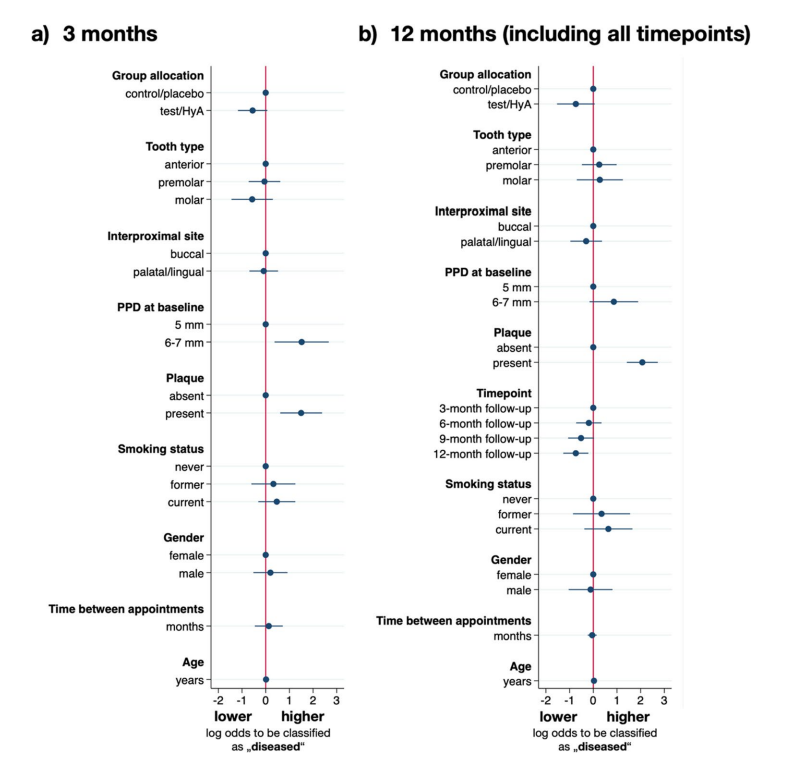
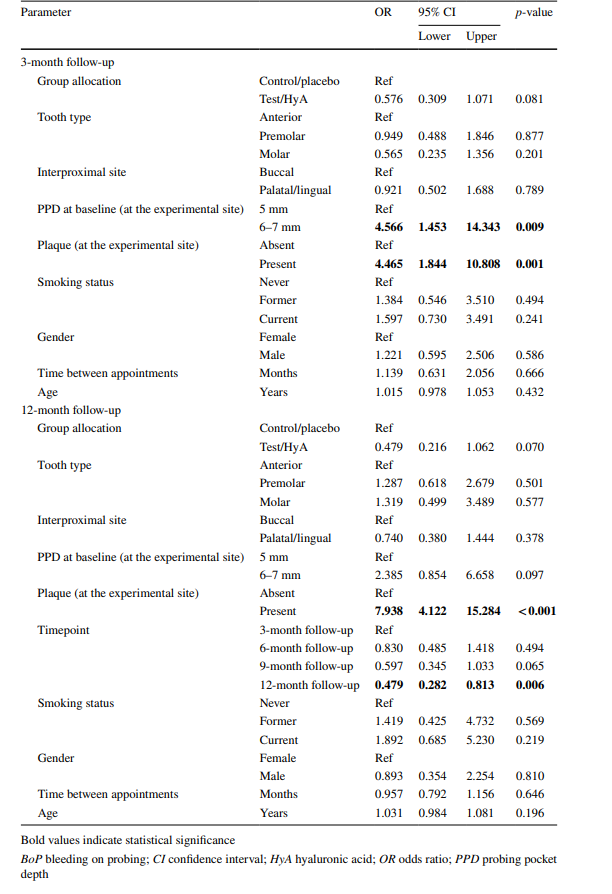
I risultati dell'analisi di regressione logistica a effetti misti multivariata dopo 3 mesi di SPC sono mostrati nella Fig. 3a e nella Tabella 3. I siti sperimentali nel gruppo test/HyA avevano probabilità leggermente, ma statisticamente non significative, più basse rispetto al gruppo di controllo/placebo di rimanere “malati” (cioè, PPD > 4 mm o PPD = 4 mm con BoP) (OR 0.58, 95% CI 0.31–1.07; p = 0.081). Tra i fattori confondenti inclusi, solo la placca e il PPD al basale avevano un effetto significativo sull'esito. In particolare, la presenza di placca (OR 4.47, 95% CI 1.84–10.81; p = 0.001) e un PPD più alto al basale (OR 4.57, 95% CI 1.45–14.34; p = 0.009) aumentavano significativamente le probabilità di rimanere “malati” al follow-up di 3 mesi.
Caratteristiche dei siti sperimentali dopo 12 mesi (livello del dente)
Le caratteristiche dei siti sperimentali alla valutazione finale (follow-up di 12 mesi) sono riportate nella Tabella 2. Alla valutazione finale, il 56,8% e il 46,6% dei siti sperimentali del gruppo test/HyA e del gruppo controllo/placebo, rispettivamente, hanno raggiunto la chiusura della tasca senza una differenza significativa tra i gruppi. Allo stesso modo, la presenza di placca e BoP era comparabile tra i 2 gruppi. Tuttavia, la mediana PPD (p = 0,007) e la distribuzione della PPD (< 5mm / 5 mm / > 5mm; p = 0,007) differivano significativamente tra i gruppi a favore del gruppo test/HyA. In particolare, il 71,2% e il 52,4% dei siti test/HyA e controllo/placebo, rispettivamente, presentavano PPD < 5 mm e la mediana PPD era più bassa nel gruppo test/HyA. Nel gruppo test/HyA, su 28 siti sperimentali che hanno ricevuto la riapplicazione a 3 mesi, il 28,6% non era più malato dopo 12 mesi, mentre su 90 siti sperimentali che non hanno ricevuto la riapplicazione a 3 mesi, il 34,4% è stato classificato nuovamente come “malato”. Nel gruppo controllo/placebo, su 42 siti sperimentali che hanno ricevuto la riapplicazione a 3 mesi, il 33,3% non era più malato dopo 12 mesi, mentre su 61 siti sperimentali che non hanno ricevuto la riapplicazione a 3 mesi, il 44,3% è stato classificato nuovamente come “malato”.
Valutazione del risultato del trattamento dopo 12 mesi
I risultati dell'analisi di regressione logistica a effetti misti multivariata sono mostrati nella Fig. 3b e nella Tabella 3. I siti sperimentali del gruppo test/HyA avevano probabilità leggermente, ma statisticamente non significative, più basse rispetto al gruppo di controllo/placebo di rimanere “malati” (cioè, PPD > 4 mm o PPD = 4 mm con BoP) (OR 0.48, 95% CI 0.22–1.06; p = 0.070). Tra i confondenti inclusi, solo la placca e il punto temporale avevano un effetto significativo sul risultato. In particolare, la presenza di placca aumentava significativamente le probabilità di rimanere “malati” di circa 8 volte (OR 7.94, 95% CI 4.12–15.28; p < 0.001), e, in generale, le probabilità di rimanere “malati” diminuivano durante il periodo di studio raggiungendo significatività nella valutazione finale (OR 0.48, 95% CI 0.28–0.81; p = 0.006).
Opinione dei pazienti
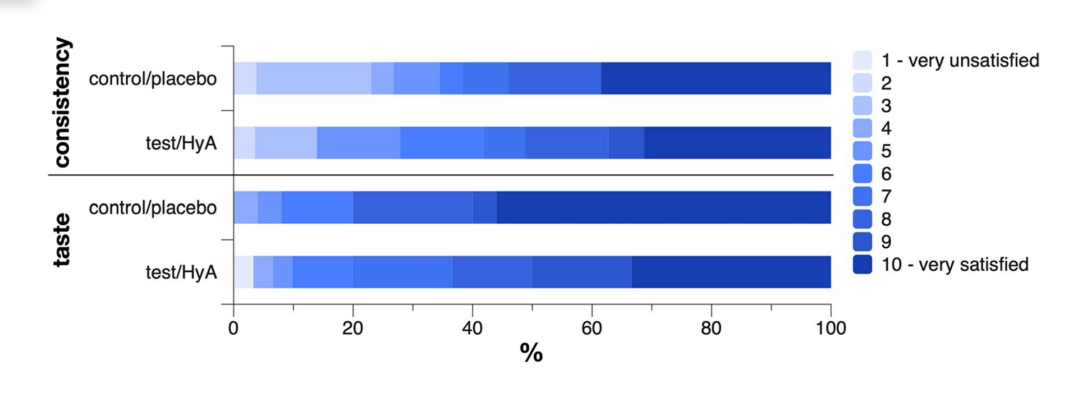
Un paziente di ciascun gruppo ha riferito di aver avvertito dolore alla gengiva durante l'applicazione del prodotto con un'intensità da 3 a 4 su 10, con 10 che rappresenta il dolore massimo. Un paziente del gruppo test/HyA non ha risposto sulla consistenza e un paziente del gruppo controllo/placebo non ha risposto sul gusto. I gruppi non hanno presentato differenze significative nella loro opinione sulla consistenza e sul gusto del prodotto (Fig. 4). In particolare, i valori medi (deviazione standard) della scala per la consistenza erano 7.2 (2.6) e 7.0 (3.0) nel gruppo test/HyA e nel gruppo controllo/placebo, rispettivamente (p = 0.822), e i valori mediani (primo, terzo quartile) della scala per il gusto erano 8.5 (7, 10) e 10 (8, 10) nel gruppo test/HyA e nel gruppo controllo/placebo, rispettivamente (p = 0.184); per entrambi i parametri un valore di 10 rappresentava una grande soddisfazione.
Sicurezza
Nessuno dei pazienti ha riportato effetti collaterali/complicazioni legati all'applicazione del prodotto e non sono stati osservati eventi avversi clinicamente.
Discussione
I chemioterapici somministrati localmente sono frequentemente utilizzati come complemento al trattamento non chirurgico nei pazienti con parodontite, sia nella fase iniziale del trattamento che in tasche residue/recidivanti durante una fase successiva del trattamento. Tuttavia, poiché l'istruzione subgengivale non chirurgica iniziale è un trattamento piuttosto efficace di per sé, un approccio più specifico per le tasche che non si sono guarite durante il secondo passo della terapia e/o per le tasche recidivanti durante la SPC potrebbe essere l'approccio più rilevante. Qui, un gel contenente HyA, applicato ripetutamente (giornalmente) per un periodo di 3 mesi, come complemento alla reinstrumentazione delle tasche residue/recidivanti in pazienti sottoposti a SPC regolare, ha mostrato una certa tendenza a migliorare il risultato, cioè, è stata osservata una percentuale di chiusura delle tasche superiore del 10% per i siti che ricevevano HyA rispetto a quelli del gruppo di controllo che ricevevano soluzione salina fisiologica (cioè, 57 contro 47% dei siti, rispettivamente), dopo 12 mesi. Inoltre, la percentuale di siti sperimentali con PPD < 5 mm era circa 1,4 volte superiore nel gruppo test/HyA rispetto al gruppo di controllo/placebo (cioè, 71 e 52% dei siti, rispettivamente).
Questi risultati sono in accordo con quelli riportati in 2 recenti RCT che valutano un gel contenente HyA come complemento alla reinstrumentazione di tasche residue/ricorrenti e mostrano che l'uso di un gel contenente HyA ha portato a una tendenza per risultati superiori rispetto alla sola reinstrumentazione. Inoltre, entrambi gli studi hanno riportato nel loro gruppo di test una frequenza simile di siti con PPD < 5 mm dopo 12 mesi, cioè, 76-77% nei 2 studi precedenti e 71% qui. Inoltre, in uno degli studi RCT che riportano sulla chiusura delle tasche (cioè, PPD ≤ 4 mm senza BoP), è stata osservata una percentuale comparabile nel gruppo HyA come qui, cioè, rispettivamente nel 59% e 57%. Tuttavia, una differenza significativa tra questi 2 RCT e lo studio attuale riguarda le caratteristiche del prodotto del gel HyA applicato. Specificamente, in questo studio è stato utilizzato un HyA non reticolato, di peso molecolare medio, con una concentrazione relativamente bassa (0,3%), mentre gli altri studi hanno utilizzato un prodotto con HyA reticolato, ad alto peso molecolare, a una concentrazione più alta o un prodotto combinato con polinucleotidi e HyA ad alto peso molecolare a una concentrazione più alta. Studi di laboratorio su cellule parodontali o patogeni associati alla parodontite hanno confrontato gli effetti di HyA non reticolato e reticolato o di HyA di diversi pesi molecolari; nessuna delle formulazioni testate ha mostrato effetti negativi in termini di guarigione delle ferite parodontali. In questo contesto, a causa della mancanza di trial clinici comparativi fino ad ora, rimane poco chiaro se le diverse caratteristiche di HyA si traducano effettivamente in differenze clinicamente rilevanti. Un'altra differenza tra questi 2 RCT e qui riguarda la modalità/frequenza di applicazione di HyA. In questo studio, il gel contenente HyA è stato applicato ripetutamente (giornalmente) sopra il gengiva per 3 mesi dai pazienti, oltre alle applicazioni subgengivali in ufficio. Uno degli studi precedenti ha valutato l'effetto di un'applicazione in ufficio ripetuta dopo 3 mesi, ma non è riuscito a mostrare alcun effetto benefico aggiuntivo di HyA dopo la riapplicazione; tuttavia, prima della riapplicazione non è stata eseguita alcuna ulteriore strumentazione subgengivale in questo specifico studio. Qui, solo i siti con segni rimanenti di patologia hanno ricevuto una riapplicazione in combinazione con la reinstrumentazione subgengivale. In entrambi i gruppi (cioè, test e controllo) circa il 30% dei siti che richiedevano reinstrumentazione e riapplicazione sono stati giudicati come trattati con successo alla fine dello studio. Tuttavia, sebbene il ritratto abbia migliorato la situazione in 1 caso su 3 e non sia stato notato alcun effetto benefico distintivo di HyA, il numero di siti che richiedevano reinstrumentazione (ritratto) a 3 mesi era significativamente inferiore nel gruppo HyA, rispetto a quello che riceveva NaCl. Infine, anche i dati attuali non consentono alcuna conclusione su un potenziale effetto aggiuntivo dell'applicazione sopra il gengiva ripetuta da parte dei pazienti per 3 mesi, poiché qui mancava un terzo gruppo con somministrazione subgengivale in ufficio solo.
In generale, ridurre il numero di tasche residue dopo il trattamento parodontale attivo (cioè, fase 1 a 3) si è dimostrato vantaggioso in termini di ricorrenza/progressione della malattia e perdita di denti in vari studi focalizzati sul SPC a lungo termine dopo il trattamento parodontale attivo. Pertanto, è ragionevole assumere che qualsiasi misura terapeutica, come l'uso di ausili localmente applicati, che migliori il tasso di chiusura delle tasche - indipendentemente dalla fase del trattamento - possa contribuire positivamente anche all'esito a lungo termine. In questo contesto, i gel contenenti HyA come ausilio all'istrumentazione subgengivale nella seconda fase della terapia hanno mostrato un certo potenziale in termini di riduzione della PPD e del BoP, che è stato riconfermato da studi RCT più recenti. Rispetto ad altri studi con un disegno di studio simile ma che valutano prodotti diversi come ausili per la reinstrumentazione delle tasche residue nei pazienti con SPC, la frequenza di chiusura delle tasche è apparsa leggermente inferiore in questo caso. Ad esempio, 2 recenti RCT che valutano l'effetto ausiliario dell'applicazione senza lembo di derivati della matrice di smalto, gel di ipoclorito di sodio e gel di clorexidina hanno riportato chiusura delle tasche (cioè, PPD ≤ 4 mm senza BoP) nell'80%, 78% e 63% dei siti rispetto al 57% in questo caso. Pertanto, e considerando la mancanza di RCT che confrontano direttamente questi prodotti, l'HyA è apparsa altrettanto efficace del gel di CHX, ma leggermente inferiore ai derivati della matrice di smalto e al gel di ipoclorito di sodio. Quest'ultimo potrebbe essere di particolare interesse, poiché la combinazione di gel di ipoclorito di sodio con gel di HyA reticolato ha recentemente ricevuto attenzione come trattamento ausiliario combinato nei pazienti con parodontite. Tuttavia, una recente serie di casi retrospettiva che include 29 pazienti con SPC con tasche residue/ricadenti ha riportato per questo approccio combinato un tasso di chiusura delle tasche leggermente inferiore del 25%.
Tra i fattori confondenti utilizzati per l'aggiustamento dell'analisi attuale, due hanno avuto un effetto significativo sull'esito alla valutazione finale, ovvero il controllo della placca e la compliance/tempo, che sono entrambi ben in accordo con la letteratura. In particolare, qui la presenza di placca, che è stata valutata in ciascun sito sperimentale ad ogni sessione di SPC, ha ridotto significativamente le probabilità di ottenere la chiusura della tasca. Motivare con successo i pazienti a mantenere livelli elevati di controllo della placca durante il SPC è una sfida clinica ben nota e recenti studi SPC a lungo termine hanno riconfermato la rilevanza clinica di ciò. Entrambi gli studi, che hanno incluso rispettivamente 100 e oltre 200 individui, sottoposti a circa 10 anni di SPC dopo un trattamento parodontale attivo, hanno mostrato un aumento del rischio di recidiva della malattia e perdita dei denti a causa della parodontite con scarso controllo della placca. Inoltre, i pazienti del presente RCT hanno mostrato in generale e indipendentemente dall'assegnazione del gruppo un miglioramento significativo nel tempo, che è diventato significativo dopo 12 mesi. In particolare, anche nel gruppo di controllo/placebo quasi il 50% dei siti sperimentali ha raggiunto la chiusura della tasca alla fine dello studio. Questa dimensione dell'effetto di ottenere la chiusura della tasca solo tramite reinstrumentazione meccanica è ben comparabile con studi precedenti che riportano tassi del 42 al 60%. Inoltre, la partecipazione allo studio di per sé probabilmente ha un effetto benefico sulla compliance dal punto di vista del paziente ma anche dal punto di vista del dentista/igienista dentale trattante, che potrebbe essere più insistente nel mantenere l'intervallo di 3 mesi. In questo contesto, è stato dimostrato che un tempo più breve tra le sessioni consecutive di SPC può portare nel tempo a una riduzione della PPD e stabilità parodontale, mentre un tempo più lungo può portare a instabilità parodontale e successivamente a perdita dei denti.
Lo studio attuale – condotto in condizioni di “vita reale” – presenta alcune limitazioni, come un tasso di abbandono relativamente alto del 30%, che non ci ha permesso di raggiungere la dimensione del campione prevista nel gruppo di controllo/placebo, ovvero sono stati analizzati 26 partecipanti invece di 30. L'alto tasso di abbandono è dovuto almeno in parte al fatto che i partecipanti hanno perso i loro appuntamenti programmati durante la pandemia di Covid-19, ovvero, sebbene fosse accettato un intervallo di 2,5-5 mesi tra 2 sessioni di SPC, quasi il 10% dei partecipanti (cioè 2 e 5 del gruppo test/HyA e del gruppo di controllo/placebo, rispettivamente) è stato escluso dall'analisi a causa di intervalli troppo lunghi. Tuttavia, poiché il tempo tra 2 sessioni di SPC appare come un fattore rilevante, questo parametro è stato incluso nelle analisi di regressione qui presentate, per correggere nel modello la leggera variazione negli intervalli di SPC. Tuttavia, poiché il presente studio è stato condotto in un design a gruppi paralleli, i pazienti non hanno ricevuto entrambi i prodotti, il che a sua volta dovrebbe limitare qualsiasi bias dovuto a una scarsa cecità dei pazienti. In questo contesto è stato interessante notare che i gruppi non presentavano differenze significative riguardo all'opinione dei pazienti sulla consistenza e sul gusto del prodotto; entrambi i prodotti sono stati ben accettati dai pazienti, il che a sua volta può indicare una buona compliance.
Conclusione
La reinstrumentazione delle tasche residue nei pazienti SPC, di per sé, porta a un aumento significativo della chiusura delle tasche nel tempo. Questo miglioramento dipendeva dall'igiene orale del paziente, cioè, la presenza di placca aumentava le probabilità di rimanere malati di circa 8 volte. L'applicazione ripetuta aggiuntiva di un gel contenente HyA, sia sotto che sopra il gengivale, ha portato a un numero significativamente inferiore di siti che richiedevano reinstrumentazione a 3 mesi, e a alcune differenze clinicamente rilevanti dopo 12 mesi di SPC rispetto al gruppo di controllo/placebo, come il 71% contro il 52% dei siti sperimentali che raggiungevano un PPD < 5 mm, rispettivamente. Tuttavia, la significatività statistica di questo effetto è stata marginalmente mancata nell'analisi aggiustata sul raggiungimento della chiusura delle tasche. Pertanto, sono necessari ulteriori studi clinici per confermare la superiorità di questo ausilio rispetto alla sola reinstrumentazione sottogengivale.
Autori: Kristina Bertl, Stefania Vlachou, Nikolaos Pandis, Antonios Zampelis, Andreas Stavropoulos
Riferimenti:
- Sanz M, Herrera D, Kebschull M et al (2020) Trattamento della parodontite di stadio I-III - Linee guida cliniche di livello S3 dell'EFP. J Clin Periodontol 47(Suppl 22):4–60. https://doi.org/10.1111/jcpe.13290
- Suvan J, Leira Y, Moreno Sancho FM, Graziani F, Derks J, Tomasi C (2020) Strumentazione sottogengivale per il trattamento della parodontite. Una revisione sistematica. J Clin Periodontol 47(Suppl 22):155–175. https://doi.org/10.1111/jcpe.13245
- Chapple ILC, Mealey BL, Van Dyke TE et al (2018) Salute parodontale e malattie e condizioni gengivali su un parodonto intatto e ridotto: rapporto di consenso del gruppo di lavoro 1 del World Workshop 2017 sulla classificazione delle malattie e condizioni parodontali e peri-implantari. J Clin Periodontol 45(Suppl 20):S68–S77. https://doi.org/10.1111/jcpe.12940
- Bertl K, Pandis N, Stopfer N, Haririan H, Bruckmann C, Stavropoulos A (2022) L'impatto dello stato di "paziente con parodontite trattata con successo e stabile" sui parametri di esito correlati al paziente durante la cura parodontale di supporto a lungo termine. J Clin Periodontol 49:101–110. https://doi.org/10.1111/jcpe.13582
- Rattu V, Raindi D, Antonoglou G, Nibali L (2023) Prevalenza di soggetti con parodontite stabile e trattata con successo e incidenza della successiva perdita dentale durante la cura parodontale di supporto: una revisione sistematica con meta-analisi. J Clin Periodontol. https://doi.org/10.1111/jcpe.13835
- Donos N, Calciolari E, Brusselaers N, Goldoni M, Bostanci N, Belibasakis GN (2020) L'uso adiuvante di modulatori dell'ospite nella terapia parodontale non chirurgica. Una revisione sistematica di studi clinici randomizzati controllati con placebo. J Clin Periodontol 47(Suppl 22):199–238. https://doi.org/10.1111/jcpe.13232
- Herrera D, Matesanz P, Martín C, Oud V, Feres M, Teughels W (2020) Effetto adiuvante degli antimicrobici somministrati localmente nella terapia della parodontite: una revisione sistematica e meta-analisi. J Clin Periodontol 47(Suppl 22):239–256. https://doi.org/10.1111/jcpe.13230
- Calciolari E, Ercal P, Dourou M, Akcali A, Tagliaferri S, Donos N (2022) L'efficacia delle terapie parodontali adiuvanti durante la cura parodontale di supporto in pazienti con tasche residue. Una revisione sistematica e meta-analisi. J Periodontal Res 57:671–689. https://doi.org/10.1111/jre.13001
- Wang CY, Yang YH, Li H et al (2020) Trattamenti locali adiuvanti per pazienti con tasche residue durante la cura parodontale di supporto: una revisione sistematica e meta-analisi di rete. J Clin Peri- odontol 47:1496–1510. https://doi.org/10.1111/jcpe.13379
- Bertl K, Bruckmann C, Isberg PE, Klinge B, Gotfredsen K, Stavropoulos A (2015) Ialuronano nella terapia parodontale non chirurgica e chirurgica: una revisione sistematica. J Clin Periodontol 42:236–246. https://doi.org/10.1111/jcpe.12371
- Eliezer M, Imber JC, Sculean A, Pandis N, Teich S (2019) Acido ialuronico come adiuvante nella terapia parodontale non chirurgica e chirurgica: una revisione sistematica e meta-analisi. Clin Oral Investig 23:3423–3435. https://doi.org/10.1007/s00784-019-03012-w
- Karakostas P, Davidopoulou S, Kalfas S (2022) Uso di acido ialuronico nel trattamento della malattia parodontale: una revisione sistematica. J Contemp Dent Pract 23:355–370
- Tan OL, Safii SH, Razali M (2021) Efficacia clinica delle applicazioni ripetute di somministrazione locale di farmaci e agenti adiuvanti nella terapia parodontale non chirurgica: una revisione sistematica. Antibiotics (Basel) 10:1178. https://doi.org/10.3390/antibiotics10101178
- Pilloni A, Rojas MA, Trezza C et al (2023) Effetti clinici dell'uso adiuvante di gel a base di polinucleotide e acido ialuronico nella reinstrumentazione sottogengivale delle tasche parodontali residue: uno studio clinico randomizzato in split-mouth. J Periodontol 94:354–363. https://doi.org/10.1002/JPER.22-0225
- Pilloni A, Zeza B, Kuis D et al (2021) Trattamento delle tasche parodontali residue utilizzando un gel a base di acido ialuronico: uno studio clinico randomizzato multicentrico in triplo cieco di 12 mesi. Antibiotics (Basel) 10:924. https://doi.org/10.3390/antibiotics10080924
- Schulz KF, Altman DG, Moher D, CONSORT G (2010) Dichiarazione CON-SORT 2010: linee guida aggiornate per la segnalazione di studi clinici randomizzati a gruppi paralleli. PLoS Med 7:e1000251. https://doi.org/ 10.1371/journal.pmed.1000251
- Papapanou PN, Sanz M, Buduneli N et al (2018) Parodontite: rapporto di consenso del gruppo di lavoro 2 del World Workshop 2017 sulla classificazione delle malattie e condizioni parodontali e peri-implantari. J Clin Periodontol 45(Suppl 20):S162–S170. https:// doi.org/10.1111/jcpe.12946
- Tonetti MS, Greenwell H, Kornman KS (2018) Staging e grading della parodontite: quadro e proposta di una nuova classificazione e definizione di caso. J Clin Periodontol 45(Suppl 20):S149– S161. https://doi.org/10.1111/jcpe.12945
- Armitage GC (2000) Sviluppo di un sistema di classificazione per le malattie e condizioni parodontali. Northwest Dent 79:31–35
- Hamp SE, Nyman S, Lindhe J (1975) Trattamento parodontale dei denti multiradicolati. Risultati dopo 5 anni. J Clin Periodontol 2:126–135. https://doi.org/10.1111/j.1600-051x.1975.tb01734.x
- Asparuhova MB, Kiryak D, Eliezer M, Mihov D, Sculean A (2019) Attività di due preparati di ialuronano su fibroblasti orali umani primari. J Periodontal Res 54:33–45. https://doi.org/10. 1111/jre.12602
- Fujioka-Kobayashi M, Müller HD, Mueller A et al (2017) Effetti in vitro dell'acido ialuronico sulle cellule del legamento parodontale umano. BMC Oral Health 17:44. https://doi.org/10.1186/ s12903-017-0341-1
- Mueller A, Fujioka-Kobayashi M, Mueller HD et al (2017) Effetto dell'acido ialuronico sui cambiamenti morfologici delle superfici dentinali e successivo effetto sulla sopravvivenza, attacco e diffusione delle cellule del legamento parodontale. Clin Oral Investig 21:1013–1019. https://doi.org/10.1007/s00784-016-1856-6
- Chen M, Li L, Wang Z, Li P, Feng F, Zheng X (2019) L'acido ialuronico ad alto peso molecolare regola l'infiammazione e la migrazione indotte da P. gingivalis nei fibroblasti gengivali umani tramite la via di segnalazione MAPK e NF-κB. Arch Oral Biol 98:75–80. https:// doi.org/10.1016/j.archoralbio.2018.10.027
- Dannewitz B, Zeidler A, Hüsing J et al (2016) Perdita di molari in pazienti trattati parodontalmente: risultati dopo 10 anni e oltre dopo terapia parodontale attiva. J Clin Periodontol 43:53–62. https:// doi.org/10.1111/jcpe.12488
- Graetz C, Schützhold S, Plaumann A et al (2015) Fattori prognostici per la perdita di molari: uno studio retrospettivo di coorte di 18 anni. J Clin Periodontol 42:943–950. https://doi.org/10.1111/jcpe.12460
- Graetz C, Plaumann A, Schlattmann P et al (2017) Ritenzione dentale a lungo termine nella parodontite cronica - risultati dopo 18 anni di un regime di trattamento parodontale conservativo in un contesto universitario. J Clin Periodontol 44:169–177. https://doi.org/10.1111/jcpe.12680
- Matuliene G, Pjetursson BE, Salvi GE et al (2008) Influenza delle tasche residue sulla progressione della parodontite e sulla perdita dentale: risultati dopo 11 anni di mantenimento. J Clin Periodontol 35:685– 695. https://doi.org/10.1111/j.1600-051X.2008.01245.x
- Salvi GE, Mischler DC, Schmidlin K et al (2014) Fattori di rischio associati alla longevità dei denti multiradicolati. Risultati a lungo termine dopo terapia parodontale attiva e di supporto. J Clin Periodontol 41:701–707. https://doi.org/10.1111/jcpe.12266
- Ariel H, Kahn A, Hila ZO, Anton S, Natan G, Kolerman R (2022) Un gel termosensibile con un ingrediente attivo di acido ialuronico che contiene un sistema di conservazione a octenidina come adiuvante alla detartrasi e al livellamento radicolare: uno studio clinico prospettico randomizzato. Clin Oral Investig 26:3721–3733. https://doi.org/10.1007/s00784-021-04344-2
- Mohammad CA, Mirza BA, Mahmood ZS, Zardawi FM (2023) L'effetto del gel di acido ialuronico sui parametri parodontali, citochine pro-infiammatorie e marcatori biochimici nei pazienti con parodontite. Gels 9:325. https://doi.org/10.3390/gels9040325
- Olszewska-Czyz I, Kralik K, Prpic J (2021) Biomolecole nelle applicazioni dentali: studio clinico controllato randomizzato che valuta l'influenza della terapia adiuvante con acido ialuronico sui parametri clinici della parodontite moderata. Biomolecules 11:1491. https://doi.org/10.3390/biom11101491
- Ramanauskaite E, Machiulskiene V, Shirakata Y, Dvyliene UM, Nedzelskiene I, Sculean A (2023) Valutazione clinica dell'ipoclorito di sodio/aminoacidi e acido ialuronico reticolato come adiuvante al trattamento parodontale non chirurgico: uno studio clinico controllato randomizzato. Clin Oral Investig. https://doi.org/10.1007/ s00784-023-05271-0
- Jentsch HFR, Roccuzzo M, Pilloni A, Kasaj A, Fimmers R, Jepsen S (2021) Applicazione senza flap del derivato della matrice dentale nel ritratamento parodontale: uno studio di fattibilità randomizzato multicentrico. J Clin Periodontol 48:659–667. https://doi.org/10.1111/jcpe.13438
- Radulescu V, Boariu MI, Rusu D et al (2022) Effetti clinici e microbiologici di un'unica applicazione di gel di ipoclorito di sodio durante la reinstrumentazione sottogengivale: uno studio clinico randomizzato controllato in triplo cieco. Clin Oral Investig 26:6639–6652. https://doi.org/10.1007/s00784-022-04618-3
- Diehl D, Friedmann A, Liedloff P, Jung RM, Sculean A, Bilhan H (2022) Applicazione adiuvante di acido ialuronico in combinazione con un gel di ipoclorito di sodio per il trattamento non chirurgico delle tasche residue riduce la necessità di chirurgia parodontale: analisi retrospettiva di una serie di casi clinici. Materials (Basel) 15:6508. https://doi.org/10.3390/ma15196508
- Costa FO, Costa AM, Cortelli JR et al (2023) Effetto del controllo della placca sopra gengivale sulla parodontite ricorrente e sulla stabilità clinica tra gli individui in terapia di mantenimento parodontale: follow-up di 10 anni. J Periodontol 94:55–65. https://doi.org/10. 1002/JPER.22-0301
- Tomasi C, Koutouzis T, Wennström JL (2008) Doxiciclina somministrata localmente come adiuvante alla detartrasi meccanica nel ritratamento delle tasche parodontali. J Periodontol 79:431–439. https:// doi.org/10.1902/jop.2008.070383
- Ramseier CA, Nydegger M, Walter C et al (2019) Il tempo tra le visite di richiamo e le profondità di sondaggio residue predice la stabilità a lungo termine nei pazienti iscritti alla terapia parodontale di supporto. J Clin Periodontol 46:218–230. https://doi.org/10.1111/jcpe.13041