Acido ialuronico nell'estrazione dentale: una revisione sistematica e meta-analisi di studi preclinici e clinici
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Abstract
Obiettivi Valutare se negli animali o nei pazienti con ≥ 1 dente estratto, l'applicazione di acido ialuronico (HyA) risulti in una guarigione superiore e/o in una gestione migliorata delle complicanze rispetto a qualsiasi altro trattamento o nessun trattamento.
Materiali e metodi Tre database sono stati consultati fino ad aprile 2022. I criteri di idoneità più rilevanti erano (1) applicazione locale di HyA come complemento all'estrazione dentale o come trattamento dell'osteite alveolare, e (2) segnalazione di dati clinici, radiografici, istologici o riportati dai pazienti. La formazione di nuovo osso e/o la qualità sono stati considerati parametri principali di esito negli studi preclinici, mentre dolore, gonfiore e trisma sono stati definiti come parametri principali di esito negli studi clinici.
Risultati Cinque studi preclinici e 22 studi clinici (1062 pazienti alla valutazione finale) sono stati inclusi. Negli studi preclinici, HyA è stato applicato nella cavità di estrazione. Sebbene un effetto positivo di HyA sia stato osservato in tutti gli studi individuali sulla formazione ossea, questo effetto non è stato confermato dalla meta-analisi. Negli studi clinici, HyA è stato applicato nella cavità di estrazione o utilizzato come spray o collutorio. L'applicazione di HyA dopo l'estrazione non chirurgica di denti normalmente erotti può avere un effetto positivo sulla guarigione dei tessuti molli. Sulla base delle meta-analisi, l'applicazione di HyA dopo la rimozione chirurgica dei terzi molari inferiori (LM3) ha portato a una significativa riduzione della percezione del dolore 7 giorni dopo l'intervento rispetto a nessuna manipolazione aggiuntiva della ferita o all'applicazione di un placebo/portatore. Il dolore post-operatorio precoce, il trisma e l'estensione del gonfiore non sono stati influenzati.
Conclusioni L'applicazione di HyA può avere un effetto positivo nella riduzione del dolore dopo la rimozione dei LM3, ma non dopo l'estrazione di denti normalmente erotti.
Rilevanza clinica L'applicazione di HyA può avere un effetto positivo nella riduzione del dolore dopo la rimozione chirurgica dei LM3, ma non sembra avere alcun impatto su altre complicazioni o dopo l'estrazione di denti normalmente erotti. Inoltre, sembra non ridurre la modellazione dell'osso alveolare post-estrazione, anche se studi preclinici mostrano una formazione ossea migliorata.
Introduzione
Sebbene il processo di guarigione dopo l'estrazione di un dente sia comunemente senza eventi, qualsiasi dolore successivo può compromettere il benessere dei pazienti, mentre possono verificarsi anche complicazioni. Ad esempio, l'estrazione chirurgica di molari terzi semi-/completamente inclusi è regolarmente associata a dolore significativo, gonfiore e trisma, che sono aggravati in caso di sviluppo di osteite alveolare (AO)— chiamata anche alveolite secca. L'AO è considerata una delle complicazioni più frequenti dell'estrazione dentale che si verifica nel 20-35% dei casi di estrazione chirurgica dei molari terzi inferiori (LM3), e nell'1,4-5% delle estrazioni (non chirurgiche) di denti normalmente erotti. Oltre a tali complicazioni precoci, che influenzano negativamente la qualità della vita dei pazienti, la guarigione compromessa del sito di estrazione può anche portare a significativi difetti nei tessuti duri, sia nel sito di estrazione che nei denti adiacenti. Ad esempio, è stato riportato che difetti parodontali profondi, ad es., profondità di sondaggio ≥ 7 mm, nel lato distale del secondo molare si verificano in quasi ogni quarto paziente dopo l'estrazione di LM3 inclusi.
Per ridurre la morbidità dei pazienti e migliorare la guarigione dei tessuti molli e duri delle cavità estrattive, così come per il trattamento delle complicanze precoci (ad es., AO), sono stati testati vari materiali e/o tecniche chirurgiche (ad es., applicazione di spugne di collagene, gel, derivati del sangue, vari materiali di innesto). Negli ultimi tempi si è posta crescente attenzione all'acido ialuronico (HyA), grazie alle sue proprietà anti-infiammatorie e antibatteriche e ai suoi effetti positivi sulla guarigione dei tessuti molli e duri. In particolare, studi preclinici hanno dimostrato un effetto positivo, istologicamente, sulla guarigione di difetti ossei e parodontali dopo l'applicazione di HyA. Sulla base dei risultati delle meta-analisi di una revisione sistematica di studi clinici sull'estrazione chirurgica dei terzi molari, è stata riportata una significativa riduzione del dolore il terzo e il settimo giorno post-operatorio, ma non sul trisma, nei gruppi che ricevevano prodotti a base di HyA. In questo contesto, manca una valutazione completa delle evidenze precliniche e cliniche disponibili sugli effetti dell'applicazione di HyA in relazione all'estrazione dentale in generale, inclusa la prevalenza, l'estensione e/o la gestione delle complicanze. Pertanto, la presente revisione sistematica ha affrontato la seguente domanda PICOS (popolazione (P), intervento (I), confronto (C), risultati (O) e disegno dello studio (S)): “Negli animali/pazienti che hanno subito l'estrazione di ≥ 1 dente, l'applicazione di HyA da sola o combinata con altri prodotti/portatori porta a una guarigione superiore dei tessuti molli/duri, a una morbidità ridotta, a una riduzione del tasso di complicanze e/o a una migliore gestione delle complicanze rispetto a qualsiasi altro trattamento o nessun trattamento?”.
Materiali e metodi
Protocollo di studio e registrazione dello studio
Il presente lavoro ha seguito le linee guida disponibili per l'esecuzione di revisioni sistematiche di studi preclinici e clinici (Preferred Reporting Items for Systematic Reviews and Meta-analysis (PRISMA); Appendice 1). Entrambi i protocolli sono stati registrati presso il registro internazionale prospettico delle revisioni sistematiche (PROSPERO), cioè uno per il preclinico (CRD42021266190) e uno per gli studi clinici (CRD42021266183).
Fonti di informazione, ricerca bibliografica e criteri di idoneità
La ricerca bibliografica è stata effettuata in 3 database (cioè, Ovid (MEDLINE e CENTRAL), EMBASE e Pubmed) il 14 ottobre 2021, e aggiornata il 7 aprile 2022. I dettagli sulla ricerca, inclusi le parole chiave, sono presentati nell'Appendice 2. Dopo aver rimosso i duplicati, i titoli e gli abstract sono stati esaminati per idoneità da 2 revisori (DD, TL) e i valori kappa per i testi completi esaminati e le pubblicazioni infine incluse sono stati calcolati. Qualsiasi ambiguità è stata risolta in discussione con un terzo autore (KB). Indipendentemente dal tipo di studio, sono stati inclusi studi se (a) scritti in lingua inglese o tedesca, (b) il testo completo era disponibile, e (c) erano forniti dati clinici, radiografici o istologici. Ulteriori criteri di inclusione per gli studi preclinici erano (a) esperimenti controllati randomizzati e non randomizzati, e (b) applicazione locale di un prodotto a base di HyA da solo o in combinazione con un altro prodotto in ≥ 1 dei gruppi dopo l'estrazione di ≥ 1 dente. Ulteriori criteri di inclusione per gli studi clinici erano (a) studio controllato randomizzato (RCT), studio controllato (CT) o serie di casi con un minimo di 10 pazienti, e (b) applicazione locale di un prodotto a base di HyA da solo o in combinazione con un altro prodotto in ≥ 1 dei gruppi sia dopo l'estrazione di ≥ 1 dente sia come trattamento di AO di ≥ 1 dente.
Raccolta ed estrazione dei dati
Due autori (DD, KB) hanno estratto i dati in modo indipendente due volte e qualsiasi disaccordo è stato risolto in discussione con un terzo autore (AS). Dagli studi preclinici, sono state estratte le seguenti informazioni: (a) primo autore, (b) anno di pubblicazione, (c) disegno dello studio, (d) modello di trattamento, (e) sito di trattamento, (f) specie, (g) forma di applicazione dell'HyA, (h) gruppi di trattamento, (i) periodo di follow-up, (j) parametri di esito disponibili, e (k) dettagli sul finanziamento. Allo stesso modo, sono state estratte le seguenti informazioni dagli studi clinici: (a) primo autore, (b) anno di pubblicazione, (c) disegno dello studio, (d) caratteristiche dei pazienti (cioè, genere, età, stato di salute e fumo), (e) criteri di inclusione specifici per sito, (f) numero di siti alla baseline e all'ultimo follow-up, (g) gruppi di trattamento, (h) dettagli del prodotto, (i) forma di applicazione, (j) periodo di follow-up, (k) medicazione post-operatoria, (l) parametri di esito disponibili, (m) contesto clinico (cioè, pratica privata o contesto universitario), e (n) dettagli sul finanziamento. Infine, tutte le informazioni disponibili sui prodotti a base di HyA sono state riassunte, cioè, (a) nome commerciale, (b) produttore, (c) concentrazione, (d) forma chimica, e (e) forma di applicazione.
Valutazione del rischio di bias
Per i trial preclinici, è stato utilizzato lo strumento di valutazione del rischio di bias (RoB) di SYRCLE. Come suggerito, sono stati valutati i seguenti criteri come aventi RoB “basso”, “alto” o “non chiaro”: (1) generazione della sequenza, (2) caratteristiche di base, (3) occultamento dell'allocazione, (4) alloggio casuale, (5) mascheramento dei caregiver o dei ricercatori, (6) valutazione casuale degli esiti, (7) mascheramento del valutatore degli esiti, (8) dati sugli esiti incompleti, (9) reporting selettivo degli esiti e (10) altre fonti di bias. Per ogni studio, sono stati calcolati il numero e la percentuale degli elementi valutati positivamente (cioè, “punteggio di qualità”).
Per il RCT, è stato utilizzato lo strumento RoB 2.0 della Cochrane Collaboration. Il RoB è stato giudicato come avente preoccupazioni “basse”, “alte” o “alcune” per ciascuno dei seguenti criteri: (1) processo di randomizzazione, (2) deviazioni dalle interventi previsti, (3) dati sugli esiti mancanti, (4) misurazione dell'esito, (5) selezione del risultato riportato e (6) rischio complessivo di bias. Per i trial non randomizzati, è stato utilizzato lo strumento ROBINS-I. Il rischio di bias è stato giudicato come “basso”, “moderato”, “grave”, “critico” o “nessuna informazione” per i seguenti criteri: (1) confondimento, (2) selezione dei partecipanti, (3) classificazione delle interventi, (4) deviazioni dalle interventi previsti, (5) dati sugli esiti mancanti, (6) misurazione dell'esito, (7) selezione del risultato riportato e (8) rischio complessivo di bias.
La valutazione è stata effettuata da 2 revisori (DD, KB) e in caso di ambiguità è stato raggiunto un consenso attraverso una discussione con un terzo autore (AS). Un autore ha ripetuto la valutazione (DD).
Sintesi dei risultati e analisi statistica
Per gli studi preclinici, la formazione di nuovo osso e il volume osseo per volume di tessuto (BV/TV) sono stati considerati parametri principali di esito, mentre per gli studi clinici il dolore, il trisma e il gonfiore sono stati definiti come parametri principali di esito. I dati sono stati estratti dal testo, dalle tabelle e dalle figure, calcolati e/o sono stati contattati gli autori delle pubblicazioni originali.
Nel caso in cui siano stati identificati almeno 2 studi randomizzati con disegno di studio comparabile (cioè, indicazione al trattamento, regime di HyA, periodo di follow-up, valutazione degli esiti), è stata eseguita una meta-analisi a coppie. Le meta-analisi sono state limitate agli RCT, includendo quindi studi di maggiore qualità metodologica. I gruppi che applicavano HyA sono stati confrontati con un gruppo di controllo negativo (cioè, senza ulteriori passaggi di trattamento) o con un gruppo di controllo che applicava un altro trattamento, incluso un placebo o il materiale portante del gruppo di test (“placebo/portante”). Sono state eseguite meta-analisi a coppie per ciascun confronto separato così come per il complesso. È stata utilizzata la massima verosimiglianza ristretta per calcolare l'eterogeneità (τ2) e l'aggiustamento dell'errore standard di Knapp–Hartung per tener conto del numero ridotto di studi. La differenza media tra il gruppo di controllo e il gruppo di test, l'errore standard della differenza media e l'intervallo di confidenza (CI) al 95% sono stati calcolati. Negli studi che utilizzano il disegno a bocca divisa, i dati sono stati trattati come dipendenti nel calcolo dell'errore standard della differenza media impostando r = 0.5. Il test del chi-quadro è stato utilizzato per valutare l'eterogeneità, e un p-valore < 0.1 è stato considerato indicativo di un'eterogeneità significativa. Inoltre, è stato effettuato il test I2 per l'omogeneità per quantificare l'estensione dell'eterogeneità e nel caso di almeno 3 studi comparabili è stato calcolato anche l'intervallo di previsione al 95%. L'analisi statistica è stata eseguita con STATA/IC 17.0 per Mac.
Qualità delle prove (GRADE)
La certezza delle prove meta-analitiche degli studi preclinici e clinici inclusi in questo documento è stata riassunta dal Grading of Recommendations Assessment, Development and Evaluation (GRADE). Per entrambi gli studi preclinici e clinici, è stato utilizzato il software GRADEpro GDT (Guideline Development Tool, Università McMaster e Evidence Prime, 2022) per valutare la qualità delle prove dei risultati.
Risultati
Selezione e caratteristiche degli studi
La ricerca della letteratura è presentata nell'Appendice 3; sono state identificate 147 potenziali referenze e, dopo aver rimosso i duplicati, sono rimasti 90 studi per lo screening del titolo e dell'abstract. Un totale di 57 studi è stato rimosso per vari motivi, lasciando 33 studi per l'analisi del testo completo. Dopo aver escluso altri 6 studi in cui il tipo di prodotto non soddisfaceva i criteri di inclusione o il disegno dello studio era errato, sono stati inclusi nella presente revisione sistematica 5 studi preclinici e 22 studi clinici. Entrambi i revisori hanno concordato perfettamente sugli studi scelti per lo screening del testo completo (kappa di Cohen = 1; 100% di accordo), mentre è stato raggiunto un accordo sostanziale per l'iscrizione finale degli studi (kappa di Cohen = 0.61; 84.9% di accordo).
In tutti gli studi preclinici, l'HyA è stata applicata nella cavità dentale dopo l'estrazione di denti erotti regolarmente. Gli studi clinici sono stati suddivisi in 3 gruppi in base all'indicazione del trattamento: (1) rimozione chirurgica di LM3 (RCT (n = 10), CT (n = 1)), (2) estrazione di denti erotti regolarmente (RCT (n = 7), studio split-mouth non randomizzato (n = 1), serie di casi prospettici (n = 1)), e (3) trattamento di AO (RCT (n = 1), serie di casi prospettici (n = 1)).
Popolazione dello studio
Per quanto riguarda gli studi preclinici, 2 studi hanno incluso 5–11 ratti Holtzman o 5–6 ratti Wistar nei vari gruppi, rispettivamente, mentre 3 studi hanno utilizzato cani beagle (20 cani in totale). Negli studi sui ratti, l'HyA è stata applicata nella cavità di estrazione in animali sani o diabetici, mentre negli studi sui cani l'HyA è stata applicata in cavità di estrazione infette (Tabella 1).
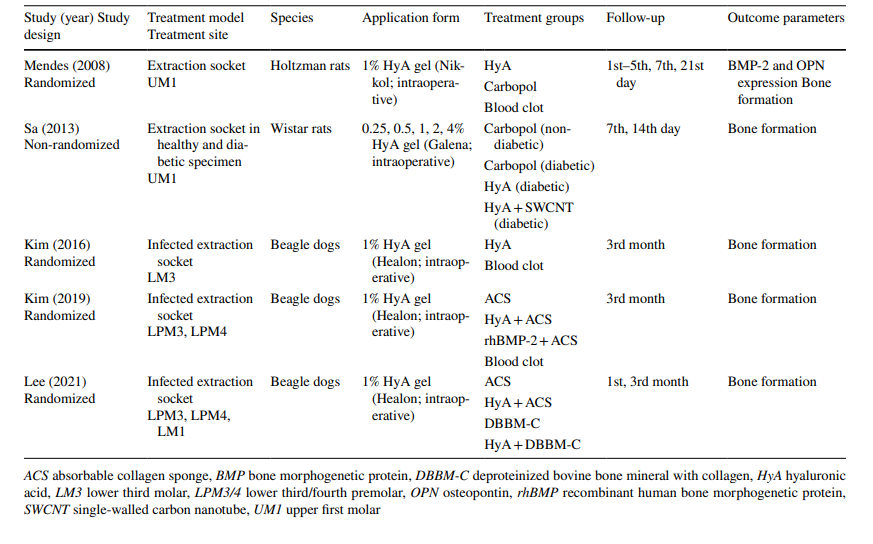
Gli studi clinici sulla rimozione chirurgica dei LM3, l'estrazione dei denti erotti regolarmente e il trattamento dell'AO hanno incluso rispettivamente 603, 349 e 110 pazienti nella valutazione finale, contribuendo con 306, 226 e 90 siti trattati con HyA, e 370, 257 e 20 siti di controllo/non trattati con HyA, rispettivamente (Tabella 2). Nella maggior parte degli studi, i pazienti erano sistemicamente sani, mentre uno studio riguardava pazienti con malattia epatica cronica o diabetici; 4 studi non hanno riportato lo stato di salute dei pazienti. Lo stato di fumatore è stato riportato in 12 studi; 8 studi includevano solo non fumatori, 2 studi includevano pazienti che fumavano ≤ 10 sigarette/giorno, e 2 studi includevano entrambi, cioè non fumatori e fumatori. Dieci studi non hanno fornito alcuna informazione sullo stato di fumatore.
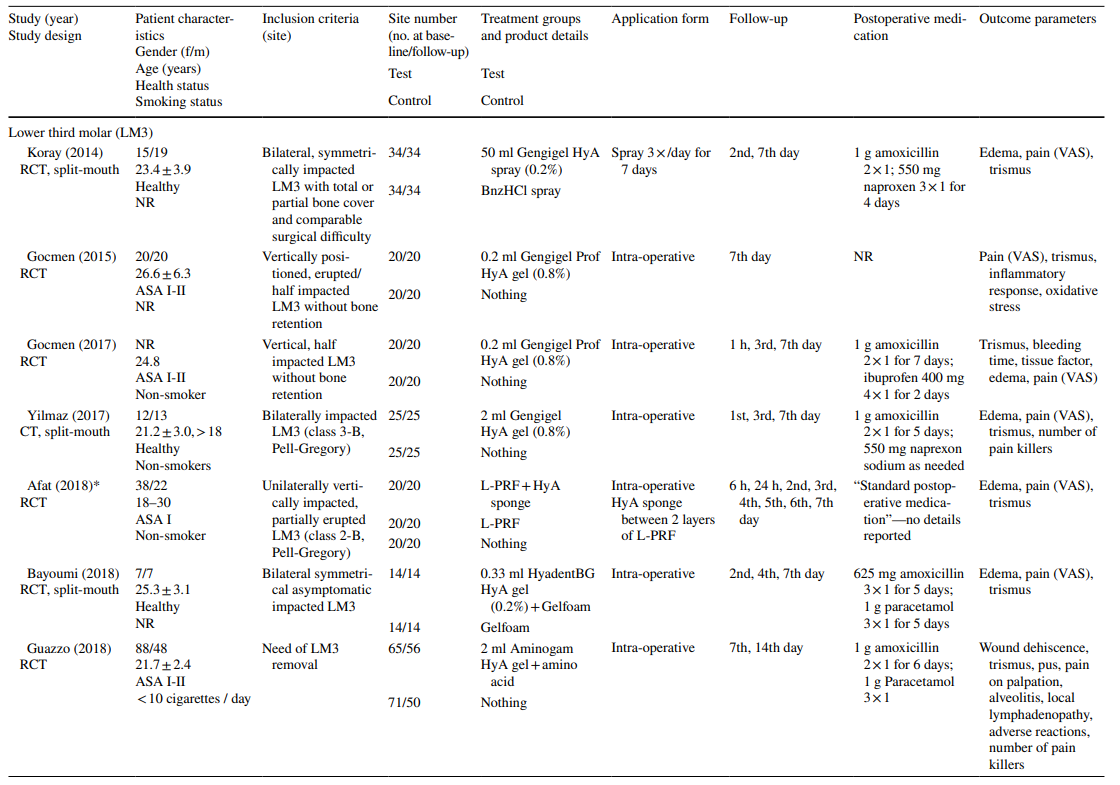
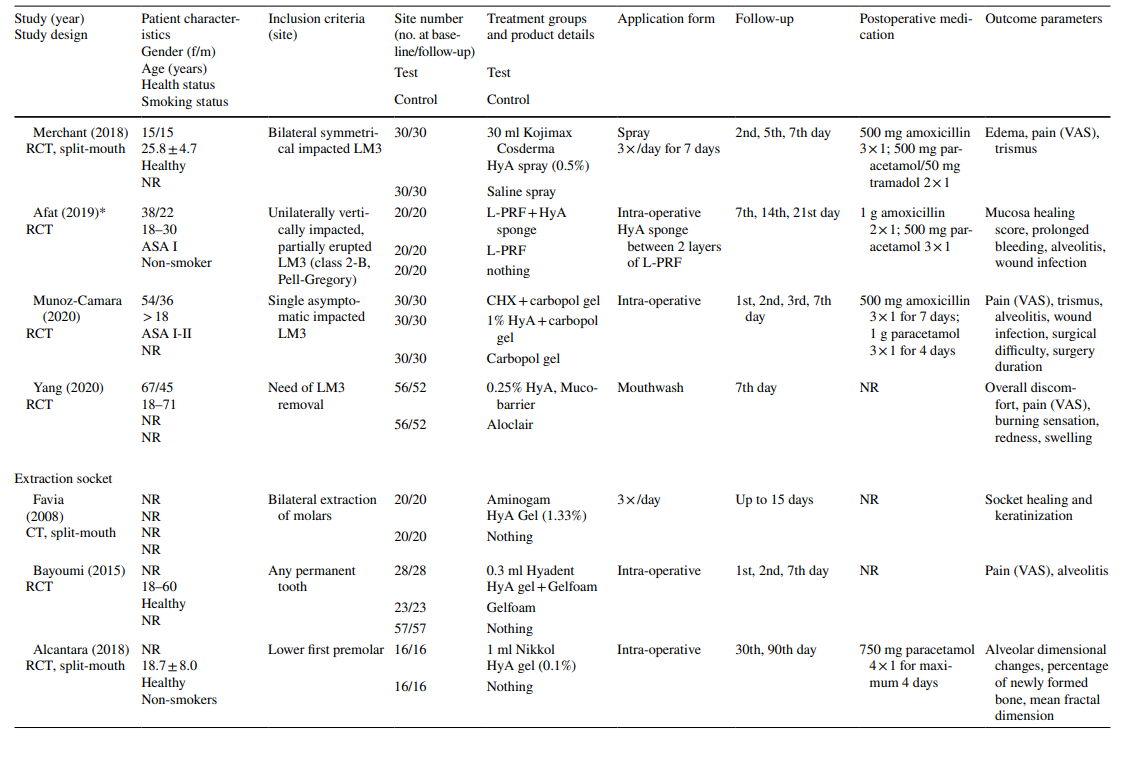
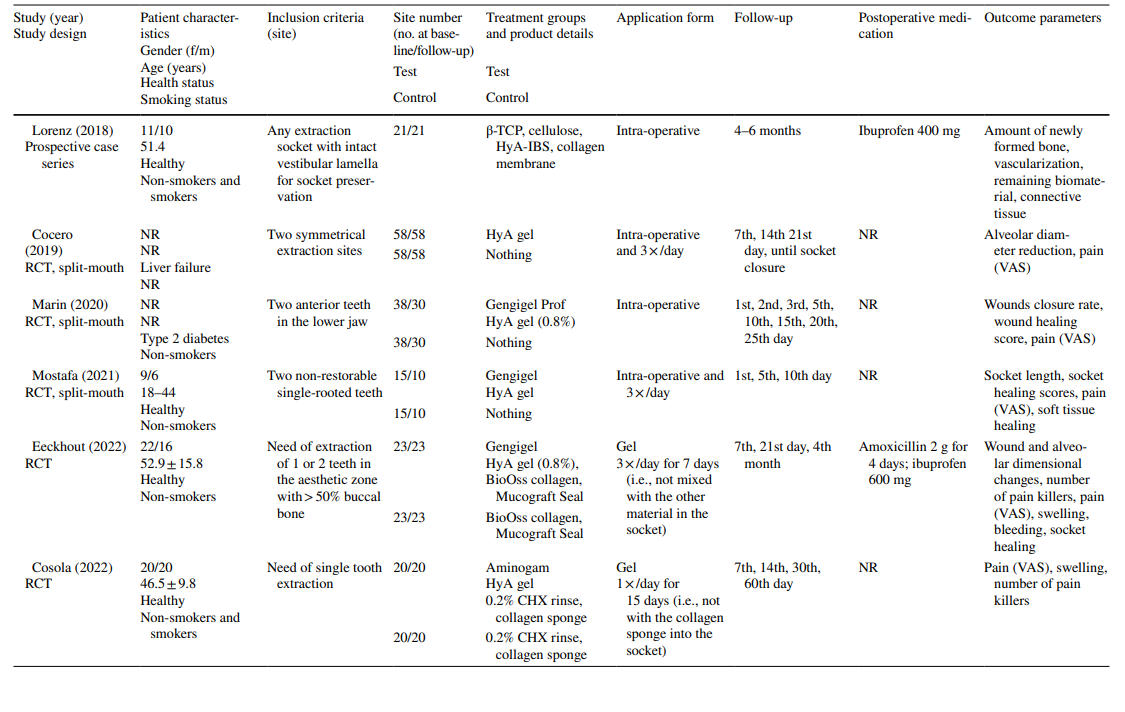
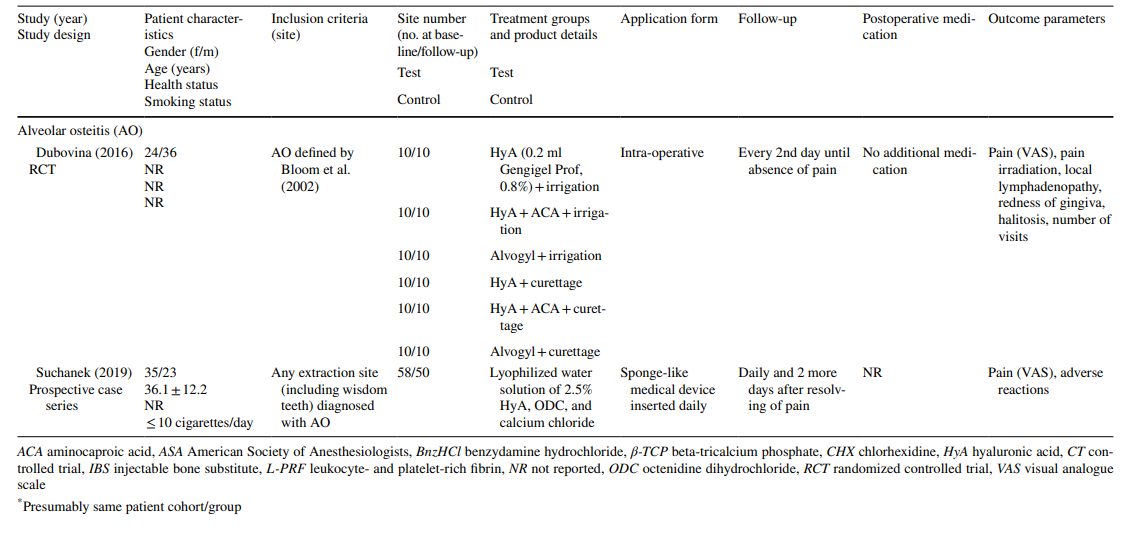
Negli studi sull'estrazione di LM3, i denti erano asintomatici, prevalentemente inclusi verticalmente o parzialmente inclusi, consentendo la chiusura primaria della ferita dopo la rimozione chirurgica. La metà degli studi sull'estrazione di denti erotti regolarmente includeva solo denti a radice singola (sia denti anteriori che premolari), mentre l'altra metà includeva molari o qualsiasi tipo di dente. Entrambi gli studi nel gruppo di trattamento AO includevano tutti i tipi di denti che soddisfacevano i criteri di AO secondo Blum et al. (2002).
Intervento dello studio
In tutti i trial preclinici, l'HyA è stata applicata come gel nella cavità di estrazione immediatamente dopo la rimozione del dente, sia da sola (n = 3) che in combinazione con una spugna di collagene assorbibile (n = 2) (Tabella 1).
Nella maggior parte degli studi clinici (n = 19) (Tabella 2), l'HyA è stata applicata come gel intraoperatoriamente nella cavità di estrazione o postoperatoriamente nel sito di estrazione, sia da sola (n = 13) che con alcuni portatori (cioè, spugna di collagene assorbibile (n = 3), fibrina ricca di leucociti e piastrine (n = 2) o sostituti ossei (n = 1)). Negli altri 3 studi clinici, l'HyA è stata utilizzata come spray 3 volte al giorno per 1 settimana (n = 2) o come collutorio (n = 1).
Informazioni su HyA
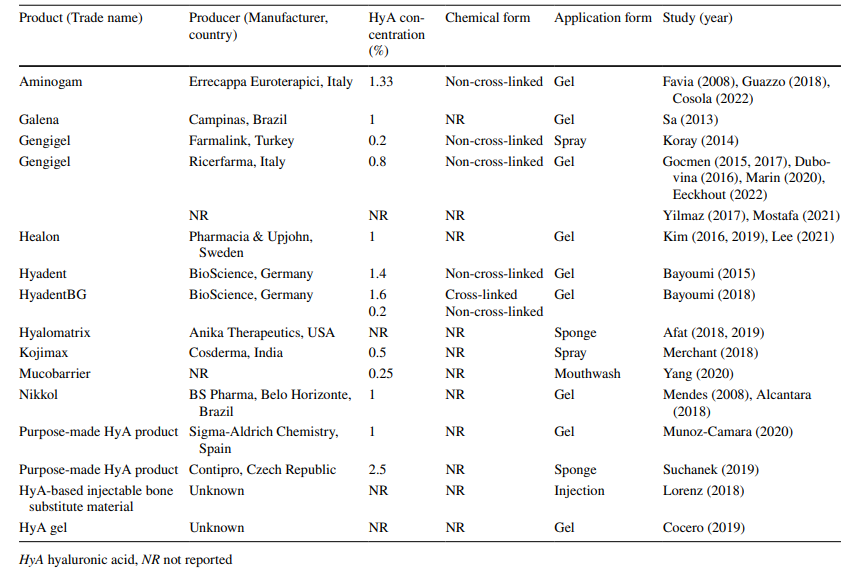
Nei 5 studi preclinici e 22 studi clinici inclusi, sono stati utilizzati 11 prodotti HyA commerciali, 2 fatti in casa e 2 di origine sconosciuta (Tabella 3). In tutti gli studi preclinici (n = 5), HyA è stato applicato come gel, mentre negli studi clinici HyA è stato applicato come gel (n = 15), spray (n = 2), collutorio (n = 1), o combinato con una spugna (n = 3) o materiale sostitutivo osseo (n = 1) durante il processo di fabbricazione. La concentrazione di HyA variava dallo 0,2% in uno spray, 0,25% in un collutorio, fino al 2,5% in una spugna HyA auto-combinata, mentre in 5 studi la concentrazione di HyA non è stata riportata. La forma chimica, cioè non reticolata o reticolata, non è stata riportata nella maggior parte degli studi (n = 16), mentre 10 studi hanno utilizzato HyA non reticolato e uno studio ha combinato HyA non reticolato e reticolato.
Dettagli sull'impostazione clinica e sul finanziamento
Tutti gli studi preclinici sono stati finanziati da sovvenzioni di ricerca indipendenti singole o multiple.
In uno studio clinico, è stato riportato un disegno di studio multicentrico che includeva 8 centri medici, mentre tutti gli altri studi clinici sono stati effettuati in un singolo dipartimento in un contesto universitario. Undici studi clinici non hanno riportato le fonti di finanziamento, mentre in 9 studi clinici il finanziamento è stato fornito dal dipartimento; tuttavia, in 3 di questi 9 studi, il gel di HyA è stato fornito dal produttore. In un singolo studio, il finanziamento è stato fornito da 3 diverse fondazioni di ricerca.
Variabili di esito riportate e follow‑up
Negli studi preclinici, la formazione ossea è stata valutata con diversi metodi tra 14 giorni e 3 mesi dopo l'intervento. Uno studio ha inoltre indagato il livello della proteina morfogenetica ossea-2 e dell'osteopontina (Tabella 1). Inoltre, 4 studi non hanno registrato effetti collaterali dopo l'applicazione di HyA, mentre uno studio non ha riportato assenze/presenze di effetti collaterali.
Negli studi clinici, i parametri di esito valutati variavano a seconda dell'indicazione terapeutica (Tabella 2). Negli studi sulla rimozione chirurgica dei LM3, la presenza di dolore misurata con la scala analogica visiva (VAS), gonfiore e trisma erano i parametri di esito più frequentemente valutati. Altri parametri valutati meno frequentemente erano la presenza/assenza di sanguinamento prolungato, la presenza/assenza di deiscenza dei tessuti molli, la velocità di guarigione della mucosa, il tasso di infezione AO/ferita e i marcatori di laboratorio di infiammazione, stress ossidativo e guarigione delle ferite. Tra gli studi sull'estrazione di denti erotti regolarmente, 3 pubblicazioni hanno utilizzato diversi punteggi di guarigione del sito/ tessuto molle, 3 pubblicazioni hanno valutato la quantità di osso neoformato e/o le variazioni dimensionali alveolari, 3 pubblicazioni hanno valutato il dolore e uno studio ha valutato il tasso di AO. Entrambi gli studi sul trattamento AO si sono concentrati sulla valutazione del dolore e delle reazioni avverse. La maggior parte degli studi clinici non ha registrato effetti collaterali dopo l'applicazione locale di HyA, mentre 6 studi non hanno menzionato l'assenza/presenza di effetti collaterali. Un singolo studio che ha applicato gel di HyA allo 0,8% dopo la rimozione del LM3 ha riportato un tempo di sanguinamento significativamente prolungato dopo la chiusura della ferita rispetto al gruppo di controllo; tuttavia, poiché l'emostasi era entro un intervallo fisiologico, questo non è stato considerato un evento avverso.
Riepilogo dei risultati dei singoli studi
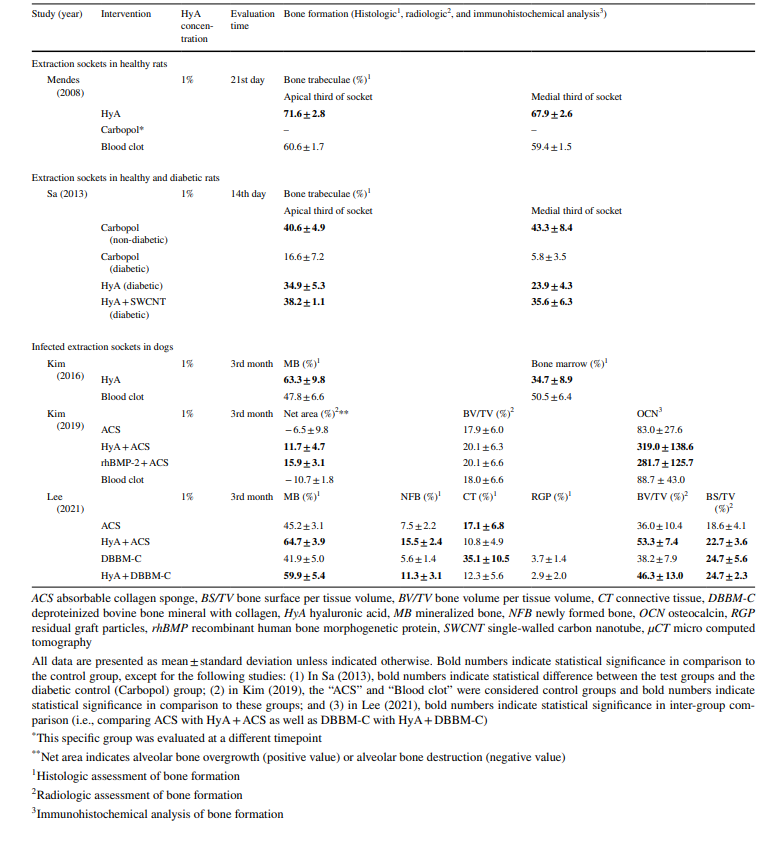
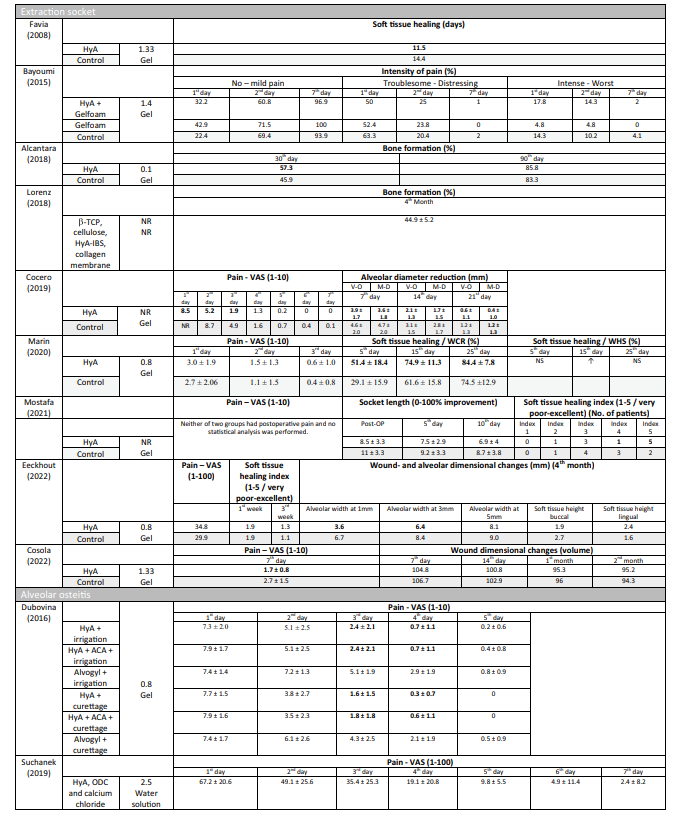
In tutti gli studi preclinici (Tabella 4), basati su analisi istologiche, radiologiche o immunoistochimiche, i gruppi di test con HyA hanno mostrato risultati significativamente migliori rispetto al gruppo di controllo in almeno uno dei parametri riguardanti la formazione ossea; questo era indipendente dalle condizioni del sito (sano o infetto) e dal tipo di trattamento di controllo.
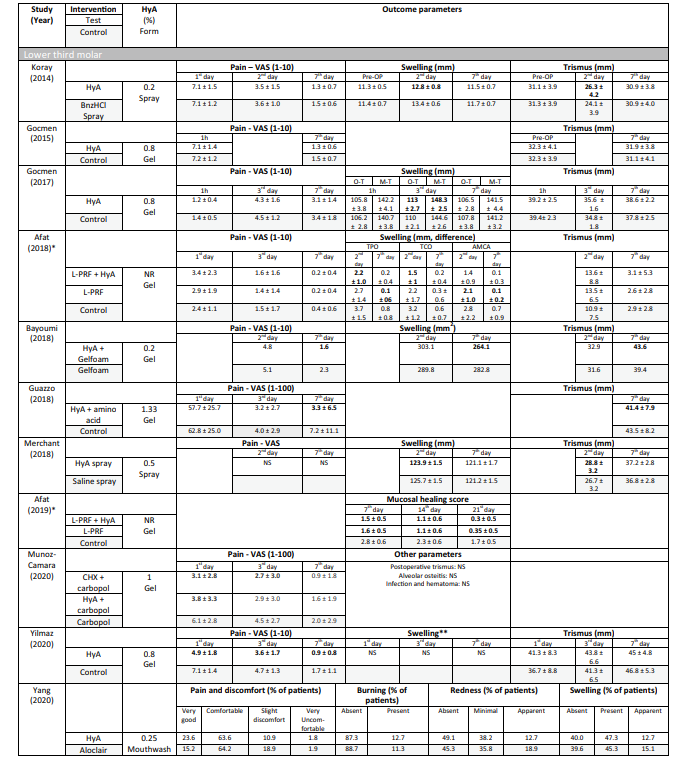
In 4 su 10 studi clinici sulla rimozione chirurgica del LM3 (Tabella 5) che riportano il dolore, sono stati segnalati vantaggi significativi per il gruppo di test che utilizzava HyA, rispetto al gruppo di controllo, in almeno un momento postoperatorio. Allo stesso modo, in 4 su 7 studi e in 3 su 9 studi che riportano rispettivamente gonfiore e trisma, sono stati segnalati vantaggi significativi a favore dell'applicazione di HyA rispetto al gruppo di controllo. In 3 su 4 studi che riportano la guarigione dei tessuti molli dopo l'estrazione di denti erotti regolarmente, è stata registrata una guarigione dei tessuti molli significativamente migliorata dopo l'applicazione di HyA rispetto al gruppo di controllo. Inoltre, uno studio ha riportato una formazione ossea migliorata dopo 30 giorni, uno studio ha riportato una riduzione diminuita del diametro alveolare dopo fino a 21 giorni, mentre 2 studi hanno riportato o nessuna differenza tra i gruppi o svantaggi significativi per il gruppo di test che utilizzava HyA in termini di cambiamenti dimensionali alveolari. Infine, la percezione del dolore è stata riportata in 6 studi, ma solo 2 studi hanno riportato differenze significative tra i gruppi a favore dell'applicazione di HyA. Uno studio che valutava il trattamento dell'AO ha riportato un dolore postoperatorio significativamente inferiore dopo l'applicazione di HyA rispetto all'applicazione di alvogyl; il secondo studio non aveva un gruppo di controllo.

Sintesi dei risultati
Studi preclinici—volume osseo per volume tissutale negli studi preclinici
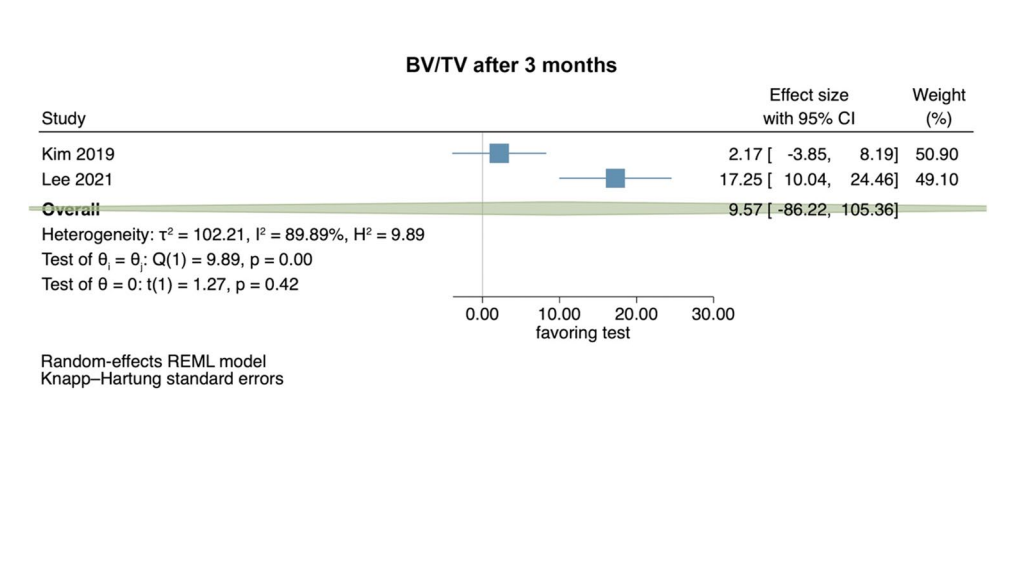
Due studi preclinici hanno fornito dati per riassumere il BV/TV valutato radiograficamente 3 mesi dopo l'intervento (Fig. 1). Gli studi hanno confrontato l'applicazione di HyA in combinazione con una spugna di collagene assorbibile rispetto alla spugna di collagene assorbibile. Complessivamente, non è stata identificata alcuna differenza significativa tra i gruppi (dimensione dell'effetto: 9.57; IC 95%: − 86.22 a 105.36; p = 0.42), ma l'eterogeneità statistica tra gli studi era significativa (I2 = 89.89%; p < 0.01).
Studi clinici—valutazione del dolore 2–3 e 7 giorni dopo la rimozione chirurgica del LM3
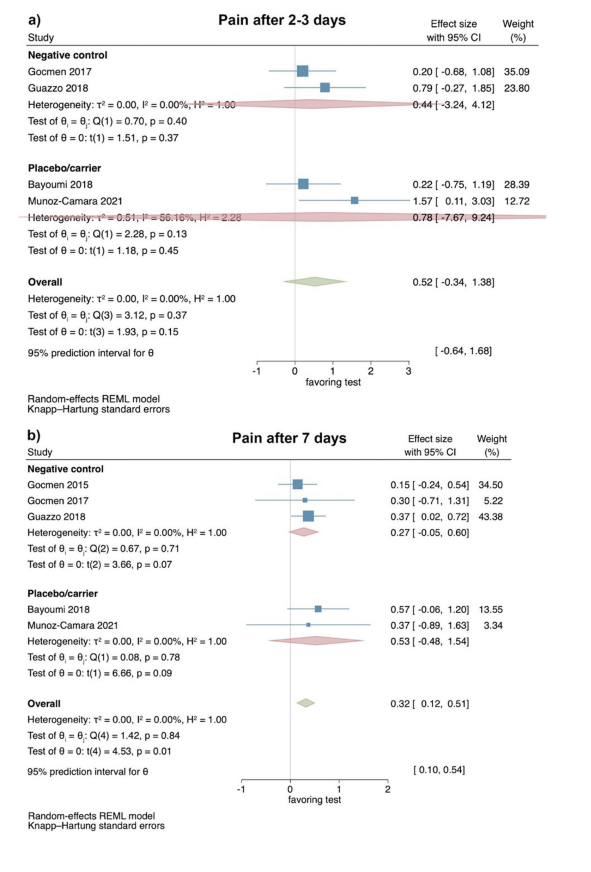
Basato sui risultati di 4 RCT, la percezione del dolore non ha mostrato differenze statisticamente significative tra i gruppi di test e di controllo 2–3 giorni dopo l'intervento (dimensione dell'effetto: 0.52; 95% CI: − 0.34–1.38; p = 0.15), senza eterogeneità statistica tra gli studi (I2 = 0.00%; p = 0.37). Analisi separate con 2 studi ciascuno che confrontano HyA con un gruppo di controllo negativo (dimensione dell'effetto: 0.44; 95% CI: − 3.24–4.12; p = 0.37) e HyA con un gruppo placebo/carrier (dimensione dell'effetto: 0.78; 95% CI: − 7.67–9.24; p = 0.45) mancavano anche di significatività statistica (Fig. 2a).
Basato sui risultati di 5 RCT, la percezione del dolore 7 giorni dopo l'intervento era significativamente inferiore nei gruppi di test che applicavano HyA (dimensione dell'effetto: 0.32; 95% CI: 0.12–0.51; p = 0.01), senza eterogeneità statistica tra gli studi (I2 = 0.00%; p = 0.84). Tuttavia, le analisi separate mancavano di significatività statistica per il confronto HyA con un gruppo di controllo negativo (3 studi; dimensione dell'effetto: 0.27; 95% CI: − 0.05–0.60; p = 0.07) e per il confronto HyA con un gruppo placebo/carrier (2 studi; dimensione dell'effetto: 0.53; 95% CI: − 0.48–1.54; p = 0.09; Fig. 2b).
Studi clinici—valutazione del gonfiore 2–3 e 7 giorni dopo la rimozione chirurgica del LM3
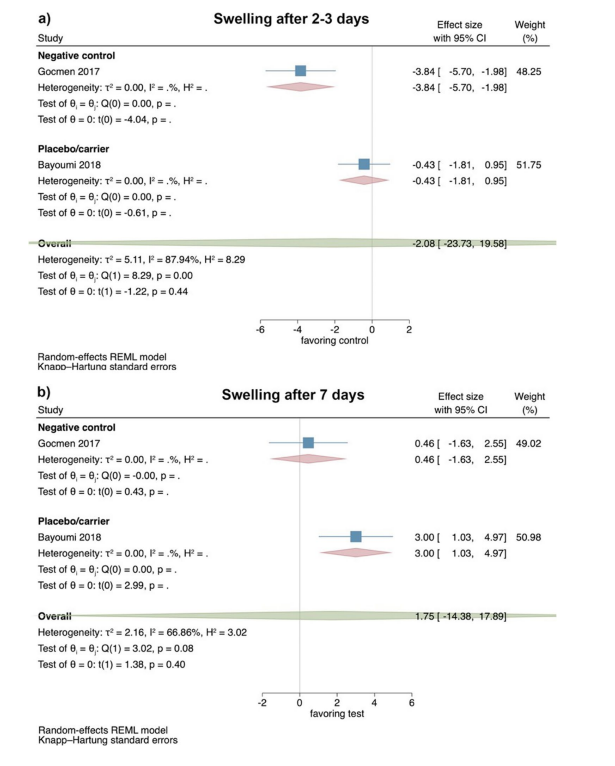
Sulla base dei risultati di 2 RCT, l'estensione del gonfiore 2–3 giorni postoperatori non ha mostrato differenze significative tra i gruppi di test e di controllo (dimensione dell'effetto: − 2.08; 95% CI: − 23.73–19.58; p = 0.44); tuttavia, l'eterogeneità statistica tra gli studi era significativa (I2 = 87.94%; p < 0.01; Fig. 3a).
Allo stesso modo, l'estensione del gonfiore 7 giorni dopo l'intervento chirurgico non ha mostrato differenze significative tra i gruppi di test e di controllo (dimensione dell'effetto: 1.75; IC 95%: − 14.38–17.89; p = 0.40), e l'eterogeneità statistica tra gli studi è stata nuovamente significativa (I2 = 66.86%; p = 0.08; Fig. 3b). Non è stata possibile un'analisi separata per il confronto tra HyA e un gruppo di controllo negativo o placebo/carrier a causa del numero limitato di studi.
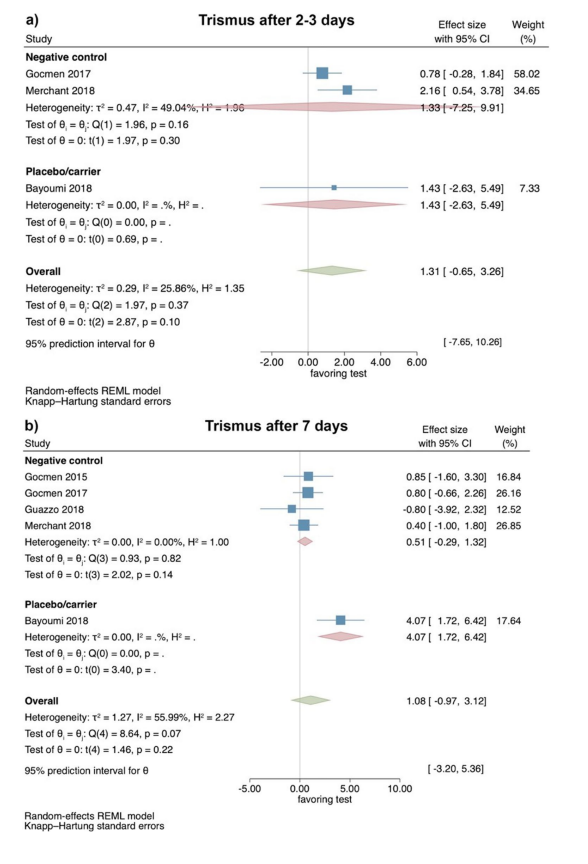
Studi clinici—valutazione del trisma 2–3 e 7 giorni dopo la rimozione chirurgica del LM3
Sulla base dei risultati di 3 RCT, il trisma non ha mostrato differenze significative tra i gruppi di test e di controllo 2–3 giorni dopo l'intervento (dimensione dell'effetto: 1.31; 95% CI: − 0.65–3.26; p = 0.10), senza eterogeneità statistica tra gli studi (I2 = 25.86%; p = 0.37). Le analisi separate non hanno mostrato significatività statistica per il confronto tra HyA e un gruppo di controllo negativo (2 studi; dimensione dell'effetto: 1.33; 95% CI: − 7.25–9.91; p = 0.30), mentre era disponibile solo un singolo studio per il confronto tra HyA e un gruppo placebo/carrier (Fig. 4a).
Sulla base dei risultati di 5 RCT, il trisma non ha mostrato differenze significative tra i gruppi di test e di controllo 7 giorni dopo l'intervento (dimensione dell'effetto: 1.08; 95% CI: − 0.97–3.12; p = 0.22); tuttavia, l'eterogeneità statistica tra gli studi era significativa (I2 = 55.99%; p = 0.07). Le analisi separate hanno anche mostrato nessuna differenza significativa tra HyA e un gruppo di controllo negativo (4 studi; dimensione dell'effetto: 0.51; 95% CI: − 0.29–1.32; p = 0.14), mentre era disponibile solo un singolo studio per il confronto tra HyA e un gruppo placebo/carrier (Fig. 4b).
Valutazione del rischio di bias
Tra gli studi preclinici, il punteggio di qualità variava tra il 20 e il 40% (Appendice 4); solo la segnalazione delle caratteristiche di base e altre fonti di bias sono state giudicate in tutti gli studi a basso rischio di bias.
Gli RCT inclusi sono stati giudicati come aventi alcune preoccupazioni (n = 13) o basso rischio di bias (n = 5) (Appendice 5). Nessuno degli RCT ha deviato dall'intervento previsto, 5 RCT sono stati giudicati come aventi alcune preoccupazioni nel processo di randomizzazione, e circa la metà degli studi è stata giudicata come avente alcune preoccupazioni nella loro reportistica sui dati di esito mancanti, misurazione dell'esito e selezione dei risultati riportati. La maggior parte degli studi non randomizzati è stata giudicata come avente un basso rischio di bias (n = 3), mentre uno studio è stato giudicato come avente alcune preoccupazioni (Appendice 6).
Qualità delle prove (GRADE)
Per i risultati della meta-analisi che include 2 trial preclinici, la certezza delle prove per il parametro di esito BV/TV dopo 3 mesi è stata valutata bassa (Appendice 8a).
La certezza delle prove ottenute da meta-analisi che includono trial clinici è stata giudicata come moderata per la percezione del dolore e il trisma e come bassa per la valutazione del gonfiore (Appendice 8b).
Discussione
È stato dimostrato che l'HyA possiede proprietà anti-infiammatorie, antiedematose, osteoinduttive e pro-angiogenetiche; pertanto, sembra che l'HyA migliori la guarigione delle ferite.
La presente revisione sistematica mirava a fornire una valutazione completa di tutte le evidenze disponibili (cioè, precliniche e cliniche) sull'effetto dell'applicazione di HyA in relazione all'estrazione dentale. In generale, sembra che l'applicazione di HyA in relazione alla rimozione chirurgica del LM3 possa avere un effetto positivo nella riduzione del dolore durante la prima settimana post-operatoria. In particolare, la meta-analisi di 5 studi clinici ha mostrato che l'applicazione locale (intra-chirurgica) del gel di HyA era associata a una percezione del dolore statisticamente significativamente ridotta 7 giorni dopo l'intervento chirurgico rispetto al gruppo di controllo con nessuna manipolazione aggiuntiva della ferita o l'applicazione di un placebo/carrier. L'applicazione di HyA non sembrava avere alcun impatto su altre complicazioni che si presentano spesso dopo la rimozione del LM3 (cioè, gonfiore e trisma) o in relazione all'estrazione non chirurgica di denti normalmente erotti.
Questo effetto positivo dell'applicazione intra-chirurgica di HyA sulla percezione del dolore nella prima settimana post-operatoria della rimozione del LM3 si aggiunge ai risultati di una precedente revisione sistematica, che ha valutato anche il possibile beneficio di HyA nella stessa indicazione. In particolare, sulla base di una selezione di studi diversa, l'applicazione di HyA ha ridotto significativamente il dolore sia il 3° che il 7° giorno post-operatorio. Apparentemente, l'effetto positivo di HyA nei primissimi giorni post-operatori osservato in quella revisione non è stato riscontrato nella presente meta-analisi, a causa delle informazioni aggiuntive fornite da 2 studi supplementari inclusi qui e a causa dell'esclusione di uno studio non randomizzato, che favoriva fortemente il gruppo di test HyA. Un effetto positivo di HyA in termini di riduzione della percezione del dolore può essere parzialmente spiegato dal suo effetto modulante sulla risposta infiammatoria nel sito chirurgico. È stato precedentemente dimostrato che HyA può downregolare la produzione e l'espressione della prostaglandina E2, della bradichinina e della sostanza P, tutte coinvolte nella trasmissione e nella sensazione del dolore. Tuttavia, qualsiasi potenziale effetto positivo di HyA sulla risposta infiammatoria locale non si traduce necessariamente in meno gonfiore e/o trisma in clinica, poiché sia le analisi incluse qui che quelle nella revisione sopra menzionata non hanno indicato differenze tra i gruppi di test e di controllo riguardo a questi aspetti. Tuttavia, questi risultati devono essere interpretati con cautela a causa del numero ridotto di studi originali e della mancanza di standardizzazione nei metodi di valutazione del gonfiore facciale così come nell'intervento stesso. Ad esempio, gli studi inclusi raramente fornivano informazioni sul livello di difficoltà chirurgica e/o sul design del lembo applicato, aspetti che possono influenzare i parametri di esito. Inoltre, la mancanza di un effetto positivo significativo di HyA nella percezione del dolore nell'estrazione non chirurgica di denti erotti regolarmente, riscontrata nella maggior parte degli studi (4 su 5) inclusi in questa revisione, non dovrebbe essere interpretata come una mancanza di azione di HyA in sé. Potrebbe essere dovuta a differenze nel modo di guarigione, cioè “chiuso” dopo la rimozione chirurgica del LM3 rispetto a “aperto” dopo l'estrazione di denti erotti regolarmente, dove la mancanza di chiusura primaria e di un qualsiasi portatore potrebbe aver portato a un rapido wash-out di HyA. Se l'applicazione di HyA in un portatore potrebbe migliorare la sua azione, è difficile da valutare, poiché è stata utilizzata solo in un singolo studio che non ha mostrato differenze. Tuttavia, va anche tenuto presente che nella maggior parte dei casi, l'estrazione dentale non complicata è associata a bassi livelli di dolore, e quindi qualsiasi possibile effetto positivo di HyA potrebbe essere difficile da catturare. Infatti, nell'unico studio comparativo sulla gestione dell'AO incluso in questa revisione, è stato riportato un dolore significativamente ridotto post-operatorio nei gruppi che ricevevano HyA (senza chiusura primaria e senza uso di un portatore).
Alcuni degli studi sulla guarigione dopo l'estrazione di denti erotti regolarmente, inclusi in questa revisione, hanno anche valutato il possibile impatto dell'applicazione di HyA sulla guarigione dei tessuti molli e duri. In 3 su 4 studi che valutavano la guarigione dei tessuti molli, è stato riportato un effetto positivo di HyA basato sul tempo fino e/o sulla percentuale di chiusura del sito, così come sui punteggi per giudicare la guarigione dei tessuti molli. Al contrario, in 3 studi comparativi, l'uso intra- o post-operatorio del gel di HyA non ha avuto alcun effetto positivo in termini di cambiamenti dimensionali alveolari rispetto all'assenza di applicazione di HyA, dopo un periodo di follow-up di 3-4 mesi. Infatti, in uno degli studi, dove dopo la preservazione dell'osso con innesto del sito con minerale osseo bovino deproteinizzato arricchito di collagene e sigillatura del sito mediante una matrice di collagene, il gel di HyA è stato applicato sulla matrice di collagene tre volte al giorno per 1 settimana, è stata osservata una perdita ossea orizzontale significativamente maggiore nell'aspetto coronale dei siti di estrazione. Questi risultati sulla mancanza di un effetto positivo di HyA sull'osso possono apparire in qualche modo in contrasto con i risultati riportati negli studi preclinici inclusi qui. Negli 2 studi che riportano sulla guarigione di siti di estrazione non infetti in ratti sani o diabetici, l'applicazione di HyA ha significativamente migliorato la guarigione ossea rispetto al gruppo di controllo. Allo stesso modo, in 3 su 3 studi su cani che riportano sulla guarigione di siti di estrazione infetti, l'applicazione di HyA, sia da sola che con una spugna di collagene o minerale osseo bovino deproteinizzato con collagene come vettore, ha migliorato la guarigione ossea. È importante menzionare, tuttavia, che questo effetto positivo di HyA sulla guarigione ossea non è stato mostrato nell'unica meta-analisi possibile qui riguardante BV/TV, probabilmente a causa del fatto che entrambi gli studi hanno utilizzato un tempo di guarigione tardivo per questo particolare modello animale; cioè, la guarigione ossea all'interno di un sito di estrazione nel cane è piuttosto avanzata dopo 3 mesi, anche senza alcun trattamento. È degno di nota che BV/TV nel gruppo HyA era simile a quello di un altro gruppo di test, trattato con proteina morfogenetica ossea umana ricombinante-2 (rhBMP-2), un noto agente potenziatore dell'osso molto potente. Inoltre, tali effetti positivi di HyA sulla guarigione ossea sono stati mostrati anche in altri studi preclinici, utilizzando modelli di difetto di dimensioni critiche. In prospettiva, nessuno studio sulla rimozione chirurgica di LM3 ha valutato l'esito della guarigione nell'aspetto distale del secondo molare inferiore, un sito spesso associato a un profondo difetto parodontale dopo l'estrazione di LM3 impattati.
Questa revisione ha cercato anche di identificare se l'applicazione di HyA possa ridurre il tasso di AO dopo l'estrazione dentale; tuttavia, ci sono state segnalazioni limitate su questa complicanza negli studi. In questo contesto, l'applicazione di HyA è generalmente considerata sicura e senza effetti collaterali; tuttavia, va detto che HyA può portare a eventi avversi significativi nel caso venga applicata (iniettata) all'interno dei tessuti. Qui, solo un singolo studio ha riportato un prolungamento del tempo di sanguinamento dopo la chiusura della ferita rispetto al gruppo di controllo; tuttavia, l'emostasi è stata giudicata all'interno di un intervallo fisiologico e quindi non considerata un evento avverso. Tutti gli altri studi inclusi in questa revisione non hanno menzionato effetti collaterali o complicazioni dopo l'applicazione di HyA. Oltre al fatto che HyA è sicura da applicare in relazione all'estrazione chirurgica LM3 o non chirurgica, non possono essere tratte conclusioni riguardo alla formulazione di HyA più efficiente (ad es., bassa vs. alta concentrazione, non incrociata vs. incrociata, gel vs. spray) o modalità di applicazione (ad es., con vs. senza un vettore, frequenza), e quindi non può essere fornita una chiara raccomandazione.
In totale, è stato possibile identificare solo un numero limitato di studi preclinici e clinici ben progettati e randomizzati, che sono stati combinati in una meta-analisi. Inoltre, come accennato sopra, c'è una mancanza di consenso e di informazioni sui dettagli dei prodotti HyA, ma anche sui dettagli chirurgici (ad esempio, livello di difficoltà chirurgica o design del lembo). Queste limitazioni hanno portato a una certezza complessiva delle evidenze bassa o moderata. Negli studi futuri, dovrebbe essere implementata una segnalazione migliore e più standardizzata sui dettagli dei prodotti HyA, dosaggio e applicazione, e tempi di follow-up più lunghi per consentire una valutazione più completa del potenziale utilizzo di HyA in relazione all'estrazione dentale. Inoltre, future revisioni sistematiche aggiornate che includano un numero maggiore di studi dovrebbero considerare nelle meta-analisi anche un confronto tra studi con bracci paralleli e studi in design split-mouth. Questo sarebbe di particolare interesse per parametri come la percezione del dolore, qualcosa di non fattibile qui a causa del numero molto limitato di studi split-mouth.
Conclusione
I risultati della presente revisione sistematica e delle meta-analisi hanno mostrato che l'applicazione intra-chirurgica di HyA in connessione con la rimozione chirurgica del LM3 ha portato a una significativa riduzione della percezione del dolore 7 giorni dopo l'intervento, mentre il dolore post-operatorio precoce, il trisma e l'estensione del gonfiore non sono stati influenzati. Inoltre, sembra che l'applicazione di HyA possa avere un effetto positivo sulla guarigione dei tessuti molli dopo l'estrazione non chirurgica di denti normalmente erotti, ma sembra non ridurre la modellazione dell'osso alveolare post-estrazione, anche se le evidenze provenienti da studi preclinici indicano che HyA potrebbe migliorare la formazione ossea.
Autori: Danijel Domic, Kristina Bertl, Tobias Lang, Nikolaos Pandis, Christian Ulm, Andreas Stavropoulos
Riferimenti:
- Upadhyaya C, Humagain H (2010) Prevalenza di secchezza della cavità dopo l'estrazione di denti permanenti presso l'ospedale universitario di Kathmandu (KUTH), Dhulikhel, Kavre, Nepal: uno studio. Kathmandu Univ Med J (KUMJ) 8(29):18–24
- Akinbami BO, Godspower T (2014) Secchezza della cavità: incidenza, caratteristiche cliniche e fattori predisponenti. Int J Dent 2014:796102
- Duarte-Rodrigues L et al (2018) Rimozione del terzo molare e il suo impatto sulla qualità della vita: revisione sistematica e meta-analisi. Qual Life Res 27(10):2477–2489
- Halabi D et al (2018) Clorexidina per la prevenzione dell'osteite alveolare: uno studio clinico randomizzato. J Appl Oral Sci 26:e20170245
- Kan KW et al (2002) Difetti parodontali residui distali al secondo molare mandibolare 6–36 mesi dopo l'estrazione del terzo molare incluso. J Clin Periodontol 29(11):1004–1011
- Peng KY et al (2001) Stato parodontale del secondo molare mandibolare dopo l'estrazione del terzo molare. J Periodontol 72(12):1647–1651
- MacBeth N et al (2017) Cambiamenti nei tessuti duri e molli dopo la preservazione dell'osso alveolare: una revisione sistematica. Clin Oral Implants Res 28(8):982–1004
- Taberner-Vallverdú M et al (2015) Efficacia di diversi metodi utilizzati per la gestione della secchezza della cavità: una revisione sistematica. Med Oral Patol Oral Cir Bucal 20(5):e633–e639
- Taberner-Vallverdú M, Sánchez-Garcés M, Gay-Escoda C (2017) Efficacia di diversi metodi utilizzati per la prevenzione della secchezza della cavità e analisi dei fattori di rischio: una revisione sistematica. Med Oral Patol Oral Cir Bucal 22(6):e750–e758
- Han W et al (2022) L'attività anti-infiammatoria di oligosaccaridi di acido ialuronico di dimensioni specifiche. Carbohydr Polym 276:118699
- Harris LG, Richards RG (2004) Adesione di Staphylococcus aureus a diverse superfici di titanio trattate. J Mater Sci Mater Med 15(4):311–314
- Romanò CL et al (2017) Acido ialuronico e i suoi compositi come barriera antimicrobica/antiadesiva locale. J Bone Jt Infect 2(1):63–72
- Matheus HR et al (2021) Associazione dell'acido ialuronico con un innesto bovino deproteinizzato migliora la riparazione ossea e aumenta la formazione ossea in difetti ossei di dimensioni critiche. J Periodontol 92(11):1646–1658
- Yun J, Lee J, Ha CW et al (2021) L'effetto di uno scaffold in acido polilattico stampato in 3D con e senza acido ialuronico sulla rigenerazione ossea. J Periodontol 1–11. https://doi.org/10.1002/JPER.21-0428
- Shirakata Y et al (2021) Guarigione delle recessioni gengivali buccali dopo trattamento con lembo avanzato coronale da solo o combinato con un gel di acido ialuronico reticolato: uno studio preclinico in cani. Quintessence Int 0(0):308–316
- Shirakata Y et al (2021) Guarigione delle recessioni gengivali buccali dopo trattamento con lembo avanzato coronale da solo o combinato con un gel di acido ialuronico reticolato: uno studio sperimentale in cani. J Clin Periodontol 48(4):570–580
- Maria de Souza G et al (2020) L'efficacia dell'acido ialuronico nel controllo del dolore, edema e trisma dopo l'estrazione dei terzi molari: revisione sistematica e meta-analisi. J Oral Maxillofac Surg 14:14
- de Vries R et al (2015) Un formato di protocollo per la preparazione, registrazione e pubblicazione di revisioni sistematiche di studi di intervento sugli animali. Evid-Based Preclin Med 2:e00007
- Page MJ et al (2021) La dichiarazione PRISMA 2020: una linea guida aggiornata per la segnalazione delle revisioni sistematiche. Syst Rev 10(1):89
- Hooijmans CR et al (2014) Strumento di rischio di bias di SYRCLE per studi sugli animali. BMC Med Res Methodol 14:43
- Sterne JAC et al (2019) RoB 2: uno strumento rivisto per valutare il rischio di bias negli studi randomizzati. BMJ 366:l4898
- Sterne JA et al (2016) ROBINS-I: uno strumento per valutare il rischio di bias negli studi non randomizzati di interventi. BMJ 355:i4919
- Higgins JPT, Thompson SG, Spiegelhalter DJ (2009) Una rivalutazione della meta-analisi a effetti casuali. J R Stat Soc A Stat Soc 172(1):137–159
- Wei D et al (2016) L'uso dell'approccio GRADE nelle revisioni sistematiche di studi sugli animali. J Evid Based Med 9(2):98–104
- Chen H et al (2015) Come utilizzare gradepro gdt per valutare la qualità delle evidenze nelle revisioni sistematiche di studi di intervento: un'introduzione. Chin J Evid Based Med 15:600–606
- Mendes RM et al (2010) Effetti dei nanotubi di carbonio a parete singola e della loro funzionalizzazione con sodio ialuronato sulla riparazione ossea. Life Sci 87(7–8):215–222
- Kapitan M et al (2021) Osservazione iniziale di fattori che interferiscono con il trattamento dell'osteite alveolare utilizzando acido ialuronico con octenidina: una serie di rapporti di casi. Biomolecules 11(8):04
- Martins-Junior PA et al (2016) Valutazione dei nanotubi di carbonio funzionalizzati con sodio ialuronato nei processi infiammatori per applicazioni di medicina rigenerativa orale. Clin Oral Invest 20(7):1607–1616
- Catanzano O et al (2018) Spugne composite alginato-ialuronano per la somministrazione di acido tranexamico in ferite alveolari post-estrattive. J Pharm Sci 107(2):654–661
- Mendes RM et al (2008) Il sodio ialuronato accelera il processo di guarigione nelle cavità dentali dei ratti. Arch Oral Biol 53(12):1155–1162
- Sa MA et al (2013) I nanotubi di carbonio funzionalizzati con sodio ialuronato ripristinano la riparazione ossea nelle cavità dentali di ratti diabetici. Oral Dis 19(5):484–493
- Kim JJ et al (2016) L'acido ialuronico migliora la formazione ossea nelle cavità di estrazione con patologia cronica: uno studio pilota in cani. J Periodontol 87(7):790–795
- Kim JJ et al (2019) Biomodificazione delle cavità di estrazione compromesse utilizzando acido ialuronico e rhBMP-2: uno studio sperimentale in cani. J Periodontol 90(4):416–424
- Lee JB et al (2021) Effetti dell'acido ialuronico e del minerale osseo bovino deproteinizzato con il 10% di collagene per la preservazione dell'osso in cavità di estrazione compromesse. J Periodontol 23:23
- Koray M et al (2014) Efficacia dello spray di acido ialuronico su gonfiore, dolore e trisma dopo l'estrazione chirurgica dei terzi molari mandibolari inclusi. Int J Oral Maxillofac Surg 43(11):1399–1403
- Gocmen G et al (2015) L'efficienza antiossidante e anti-infiammatoria dell'acido ialuronico dopo l'estrazione del terzo molare. J Craniomaxillofac Surg 43(7):1033–1037
- Gocmen G et al (2017) Effetti dell'acido ialuronico sul sanguinamento dopo l'estrazione del terzo molare. J Appl Oral Sci 25(2):211–216
- Afat İM, Akdoğan ET, Gönül O (2018) Effetti del fibrin ricco di leucociti e piastrine da solo e combinato con acido ialuronico su dolore, edema e trisma dopo l'estrazione chirurgica dei terzi molari mandibolari inclusi. J Oral Maxillofac Surg 76(5):926–932
- Bayoum A, Nadershah M, Albandar A, Alsulaimani B, Sankour I et al (2018) L'effetto dell'acido ialuronico reticolato nell'estrazione chirurgica dei terzi molari mandibolari inclusi. Int J Dent Oral Health 4(2). https://doi.org/10.16966/2378-7090.254
- Guazzo R et al (2018) Effetto sulla guarigione delle ferite di un gel topico contenente aminoacidi e sodio ialuronato applicato alla cavità alveolare dopo l'estrazione del terzo molare mandibolare: uno studio controllato randomizzato in doppio cieco. Quintessence Int 49(10):831–840
- Merchant R et al (2018) Valutazione comparativa dell'efficacia clinica dello spray di acido ialuronico rispetto allo spray di soluzione salina normale su gonfiore, dolore e trisma dopo l'estrazione chirurgica del terzo molare mandibolare incluso – uno studio controllato randomizzato a bocca divisa. Int J Sci Res 7:152
- Afat IM, Akdoğan ET, Gönül O (2019) Effetti del fibrin ricco di leucociti e piastrine da solo e combinato con acido ialuronico sulla guarigione precoce dei tessuti molli dopo l'estrazione chirurgica dei terzi molari mandibolari inclusi: uno studio clinico prospettico. J Craniomaxillofac Surg 47(2):280–286
- Munoz-Camara D, Pardo-Zamora G, Camacho-Alonso F (2020) Effetti post-operatori dell'applicazione intra-alveolare di gel bioadesivo di clorexidina allo 0,2% o di acido ialuronico all'1% dopo l'estrazione del terzo molare mandibolare: uno studio clinico controllato randomizzato in doppio cieco. Clin Oral Investig 24:24
- Yilmaz N et al (2017) L'efficacia dell'acido ialuronico nelle cavità post-estrazione dei terzi molari inclusi: uno studio pilota. Niger J Clin Pract 20(12):1626–1631
- Yang H et al (2020) Studio di non inferiorità dell'efficacia di due prodotti a base di acido ialuronico nelle cavità post-estrazione dei terzi molari inclusi. Maxillofac Plast Reconstr Surg 42(1):40
- Favia G et al (2008) Guarigione accelerata delle ferite dei tessuti molli orali e effetto angiogenico indotto da un pool di aminoacidi combinato con sodio ialuronato (AMINOGAM®). J Biol Regul Homeost Agents 22(2):109–116
- Bayoumi AM, Jan A, Amoudi WA, Shakir M (2015) Gli effetti dell'uso dell'acido ialuronico sulle cavità di estrazione. Int J Dent Oral Health 2(1). https://doi.org/10.16966/2378-7090.157
- Alcântara CEP et al (2018) L'acido ialuronico accelera la riparazione ossea nelle cavità dentali umane: uno studio clinico randomizzato in triplo cieco. Braz Oral Res 32:e84
- Lorenz J et al (2018) Materiale sostitutivo osseo iniettabile a base di beta-TCP e ialuronano raggiunge una completa rigenerazione ossea mentre subisce una degradazione quasi completa. Int J Oral Maxillofac Implants 33(3):636–644
- Marin S et al (2020) Risultato del trattamento con acido ialuronico sulla guarigione delle ferite post-estrazione in pazienti con diabete di tipo 2 mal controllato: uno studio controllato randomizzato a bocca divisa. Med Oral Patol Oral Cir Bucal 25(2):e154–e160
- Mostafa D et al (2021) Effetto del gel di acido ialuronico sulla guarigione delle cavità di estrazione dentale semplice: uno studio pilota. Open Access Maced J Med Sci 9(D):190–195
- Eeckhout C et al (2022) Uno studio controllato randomizzato che valuta il gel di acido ialuronico come agente di guarigione delle ferite nella preservazione dell'osso alveolare. J Clin Periodontol 49(3):280–291
- Cosola S, Oldoini G, Boccuzzi M, Giammarinaro E, Genovesi A, Covani U, Marconcini S (2022) Formula arricchita di aminoacidi per la cura post-operatoria delle cavità di estrazione valutata tramite scansione intraorale 3D. Int J Environ Res Public Health 19(6):3302. https://doi.org/10.3390/ijerph19063302
- Cocero N et al (2019) Efficacia del sodio ialuronato e degli aminoacidi sintetici nelle cavità post-estrattive in pazienti con insufficienza epatica: studio a bocca divisa. J Biol Regul Homeost Agents 33(6):1913–1919
- Dubovina D et al (2016) L'uso di acido ialuronico e acido aminocaproico nel trattamento dell'osteite alveolare. Vojnosanit Pregl 73(11):1010–1015
- Suchánek J, Ivančaková RK, Mottl R, Browne KZ, Pilneyová KC, Pilbauerová N, Schmidt J, Suchánková Kleplová T (2019) Dispositivo medico a base di acido ialuronico per il trattamento dell'osteite alveolare: studio clinico. Int J Environ Res Public Health 16:3698. https://doi.org/10.3390/ijerph16193698
- Blum IR (2002) Visioni contemporanee sulla secchezza della cavità (osteite alveolare): una valutazione clinica della standardizzazione, eziopatogenesi e gestione: una revisione critica. Int J Oral Maxillofac Surg 31(3):309–317
- Lee J-B, Chu S, Amara HB et al (2021) Gli effetti dell'acido ialuronico e del minerale osseo bovino deproteinizzato con il 10% di collagene per la preservazione dell'osso in cavità di estrazione compromesse. J Periodontol 1–12. https://doi.org/10.1002/JPER. 20-0832
- Sá MA et al (2013) I nanotubi di carbonio funzionalizzati con sodio ialuronato ripristinano la riparazione ossea nelle cavità dentali di ratti diabetici. Oral Dis 19(5):484–493
- Marin S et al (2020) Risultato del trattamento con acido ialuronico sulla guarigione delle ferite post-estrazione in pazienti con diabete di tipo 2 mal controllato: uno studio controllato randomizzato a bocca divisa. Medicina Oral, Patologia Oral y Cirugia Bucal 25(2):e154–e160
