Impianti di Disco Articolare Temporomandibolare Bioingegnerizzati: Protocollo di Studio per un Trial Pilota Preclinico Esplorativo Randomizzato in Due Fasi su 18 Pecore Merino Nere (TEMPOJIMS)
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Astratto
Background: I trial preclinici sono essenziali per testare opzioni efficaci per sostituire il disco dell'articolazione temporomandibolare (ATM). L'assenza contemporanea di un trattamento ideale per i pazienti con gravi disturbi dell'ATM può essere correlata a difficoltà riguardanti il design di studio appropriato per condurre trial preclinici nel campo dell'ATM. Queste difficoltà possono essere associate all'uso di modelli animali eterogenei, all'uso dell'ATM controlaterale come controllo, all'assenza di rigorosi trial preclinici controllati randomizzati con valutatori degli esiti in cieco e alle difficoltà che coinvolgono team multidisciplinari.
Obiettivo: Questo studio mira a sviluppare un nuovo design di studio riproducibile ed efficace per la ricerca preclinica nel dominio dell'ATM, ottenendo dati rigorosi relativi a (1) identificare l'impatto della discectomia bilaterale in pecore Merino nere, (2) identificare l'impatto della discopexia bilaterale in pecore Merino nere e (3) identificare l'impatto di tre diversi dischi TMJ bioingegnerizzati in pecore Merino nere.
Metodi: È stato proposto un trial preclinico controllato randomizzato esplorativo in due fasi con risultati ciechi. Nella prima fase, nove pecore vengono randomizzate in tre diverse procedure chirurgiche bilaterali: discectomia bilaterale, discopexia bilaterale e chirurgia simulata. Nella seconda fase, nove pecore vengono randomizzate per testare bilateralmente tre diversi impianti di disco bioingegnerizzati per l'ATM. L'esito primario è la gradazione istologica dell'ATM. Gli esiti secondari sono le modifiche di imaging, il tempo masticatorio assoluto, il tempo di ruminazione per ciclo, la cinetica della ruminazione, l'area di ruminazione e il peso delle pecore.
Risultati: Studi preclinici precedenti in questo campo hanno utilizzato il lato controlaterale non operato come controllo, diversi modelli animali che vanno dai topi a un modello canino, con disegni di studio non randomizzati, non ciechi e non controllati e misure di esito limitate. L'obiettivo principale di questo protocollo preclinico esplorativo è stabilire un nuovo standard per futuri trial preclinici in chirurgia oromaxillofacciale, in particolare nel campo dell'ATM, proponendo un design rigoroso in pecore Merino nere. Gli autori intendono anche testare la fattibilità degli esiti pilota. Gli autori si aspettano di aumentare la qualità di ulteriori studi in questo campo e di progredire nelle future opzioni di trattamento per i pazienti sottoposti a chirurgia per la sostituzione del disco dell'ATM.
Conclusioni: Lo studio è iniziato, ma è troppo presto per fornire risultati o conclusioni.
Introduzione
L'articolazione temporomandibolare (ATM) è l'articolazione più frequentemente utilizzata nel corpo umano. L'ATM si apre e si chiude 1500 a 2000 volte al giorno ed è essenziale per le funzioni quotidiane della bocca, come la masticazione, il linguaggio, la deglutizione, lo sbadiglio e il russare, coinvolgendo una sinergia obbligatoria speciale di entrambi i lati articolari. Il disco dell'ATM è un componente essenziale nell'ATM normale e ha le seguenti funzioni: (1) distribuisce il carico intra-articolare, (2) stabilizza le articolazioni durante la traduzione e (3) riduce l'usura della superficie articolare. La maggior parte dei disturbi dell'ATM (TMD) sono trattati con successo con trattamenti reversibili, conservativi e a bassa tecnologia come educazione e consulenza, esercizi terapeutici, terapia con splint e farmacoterapia.
Quando il disco dell'ATM è spostato, malformato o danneggiato, può indurre seri processi patologici interni e/o osteoartrite. Attualmente, i pazienti che soffrono di TMD severa hanno opzioni di trattamento validate limitate. La maggior parte degli approcci chirurgici, come la discectomia dell'ATM, non ripristina le proprietà strutturali o biologiche dell'articolazione e del disco. Questa procedura potrebbe non essere ideale poiché l'ATM rimane priva di una struttura funzionale importante. Una varietà di materiali interposizionali è stata utilizzata per sostituire i dischi rimossi, inclusi materiali sintetici prodotti in silicone, Teflon, politetrafluoroetilene e innesti biologici interposizionali prelevati da diversi siti anatomici. Questi materiali interposizionali non tengono in considerazione l'anatomia e le caratteristiche biochimiche e biomeccaniche del disco nativo dell'ATM, e alcuni di essi sono stati associati a gravi complicazioni per i pazienti. Alla fine degli anni '80, si è scoperto che Proplast/Teflon ATM (impianto interposizionale sintetico) erano dannosi per molti pazienti. La degradazione del materiale, probabilmente causata dalle elevate forze biomeccaniche dell'ATM, ha portato a particelle frammentate che hanno provocato una risposta immunitaria da corpo estraneo, causando problemi che vanno da gravi reazioni infiammatorie cutanee nelle aree preauricolari e guanciali a gravi malattie articolari degenerative con perforazione nella fossa cranica media. Il risultato è stato uno spettro clinico drammatico di fallimenti per questi impianti. Nel dicembre 1991, il bollettino della FDA statunitense ha raccomandato la rimozione immediata di tutti i precedenti impianti Proplast/Teflon ATM a causa dei fallimenti meccanici, molti dei quali hanno portato a una progressiva degenerazione ossea. In un workshop del 1992, l'Accademia Americana di Chirurgia Orale e Maxillofacciale ha istruito la cessazione dell'uso di Proplast/Teflon.
L'assenza di opzioni efficaci per sostituire il disco dell'ATM può essere correlata alle difficoltà nella traduzione delle evidenze animali nella pratica clinica negli esseri umani. Queste limitazioni sono probabilmente correlate a:
l'uso di modelli animali eterogenei con risultati contrastanti, probabilmente a causa di anatomia variabile e carico intra-articolare tra le specie;
l'uso dell'ATM controlaterale come controllo, che può essere associato a sovraccarico controlaterale;
i biomateriali utilizzati per sostituire il disco non tengono conto delle caratteristiche morfologiche e biomeccaniche del disco nativo;
assenza di studi controllati randomizzati con cieco per gli valutatori degli esiti; e
mancanza di team multidisciplinari coinvolti nel progetto.
La ricerca preclinica dovrebbe promuovere la efficace traduzione delle conoscenze nella pratica. Gli aspetti precedentemente menzionati possono limitare la traduzione efficace delle conoscenze scientifiche di qualità nella pratica clinica e questi possono presentare potenziali problemi per i pazienti, i clinici e il progresso scientifico.
L'assenza contemporanea di opzioni di successo per sostituire il disco dell'ATM è ancora un problema importante per la salute pubblica. Poco è cambiato nell'ultimo decennio riguardo ai disegni di studio per l'indagine sull'ATM, e il trattamento per i pazienti con TMD severa rimane controverso. L'obiettivo principale dello Studio sul Materiale Interposizionale dell'Articolazione Temporomandibolare (TEMPOJIMS) è sviluppare un nuovo disegno di studio riproducibile ed efficace per la ricerca preclinica nel campo dell'ATM. Il secondo obiettivo è progredire nella bioingegneria e nella medicina rigenerativa valutando i benefici di un impianto di bioingegneria dell'ATM per sostituire il disco nativo danneggiato. Questo studio esplorativo preclinico è suddiviso in due fasi. La Fase 1 di questo studio è un trial preclinico randomizzato in cieco, progettato per indagare se l'ATM subisce un'importante lesione in caso di discectomia bilaterale, discopexia bilaterale e chirurgia simulata. Le intenzioni della Fase 2 sono valutare la sicurezza e l'efficacia di tre diversi impianti di bioingegneria dell'ATM utilizzando lo stesso rigoroso metodo della fase 1.
Metodi
Progettazione dello Studio
Il TEMPOJIMS è uno studio preclinico controllato randomizzato esplorativo in due fasi progettato per raccogliere informazioni preliminari per (1) valutare un nuovo disegno di studio per l'indagine dell'ATM; (2) valutare il modello animale delle pecore Merino nere per l'indagine dell'ATM; (3) valutare il comportamento dell'ATM sotto intervento chirurgico bilaterale (discectomia e discopessia) utilizzando un esito primario istologico (valutazione microscopica dei cambiamenti distruttivi nell'ATM utilizzando un sistema di punteggio Mankin modificato), esito secondario di imaging (valutazione di imaging dell'ATM); (4) testare l'applicabilità di esiti secondari pilota prevalentemente per la cinetica dei ruminanti; e (5) ottenere una linea di base per l'interpretazione dei risultati degli impianti bioingegneristici del disco dell'ATM. La Fase II è mirata a testare la sicurezza e l'efficacia di tre diversi impianti bioingegneristici del disco dell'ATM bilaterali (Figura 1). Gli valutatori e gli analisti degli esiti sono ciechi per le valutazioni chirurgiche.
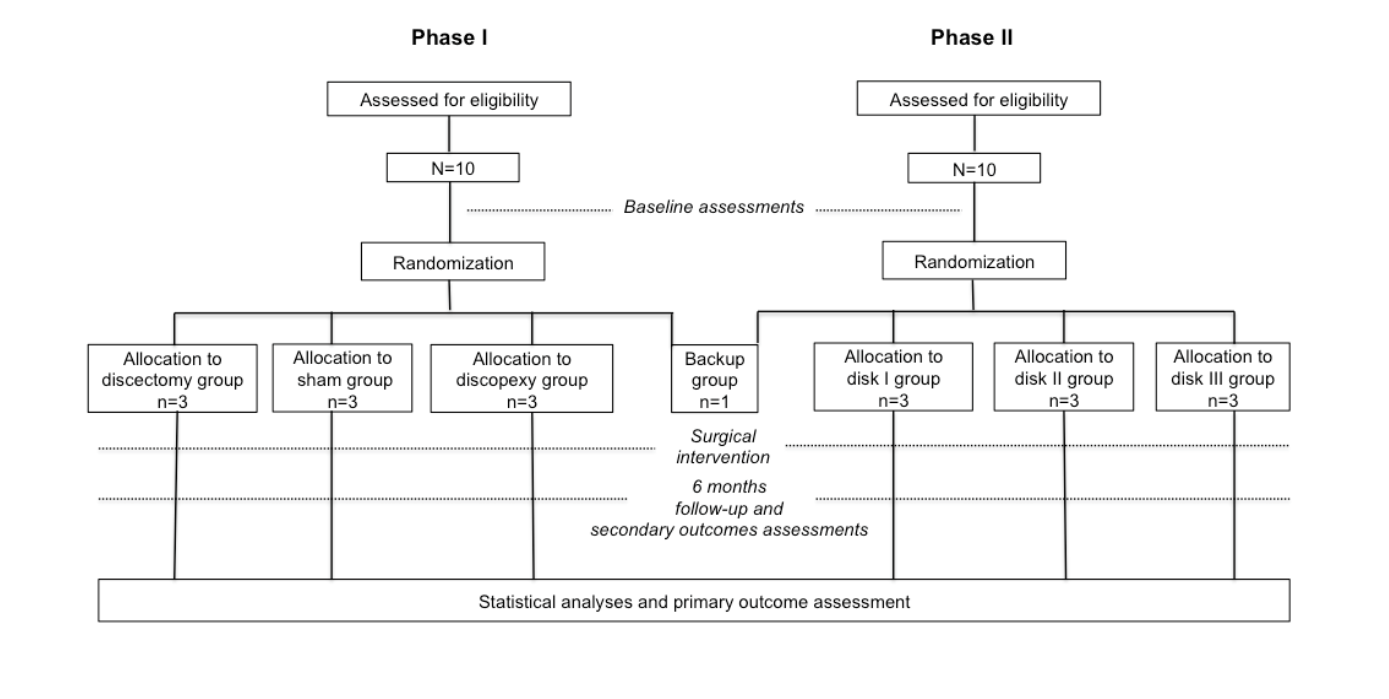
Le principali istituzioni coinvolte in questo studio sono (1) la Facoltà di Medicina di Lisbona per la progettazione dello studio, il coordinamento e l'analisi statistica; (2) il Centro Interdisciplinare di Ricerca in Salute Animale della Facoltà di Medicina Veterinaria per la preparazione istologica e il supporto veterinario di tutti gli animali; (3) il Centro per lo Sviluppo Rapido e Sostenibile di Prodotti per gli impianti a disco bioingegnerizzati (dischi I e II); (4) Bioingegneria, Chirurgia, Ingegneria Chimica, Ingegneria Meccanica e Scienza dei Materiali, Università di Pittsburgh, per gli impianti a disco bioingegnerizzati (disco III); (5) Dipartimento di Chirurgia Orale e Maxillo-Facciale-Collo e Testa, Ospedale Universitario Infanta Cristina, Badajoz, Spagna, per il supporto chirurgico; (6) Istituto di Ricerca sulle Ossa e le Articolazioni-Distretto Sanitario Locale di Sydney Settentrionale-Scuola Medica di Sydney Settentrionale, Università di Sydney, Australia, per l'analisi istologica; e (7) Dipartimento di Radiologia dell'Ospedale Santa Maria, Lisbona, Portogallo, per l'analisi delle immagini.
Modello Animale
Una varietà di ceppi/razze di pecore è stata utilizzata nelle indagini sull'ATM. Per ridurre la variabilità biologica, gli autori hanno raccomandato le pecore Merino nere come modello animale per condurre lo studio. Come raccomandato, gli autori hanno proposto di utilizzare “pecore scheletricamente mature” di età ≥2 anni. I criteri di inclusione sono pecore Merino nere certificate, adulte (età 2-5 anni), femmine e in buone condizioni di salute (viene effettuato un controllo veterinario su tutti gli animali). Per quanto riguarda le considerazioni etiche sugli animali, il disegno dello studio è stato approvato dall'Autorità Nazionale Portoghese per la Salute Animale registrata con il numero 026618. Il disegno e l'organizzazione dello studio rispettano le linee guida per la Ricerca Animale: Reporting of In Vivo Experiments (ARRIVE).
Valutazione Iniziale e di Follow-Up
Le valutazioni iniziali e di follow-up sono delineate in momenti specifici (Figura 2). Gli esiti secondari pilota e il peso vengono misurati nei giorni 11, 10 e 9 prima dell'intervento chirurgico (i dettagli sugli esiti secondari sono riportati nelle misure degli esiti). Il trasporto verso le strutture chirurgiche viene effettuato 5 giorni prima dell'intervento per evitare stress negli animali e consentire la familiarizzazione con le strutture temporanee. La tomografia computerizzata (TC) della testa viene eseguita il giorno dell'intervento sfruttando la sedazione pre-anestetica. Dieci giorni dopo l'intervento, gli animali vengono trasportati nelle principali strutture di TEMPOJIMS. Nei giorni 19, 20 e 21 dopo l'intervento, gli esiti secondari di follow-up iniziano a essere registrati ogni 30 giorni per 6 mesi (Figura 2). Alla fine, gli animali vengono sacrificati e viene eseguita una nuova TC per misurare l'esito dell'imaging e per iniziare la preparazione istologica.
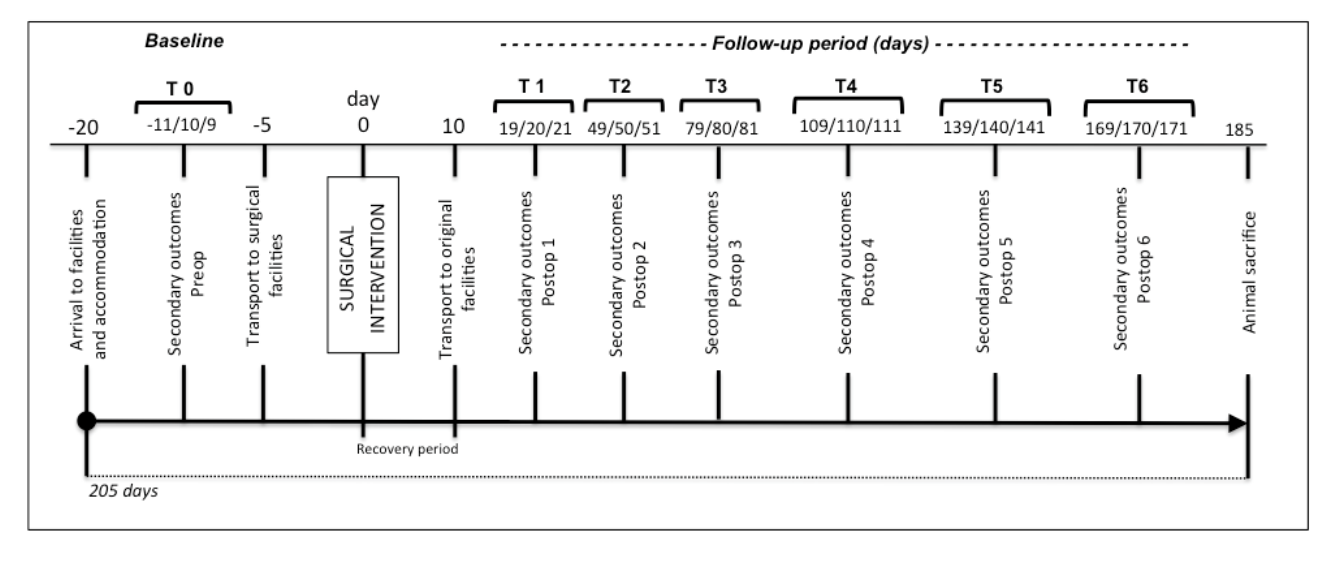
Randomizzazione, Assegnazione e Cieco
La randomizzazione è effettuata da un gruppo statistico non coinvolto nelle valutazioni dei risultati, gestito dalla Facoltà di Medicina di Lisbona. L'assegnazione a ciascun gruppo randomizzato viene effettuata preoperatoriamente tramite busta sigillata e separatamente per la fase 1 e la fase 2 dello studio. Il team chirurgico non è accecato rispetto all'assegnazione del trattamento data la tipologia di intervento; tuttavia, i membri del team chirurgico non sono coinvolti nelle valutazioni dei risultati. Tutti i valutatori dei risultati sono accecati rispetto all'intervento. Nella fase 1, 10 pecore sono assegnate al gruppo di intervento: gruppo di chirurgia simulata (n=3), gruppo di discectomia (n=3), gruppo di discopexia (n=3) e gruppo di riserva (n=1). La pecora di riserva è prevista per essere utilizzata se si verifica un decesso a causa dell'anestesia o di un'altra complicazione non correlata all'intervento chirurgico. Nella fase 2, 10 pecore sono assegnate casualmente al gruppo disco I (n=3), gruppo disco II (n=3), gruppo disco III (n=3) e gruppo di riserva (n=1) (Figura 1).
Fase di Intervento
Protocollo di Anestesia
Il digiuno e la restrizione di acqua sono richiesti 24 ore prima dell'intervento. La sedazione viene effettuata con diazepam (0,5 mg/kg iv), seguita dall'induzione dell'anestesia con ketamina (5 mg/kg iv). Viene eseguita l'intubazione orale e l'anestesia viene mantenuta con isoflurano (1,5% a 2%). Per garantire l'analgesia dell'animale, viene somministrato meloxicam (0,5 mg/kg iv, bid) il giorno dell'intervento e per 4 giorni postoperatori. La profilassi antibiotica con amoxicillina e acido clavulanico viene utilizzata per 5 giorni.
Protocollo di Intervento Chirurgico per le Fasi 1 e 2
Fase 1
Discectomia bilaterale (n=3): sotto anestesia generale, il team chirurgico esegue un'incisione cutanea preauricolare e una dissezione blunt dei tessuti molli che coprono l'articolazione. L'area articolare viene esposta e la capsula articolare viene incisa. Il disco e i suoi attacchi vengono identificati. Gli attacchi mediali, anteriori, posteriori e laterali del disco vengono staccati e viene eseguita la discectomia. La ferita viene chiusa in strati.
Discopexia bilaterale (n=3): sotto anestesia generale, il team chirurgico esegue un'incisione cutanea preauricolare e una dissezione blunt dei tessuti molli che coprono l'articolazione. L'area articolare viene scoperta e la capsula articolare viene incisa. Il disco e i suoi attacchi vengono identificati. Gli attacchi laterali e posteriori del disco vengono staccati e suturati con poli- p-diossanone (PDS) 3/0. La ferita viene chiusa a strati.
Chirurgia fittizia (n=3): sotto anestesia generale, il team chirurgico eseguirà un'incisione cutanea preauricolare e una dissezione blunt dei tessuti molli che coprono l'articolazione. La capsula non viene incisa. La ferita viene chiusa a strati.
Fase 2
Disco I (n=3): sotto anestesia generale, il team chirurgico esegue un'incisione cutanea preauricolare e una dissezione blunt dei tessuti molli che coprono l'articolazione. L'area articolare viene scoperta e la capsula articolare viene incisa. Il disco e i suoi attacchi vengono identificati. Gli attacchi mediali, anteriori, posteriori e laterali del disco vengono staccati e viene eseguita una discectomia. Il disco I viene introdotto nello spazio articolare e suturato negli attacchi laterali. La ferita viene chiusa a strati. Il disco I sarà un biomateriale alternativo e per motivi intellettuali non può essere rivelato in questo documento.
Disco II (n=3): sotto anestesia generale, il team chirurgico esegue un'incisione cutanea preauricolare e una dissezione blunt dei tessuti molli che coprono l'articolazione. L'area articolare viene scoperta e la capsula articolare viene incisa. Il disco e i suoi attacchi vengono identificati. Gli attacchi mediali, anteriori, posteriori e laterali del disco vengono staccati e viene eseguita la discectomia. Il disco II viene introdotto nello spazio articolare e suturato negli attacchi laterali. La ferita viene chiusa a strati. Il disco II sarà un'impalcatura porosa in poli(glicerolo sebacato) (PGS) rinforzata con poli(caprolattone) (PCL).
Disco III (n=3): sotto anestesia generale, il team chirurgico esegue un'incisione cutanea preauricolare e una dissezione blunt dei tessuti molli che coprono l'articolazione. L'area articolare viene scoperta e la capsula articolare viene incisa. Il disco e i suoi attacchi vengono identificati. Gli attacchi mediali, anteriori, posteriori e laterali del disco vengono staccati e viene eseguita la discectomia. Il disco III viene introdotto nello spazio articolare e suturato nell'attacco laterale. La ferita viene chiusa a strati. Il disco III sarà un'impalcatura porosa in PGS preparata mediante un metodo di fusione salina modificato. In breve, particelle di sale macinate (150 mg) con una dimensione compresa tra 25 e 32 µm verranno posizionate in uno stampo stampato in 3D. Lo stampo verrà trasferito in un'incubatrice a 37°C e 90% di umidità relativa per 1 ora. I modelli fusi di particelle di sale si asciugheranno in un forno a vuoto a 90°C e 100 millitorr (mTorr) durante la notte, rimuovendo con attenzione la torta di sale dallo stampo prima di ulteriori lavorazioni. PGS fresco disciolto in tetrahydrofuran (THF; 20 wt%, 380 µL, sale:PGS=2:1) verrà aggiunto alla torta di sale, e il THF verrà lasciato evaporare completamente in una cappa per 30 minuti. La torta di sale verrà trasferita in un forno a vuoto e curata a 150°C e 100 mTorr per 24 ore. I modelli di sale impregnati di PGS risultanti vengono immersi in acqua deionizzata per 4 ore, e poi sostituiti con acqua per 4 ore, con scambio d'acqua ogni 4 ore durante le prime 12 ore. Dopo il bagno d'acqua di 12 ore, le impalcature vengono trasferite in acqua deionizzata per altre 24 ore con scambio d'acqua ogni 8 ore. Le impalcature risultanti vengono congelate a –80°C e poi viene applicato il processo di liofilizzazione.
Dieci giorni per il recupero sono previsti per la cura delle ferite e la medicazione postoperatoria (vedi Figura 2).
Misure di Risultato
L'esito primario è la valutazione microscopica dei cambiamenti distruttivi nell'ATM utilizzando un sistema di punteggio Mankin modificato. Gli esiti secondari sono la valutazione per immagini dei cambiamenti distruttivi nell'ATM, il tempo masticatorio assoluto, il tempo di ruminazione per ciclo, la cinetica della ruminazione, l'area di ruminazione e il peso corporeo delle pecore. I parametri di esito primari e secondari sono descritti in maggiore dettaglio in Figura 3.
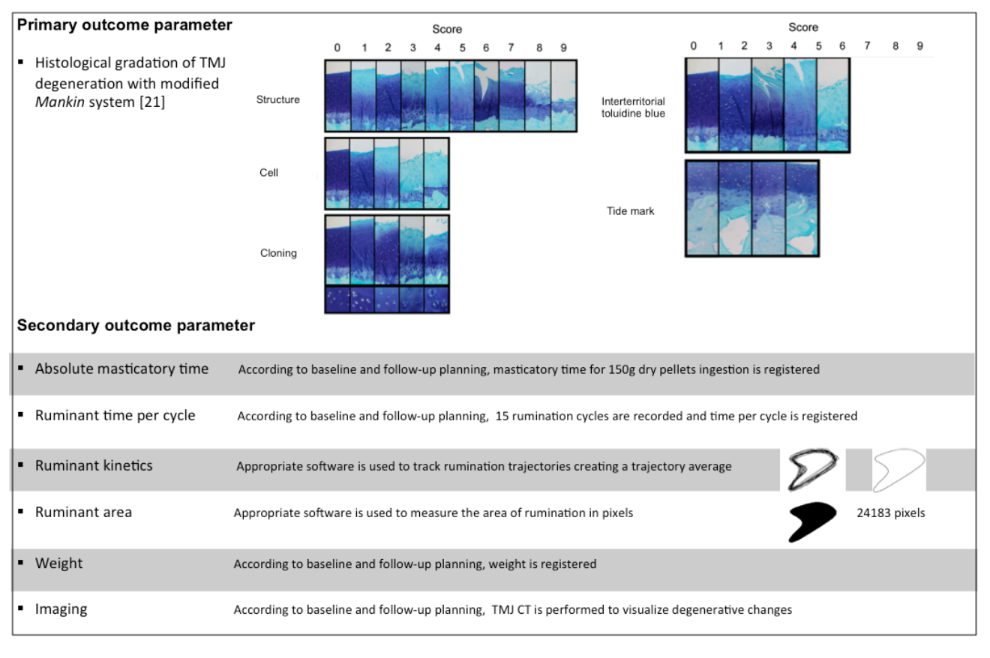
Risultato Primario
L'obiettivo è valutare la gradazione istologica dei cambiamenti distruttivi dell'ATM. Il punto temporale è di 6 mesi dopo l'intervento chirurgico.
Sei mesi dopo l'intervento, l'ATM viene rimossa utilizzando una sega ossea oscillante da necroscopia secondo i seguenti riferimenti anatomici: craniale (aspetto craniale del processo coronoide nella regione di unione del processo zigomatico), caudale (esterno al meato acustico), dorsale (il riferimento è stabilito rispetto all'osso temporale squamoso) e ventrale (il riferimento è fissato 2 cm sotto il meato acustico nella zona dell'angolo stilohioideo). Le articolazioni vengono fissate in formalina tamponata al 10% per 24 ore e conservate in etanolo al 70%. La decalcificazione si ottiene mediante immersione in acido formico al 10% in formalina al 5% per un massimo di 20 giorni, dopo di che le articolazioni vengono tagliate sagittalmente attraverso l'intero condilo. Dopo la decalcificazione, le articolazioni dell'ATM vengono immerse in tre miscele di salicilato di metile/paraffina in diverse gradazioni e tagliate sagittalmente dalla parte laterale verso la parte centrale dell'ATM. Le sezioni istologiche vengono inviate all'Istituto di Ricerca sulle Ossa e le Articolazioni di Sydney per la valutazione istologica utilizzando un sistema di punteggio Mankin modificato. Questa valutazione viene eseguita e classificata in modo indipendente da due istologi che saranno accecati all'intervento. Un terzo istologo agirà come arbitro in caso di disparità.
Risultati Secondari
Le caratteristiche valutate sono analisi di imaging, tempo masticatorio assoluto, tempo di ruminazione per ciclo, cinematica della ruminazione, area di ruminazione e peso delle pecore (vedi Appendici Multimediali 1 e 2). Il punto temporale è ogni mese dopo l'intervento chirurgico per un totale di 6 mesi.
Per misurare i risultati secondari, è stata costruita una gabbia specifica (vedi Figura 4) con una finestra frontale e un mangiatoia.
Analisi di imaging: la TC preoperatoria viene eseguita su tutte le pecore. Dopo il sacrificio dell'animale, i blocchi dell'ATM vengono scansionati tramite TC e la valutazione dell'imaging viene eseguita utilizzando i criteri e il punteggio descritti in Tabella 1.
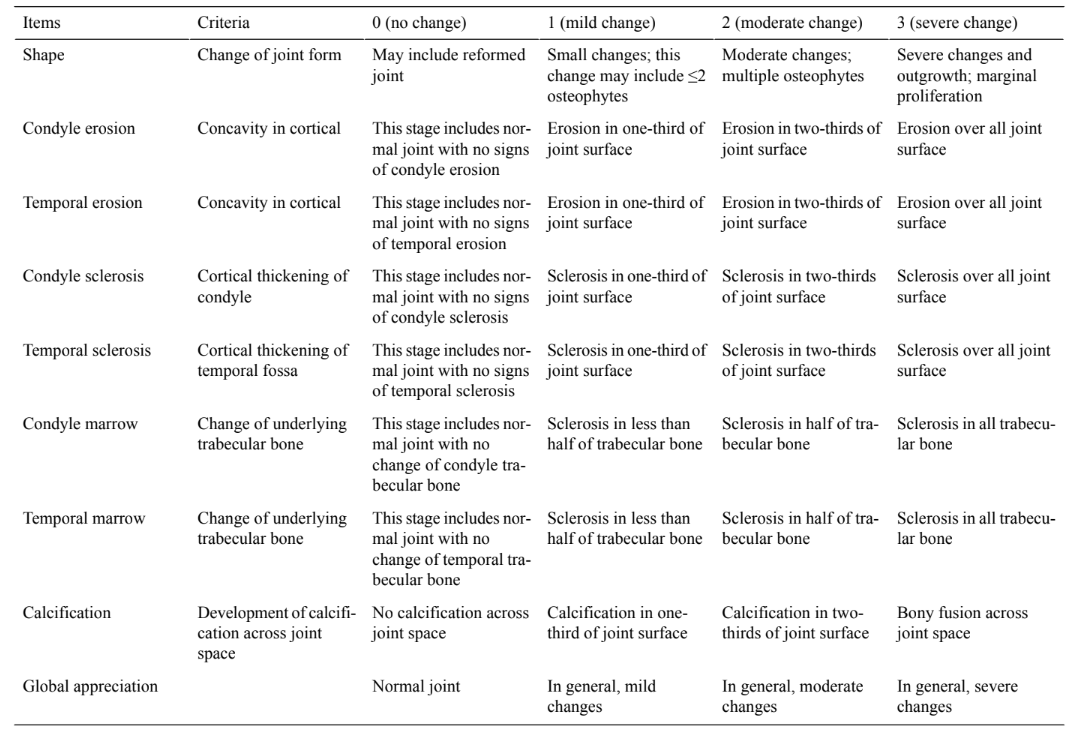

Questa valutazione viene eseguita e classificata in modo indipendente da due radiologi esperti che saranno accecati all'intervento. Un terzo radiologo agirà come arbitro in caso di disparità.
Tempo masticatorio assoluto: rispettando il diagramma di flusso (Figura 2), alle 9:00 gli animali vengono collocati in gabbie individuali. Una dose di 150 grammi di pellet secchi (Rico Gado A3) viene introdotta nel mangiatoia e il tempo fino a quando mangiano tutti i pellet viene misurato con un cronometro (vedi Appendice Multimediale 1).
Tempo di ruminazione per ciclo: rispettando il programma (Figura 2), registriamo 15 cicli ruminatori circa 4 ore dopo l'alimentazione di 150 grammi. Utilizziamo una videocamera Canon 7D e immagini con 25 fotogrammi al secondo. Poi, il numero di fotogrammi per ciclo viene diviso per 25 per ottenere il tempo in secondi per ciclo (vedi Appendice Multimediale 2).
Cinetica dei ruminanti: utilizziamo il software Foundry Nuke (tracciamento 2D) per eseguire il tracciamento ruminatorio e ottenere la media del ciclo ruminatorio. Con il software After Effects , convertiamo il tracciamento 2-D in una forma geometrica (vedi AppendiceMultimediale 2).
Area ruminante: determiniamo la media di 15 cicli e creiamo una forma geometrica. Utilizzando il software Image J, effettuiamo una misura quantitativa in pixel della media dell'area ruminante.
Peso: secondo il programma, dopo aver mangiato 150 grammi di pellet secchi, le pecore vengono pesate (vedi AppendiceMultimediale 1).
Tutte le valutazioni sono effettuate da ricercatori che non sono a conoscenza dell'intervento chirurgico.
Analisi Statistiche
Tutte le analisi statistiche saranno eseguite utilizzando la versione 22 di SPSS (IBM Corp, Armonk, NY, USA). Sarà eseguita un'analisi trasversale per confrontare le variabili di esito nei tre livelli della variabile indipendente prima e dopo l'assegnazione del gruppo di trattamento randomizzato. Nelle analisi trasversali, sarà eseguita un'analisi della varianza unidirezionale (ANOVA), dopo aver testato tutte le assunzioni. Per l'analisi longitudinale, sarà eseguita un'ANOVA unidirezionale con misure ripetute considerando come effetti intra-soggetti le osservazioni dopo l'intervento chirurgico (mesi 1-6). Il test di Fisher per la minima differenza significativa sarà eseguito come test post hoc per verificare le differenze significative tra i diversi trattamenti.
Segnalazione di Eventi Avversi
Gli eventi avversi correlati allo studio saranno presi in considerazione, inclusi (1) eventi anestetici: morte idiopatica, pneumotorace, altre complicazioni correlate all'anestesia; (2) tecnica chirurgica: emorragia massiva, frattura condilare, altre complicazioni correlate alla tecnica chirurgica; e (3) eventi postoperatori: infezione dell'ATM, deiscenza della sutura, diminuzione dell'appetito, paresi facciale, diminuzione della ruminazione, diminuzione del peso.
Discussione
Questo studio indaga gli effetti e gli effetti avversi di (1) discectomia bilaterale, (2) discopexia bilaterale e (3) impianti di disco bioingegnerizzati. Sebbene questo studio preclinico servirà principalmente come studio pilota, ci aspettiamo di ottenere una migliore comprensione dei cambiamenti morfologici e istologici nell'ATM e delle implicazioni nella cinetica masticatoria.
Finora, i risultati sulla discectomia sono contrastanti. Studi preclinici precedenti in questo campo hanno utilizzato il lato controlaterale non operato come controllo e diversi modelli animali che vanno dai topi a un modello canino. Utilizzare il lato controlaterale come controllo può essere inappropriato considerando l'influenza del sovraccarico controlaterale. Teoricamente, ci aspettiamo di ridurre questo bias utilizzando un approccio bilaterale. La variabilità animale nei diversi studi è un avvertimento sull'importanza di utilizzare lo stesso modello animale in ulteriori studi riguardanti le indagini sugli impianti ATM. Pertanto, il nostro gruppo ha condotto uno studio precedente considerando le pecore Merino nere come un promettente modello animale per studi riguardanti l'indagine sugli impianti di disco ATM, la protesi ATM e il modello di osteoartrite ATM. Per aumentare la qualità di TEMPOJIMS, gli autori utilizzeranno un gruppo di controllo di chirurgia simulata.
Ci aspettiamo di ottenere informazioni preziose relative al gruppo di discopexia di fase 1 riguardo se l'approccio chirurgico promuove danni intra-articolari. Questo può migliorare le conclusioni future sull'attribuzione di possibili danni all'intervento stesso invece che all'impianto ATM. Questa domanda è importante considerando che sarà necessario un approccio chirurgico per posizionare impianti ATM nella fase 2. Ancora una volta, utilizzare un intervento bilaterale potrebbe ridurre un possibile bias.
La maggior parte degli studi preclinici si è concentrata su valutazioni morfologiche/storiche macroscopiche e non erano progettati per caratterizzare il fondamentale movimento articolare alterato (cinematica) o le conseguenze funzionali. In questo studio, includiamo risultati secondari pilota per valutare i cambiamenti nella cinetica dei ruminanti. Ci aspettiamo di correlare i risultati primari con quelli secondari per capire se possono essere utilizzati in futuri studi ATM. Potrebbe essere interessante comprendere diversi aspetti:
- Ci sono differenze riguardo al tempo masticatorio nei gruppi di disco rispetto a discectomia e discopessia?
- C'è una correlazione tra i risultati istologici, di imaging e cinetici?
- L'area ruminante e la geometria cambiano quando si eseguono diverse interventi?
- C'è una differenza riguardo alla cinetica ruminante nei gruppi di disco rispetto a discectomia e discopessia?
- Gli impianti ATM accelerano l'osteoartrite?
Per quanto riguarda la fase 2, la scelta del biomateriale è critica. L'impianto ATM sarà esposto a un ambiente meccanico e stressante con un apporto di sangue limitato che può limitare la migrazione cellulare e la rigenerazione in situ. Testare tre diversi dischi di bioingegneria in vivo e correlare il comportamento in vitro con quello in vivo può migliorare seriamente le strategie di bioingegneria per ottenere un impianto di disco ATM sicuro ed efficace per gli esseri umani.
Il principale punto di forza di questo studio è il modello animale proposto; i risultati convenzionali e pilota descritti; il disegno dello studio con un gruppo di controllo randomizzato, in cieco e con placebo; e l'uso di procedure chirurgiche bilaterali. Le potenziali limitazioni dello studio includono la dimensione relativamente piccola del campione. Se questo studio conferma la fattibilità del protocollo proposto e l'efficacia iniziale degli impianti del disco ATM pianificati, sarebbe giustificato un trial preclinico più ampio per determinare ulteriormente l'efficacia di questi dischi e promuovere la traduzione delle evidenze animali nella pratica clinica negli esseri umani.
Autori: David Faustino Ângelo, Florencio Gil Monje, Raúl González-García, Christopher B Little, Lisete Mónico, Mário Pinho, Fábio Abade Santos, Belmira Carrapiço, Sandra Cavaco Gonçalves, Pedro Morouço, Nuno Alves, Carla Moura, Yadong Wang, Eric Jeffries, Jin Gao, Rita Sousa, Lia Lucas Neto, Daniel Caldeira, Francisco Salvado
Riferimenti
- Bae Y, Park Y. L'effetto degli esercizi di rilassamento per i muscoli masticatori sulla disfunzione dell'articolazione temporomandibolare (TMD). J Phys Ther Sci 2013;25(5):583-586. [doi: 10.1589/jpts.25.583]
- Allen K, Athanasiou K. Ingegneria dei tessuti del disco TMJ: una revisione. Tissue Eng 2006;12(5):1183-1196. [doi: 10.1089/ten.2006.12.1183]
- Tanaka E, Sasaki A, Tahmina K, Yamaguchi K, Mori Y, Tanne K. Proprietà meccaniche del disco articolare umano e la sua influenza sul carico TMJ studiato con il metodo degli elementi finiti. J Oral Rehabil 2001 Mar;28(3):273-279. [Medline: 11394374]
- Martins-Júnior RL, Palma Antônio JC, Marquardt EJ, Gondin TM, Kerber FD. Disturbi temporomandibolari: un rapporto di 124 pazienti. J Contemp Dent Pract 2010 Oct 14;11(5):71-78. [Medline: 20978727]
- Navrátil L, Navratil V, Hajkova S, Hlinakova P, Dostalova T, Vranová J. Trattamento completo dei disturbi dell'articolazione temporomandibolare. Cranio 2014 Jan;32(1):24-30. [doi: 10.1179/0886963413Z.0000000002] [Medline: 24660643]
- Mehra P, Wolford LM. L'ancora mini Mitek per il riposizionamento del disco TMJ: tecnica chirurgica e risultati. Int J Oral Maxillofac Surg 2001 Dec;30(6):497-503. [doi: 10.1054/ijom.2001.0163] [Medline: 11829231]
- Al-Baghdadi M, Durham J, Araujo-Soares V, Robalino S, Errington L, Steele J. Gestione dello spostamento del disco TMJ senza riduzione: una revisione sistematica. J Dent Res 2014 Jul;93(7 Suppl):37S-51S [FREE Full text] [doi: 10.1177/0022034514528333] [Medline: 24659775]
- Estabrooks L, Fairbanks C, Collett R, Miller L. Una valutazione retrospettiva di 301 impianti TMJ Proplast-Teflon. Oral Surg Oral Med Oral Pathol 1990 Sep;70(3):381-386. [Medline: 2216373]
- Henry CH, Wolford LM. Risultati del trattamento per la ricostruzione dell'articolazione temporomandibolare dopo il fallimento dell'impianto Proplast-Teflon. J Oral Maxillofac Surg 1993 Apr;51(4):352-358; discussione 359. [Medline: 8450350]
- Mercuri LG, Giobbie-Hurder A. Risultati a lungo termine dopo la ricostruzione totale alloplastica dell'articolazione temporomandibolare a seguito dell'esposizione a materiali falliti. J Oral Maxillofac Surg 2004 Sep;62(9):1088-1096. [Medline: 15346359]
- Morouço P, Ângelo D, Francisco L, Moura C, Alves N. Ingegneria dei tessuti per la riparazione e rigenerazione del disco dell'articolazione temporomandibolare: una prospettiva metodologica. Adv Cell Mol Otolaryngol 2017 Jan 17;4(1):33709. [doi: 10.3402/acmo.v4.33709]
- Lypka M, Yamashita DR. Reazione esuberante delle cellule giganti del corpo estraneo a un impianto temporomandibolare in teflon/proplast: rapporto di un caso. J Oral Maxillofac Surg 2007 Sep;65(9):1680-1684. [doi: 10.1016/j.joms.2006.09.030] [Medline: 17719383]
- Spagnoli D, Kent JN. Valutazione multicentrica dell'impianto del disco Proplast-Teflon dell'articolazione temporomandibolare. Oral Surg Oral Med Oral Pathol 1992 Oct;74(4):411-421. [Medline: 1408011]
- Fricton JR, Look JO, Schiffman E, Swift J. Studio a lungo termine della chirurgia dell'articolazione temporomandibolare con impianti alloplastici confrontata con chirurgia non impiantare e riabilitazione non chirurgica per lo spostamento doloroso del disco dell'articolazione temporomandibolare. J Oral Maxillofac Surg 2002 Dec;60(12):1400-1411; discussione 1411. [doi: 10.1053/joms.2002.36091] [Medline: 12465000]
- Kulber DA, Davos I, Aronowitz JA. Grave reazione cutanea delle cellule giganti del corpo estraneo dopo la ricostruzione dell'articolazione temporomandibolare con Proplast-Teflon. J Oral Maxillofac Surg 1995 Jun;53(6):719-722; discussione 722. [Medline: 7776062]
- Chuong R, Piper MA. Perdita di liquido cerebrospinale associata alla rimozione dell'impianto proplast dall'articolazione temporomandibolare. Oral Surg Oral Med Oral Pathol 1992 Oct;74(4):422-425. [Medline: 1408012]
- Berarducci JP, Thompson DA, Scheffer RB. Perforazione nella fossa cranica media come conseguenza dell'uso di un impianto Proplast-Teflon per la ricostruzione dell'articolazione temporomandibolare. J Oral Maxillofac Surg 1990 May;48(5):496-498. [Medline: 2329399]
- [Nessun autore elencato]. Raccomandazioni per la gestione dei pazienti con impianti dell'articolazione temporomandibolare. Workshop di chirurgia degli impianti dell'articolazione temporomandibolare. J Oral Maxillofac Surg 1993 Oct;51(10):1164-1172. [Medline: 8410459]
- Herring S. Anatomia del TMJ e modelli animali. J Musculoskelet Neuronal Interact 2003 Dec;3(4):391-394; discussione 406 [FREE Full text] [Medline: 15758330]
- Angelo D, Morouço P, Alves N, Viana T, Santos F, González R. Scegliere le pecore (Ovis aries) come modello animale per la ricerca sull'articolazione temporomandibolare: caratterizzazione morfologica, istologica e biomeccanica del disco articolare. Morphologie 2016 Jul:223-233 [FREE Full text] [doi: 10.1016/j.morpho.2016.06.002] [Medline: 27450042]
- Leiggener CS, Erni S, Gallo LM. Nuovo approccio allo studio della cinematica della mandibola in una ricostruzione TMJ alloplastica. Int J Oral Maxillofac Surg 2012 Sep;41(9):1041-1045. [doi: 10.1016/j.ijom.2012.06.014] [Medline: 22819692]
- Little CB, Smith MM, Cake MA, Read RA, Murphy MJ, Barry FP. L'iniziativa OARSI di istopatologia - raccomandazioni per le valutazioni istologiche dell'osteoartrite in pecore e capre. Osteoarthritis Cartilage 2010 Oct;18 Suppl 3:S80-S92 [FREE Full text] [doi: 10.1016/j.joca.2010.04.016] [Medline: 20864026]
- Cake MA, Appleyard RC, Read RA, Smith MM, Murrell GA, Ghosh P. L'ovariectomia altera le proprietà strutturali e biomeccaniche della cartilagine articolare femoro-tibiale ovina e aumenta l'iNOS cartilagineo. Osteoarthritis Cartilage 2005 Dec;13(12):1066-1075 [FREE Full text] [doi: 10.1016/j.joca.2005.07.001] [Medline: 16154775]
- Cohen W, Servais J, Polur I, Li Y, Xu L. Degenerazione della cartilagine articolare nell'articolazione temporomandibolare non chirurgica controlaterale in topi con discectomia parziale unilaterale. J Oral Pathol Med 2014 Feb;43(2):162-165. [doi: 10.1111/jop.12113] [Medline: 24044578]
- Ahtiainen K, Mauno J, Ellä V, Hagström J, Lindqvist C, Miettinen S, et al. Cellule staminali adipose autologhe e dischi di polilattide nella sostituzione del disco dell'articolazione temporomandibolare del coniglio. J R Soc Interface 2013 Aug 06;10(85):20130287 [FREE Full text] [doi: 10.1098/rsif.2013.0287] [Medline: 23720535]
- Brown B, Chung W, Almarza A, Pavlick M, Reppas S, Ochs M. Approccio induttivo, basato su scaffold, alla medicina rigenerativa per la ricostruzione del disco dell'articolazione temporomandibolare. J Oral Maxillofac Surg 2012 Nov;70(11):2656-2668. [doi: 10.1016/j.joms.2011.12.030]
- Xu L, Polur I, Lim C, Servais J, Dobeck J, Li Y, et al. Osteoartrite a esordio precoce dell'articolazione temporomandibolare del topo indotta da discectomia parziale. Osteoarthritis Cartilage 2009 Jul;17(7):917-922. [doi: 10.1016/j.joca.2009.01.002] [Medline: 19230720]
- Lai WT, Tsai Y, Su S, Su C, Stockstill JW, Burch JG. Analisi istologica della rigenerazione dei dischi dell'articolazione temporomandibolare nei conigli utilizzando un template di collagene ricostituito. Int J Oral Maxillofac Surg 2005 May;34(3):311-320. [doi: 10.1016/j.ijom.2004.05.003] [Medline: 15741041]
- Sato S, Goto S, Koeda S, Motegi K. Cambiamenti della rete di fibre elastiche dell'articolazione temporomandibolare del coniglio dopo discectomia. J Oral Rehabil 2002 Sep;29(9):847-852. [Medline: 12366539]
- Sato S, Goto S, Motegi K. Cambiamenti dell'orientamento delle fibre di collagene dell'articolazione temporomandibolare del coniglio dopo discectomia. J Craniomaxillofac Surg 2002 Jun;30(3):178-183. [Medline: 12220997]
- Bjørnland T, Haanaes HR. Discectomia dell'articolazione temporomandibolare: uno studio sperimentale nei primati. J Craniomaxillofac Surg 1999 Apr;27(2):113-116. [Medline: 10342149]
- Ogi N, Kurita K, Ishimaru JI, Goss AN. Effetto a breve termine dell'uso di un allograft di disco congelato per la riparazione dell'articolazione temporomandibolare osteoartritica della pecora: un rapporto preliminare. J Oral Maxillofac Surg1999 Feb;57(2):139-144; discussione 144. [Medline: 9973121]
- Hinton R, Stinson J. Effetto della dieta postoperatoria sulla risposta della cartilagine condilare alla discectomia. J Oral Maxillofac Surg 1997 Nov;55(11):1259-1264. [Medline: 9371117]
