Confronto in vivo della biocompatibilità di due sigillanti per canali radicolari impiantati nel tessuto connettivo sottocutaneo dei ratti
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Obiettivo. Valutare la biocompatibilità sottocutanea di 2 sigillanti per canali radicolari.
Progetto dello studio. È stata utilizzata la tecnica dell'impianto sottocutaneo raccomandata dalla Fédération Dentaire International (FDI) per testare i sigillanti per canali radicolari Endométhasone e EndoREZ. Questi materiali sono stati collocati in tubi di Teflon, con un diametro di 1 mm e una lunghezza di 10 mm, e impiantati in 2 tasche create nella parte posteriore di 40 Calomys callosus roditori, 20 per ciascun materiale. Sono state raccolte biopsie tissutali e esaminate istologicamente 15, 30, 60 e 90 giorni dopo la procedura di impianto. Il livello complessivo della risposta infiammatoria tissutale è stato classificato come assente, lieve, moderato o severo sull'interfaccia sigillante–tessuto connettivo alle estremità aperte dei tubi. La risposta del tessuto connettivo lungo la parete laterale esterna di ciascun tubo ha servito come controllo negativo.
Risultati. La reazione tissutale all'Endométhasone è diminuita nel tempo. Il sigillante EndoREZ è risultato altamente tossico durante tutti i periodi sperimentali.
Conclusione. Il sigillante per canali radicolari Endométhasone ha mostrato biocompatibilità nei periodi analizzati, mentre EndoREZ non ha mostrato comportamento biocompatibile e ha causato una reazione ipersensibile tardiva. (Chir. Orale Chir. Med. Orale Patol. Orale Radiol. Endod 2007;103:e88-e94)
Il successo della terapia endodontica dipende da diagnosi corrette, pulizia efficace, eliminazione dell'infezione e adeguata otturazione dei canali radicolari. La reazione del tessuto periapicale dopo il trattamento del canale radicolare può essere influenzata da vari fattori a seconda della natura chimica del sigillante endodontico. Attualmente in uso nella pratica clinica ci sono sigillanti endodontici a base di resina, ossido di zinco-eugenolo, ionomero di vetro, silicio e idrossido di calcio. I sigillanti a base di resina stanno guadagnando sempre più popolarità, ma studi hanno dimostrato che alcuni di questi sigillanti presentano tossicità e mutagenicità. Nonostante la grande varietà di sigillanti disponibili, un sigillante per canali radicolari che possieda tutte le proprietà fisiche e biologiche desiderabili deve ancora essere trovato. La biocompatibilità è una delle proprietà più importanti dei materiali di riempimento radicolare8 poiché il rilascio di determinate sostanze da parte dei sigillanti può generare diverse reazioni nei tessuti periapicali. Le reazioni tissutali causate dai materiali endodontici vengono normalmente investigate attraverso studi istologici dopo l'impianto del materiale nel tessuto animale. Endométhasone (Spécialities Septodont, Saint-Maur-des-Fossés, Francia) è un sigillante a base di ossido di zinco-eugenolo che è stato precedentemente valutato in vari studi riguardanti le sue proprietà biologiche. Recentemente, è stato introdotto un nuovo sigillante endodontico a base di metacrilato, EndoREZ (Ultradent Products Inc., South Jordan, UT, USA), le cui proprietà biologiche sono state poco investigate.
Lo scopo di questo studio era valutare la reazione del tessuto connettivo sottocutaneo agli sigillanti per canali radicolari EndoREZ ed Endométhasone seguendo i requisiti raccomandati dalla FDI.
Metodi
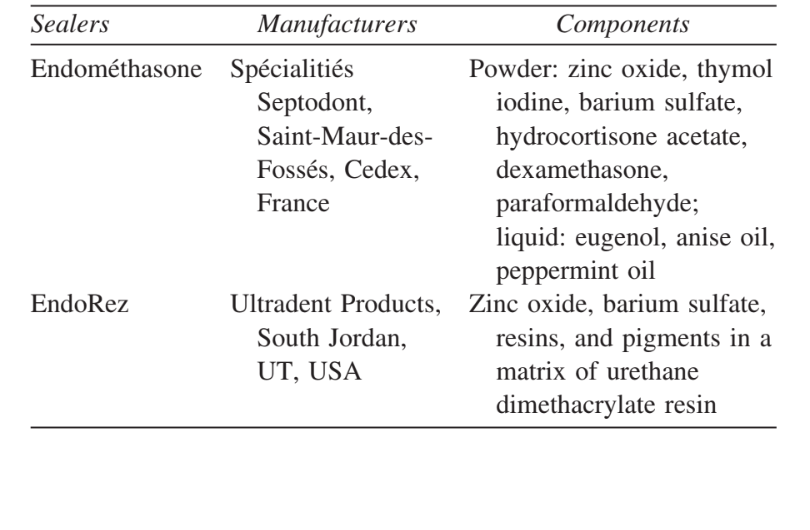
Il protocollo per questo esperimento è stato approvato dal Comitato Etico per la Ricerca dell'Università di Uberlândia, e l'esperimento è stato condotto in conformità con la Politica del Servizio Sanitario Pubblico degli Stati Uniti sulla Cura e Uso Umano degli Animali da Laboratorio. Sono stati utilizzati quaranta roditori maschi Calomys callosus (Rodentia, Cricetidae), con un peso compreso tra 150 e 200 g. I campioni sono stati divisi in 2 gruppi di 20 animali ciascuno per gli sigillanti Endométhasone ed EndoREZ. La Tabella I mostra i materiali, i produttori e i componenti principali.
Tutti i materiali sono stati preparati nel modo consigliato dai produttori per il loro uso clinico e caricati in portatori di Teflon autoclavati (politetrafluoroetilene, Du-Pont, Habia, Knivsta, Svezia), lunghi 10 mm con un singolo lume e un diametro interno di 1 mm, assicurando che l'aria non fosse intrappolata.
Gli animali sono stati anestetizzati intraperitonealmente con 0,2 mL di ketamina contenente acepromazina in proporzione 1:1. La pelle dorsale è stata rasata, disinfettata con tintura di iodio al 5% e sono state effettuate piccole incisioni, di circa 15 mm di lunghezza, su entrambi i lati del dorso. Sono state create due tasche separate mediante dissezione blunt per impiantare i tubi nel tessuto sottocutaneo a una profondità di ~15 mm. I tubi contenenti sigillanti freschi sono stati quindi posizionati nelle tasche destra e sinistra preparate in ciascun animale. Si è prestata attenzione a evitare la fuoriuscita dei materiali nel tessuto. Dopo l'impianto, le ferite sono state suturate.
Gli animali sono stati uccisi in gruppi di 5 ciascuno dopo 15, 30, 60 e 90 giorni mediante asfissia da anidride carbonica, assicurando il minimo disagio e stress. I tubi sono stati escissi insieme alla pelle e al tessuto connettivo circostante. I campioni sono stati immersi in formalina al 10% in soluzione tampone fosfato 0,1 mol/L per 24 ore, disidratati in soluzioni di etanolo gradate a temperatura ambiente e incorporati in glicole metacrilato (Historesin; Leica Microsystems, Nussloch GmbH, Germania). Per il taglio in sezione trasversale, i blocchi sono stati orientati parallelamente all'asse lungo del tubo. Le sezioni sono state tagliate a uno spessore di 3 µm e colorate con blu di toluidina al 1%. Le sezioni istologiche sono state analizzate a diverse ingrandimenti sotto un microscopio ottico, notando le reazioni tissutali sull'interfaccia sigillante–tessuto connettivo agli estremi aperti dei tubi. La risposta del tessuto connettivo lungo la parete laterale esterna dei tubi ha servito come controllo negativo.
L'interfaccia all'apertura della coppa tra il materiale e l'osso è stata esaminata e valutata per l'intensità dell'infiammazione. La valutazione dei criteri della Fédération Dentaire International (FDI) è esclusivamente qualitativa e non è stato utilizzato alcun indice di punteggio. Pertanto, il livello complessivo della reazione tissutale è stato classificato come assente, lieve, moderato o severo, a seconda della presenza o assenza di leucociti neutrofili, macrofagi, linfociti, cellule plasmatiche, cellule giganti di corpo estraneo, materiale disperso, capsula, osso sano neoformato, tessuto necrotico e riassorbimento. Il livello complessivo della risposta tissutale infiammatoria è stato classificato come segue: 1) assente/lieve: spessore della zona di reazione simile o solo leggermente più ampio dello spessore lungo il tubo laterale, con nessuna o poche cellule infiammatorie; 2) moderato: zona di reazione aumentata in cui sono presenti macrofagi, cellule plasmatiche, o entrambi; e 3) severo: zona di reazione aumentata in cui sono presenti macrofagi e cellule plasmatiche e occasionali focolai di granulociti neutrofili, linfociti, o entrambi.
Le interpretazioni dei risultati si basavano sui seguenti criteri FDI: nessuna o leggera reazione sia a 2 che a 12 settimane è accettabile; nessuna o leggera reazione a 2 settimane che aumenta a reazione moderata o severa a 12 settimane non è accettabile; reazione moderata a 2 e 12 settimane non è accettabile; reazione moderata a 2 settimane che diminuisce a 12 settimane è accettabile; e una reazione severa in qualsiasi periodo è inaccettabile.
Risultati
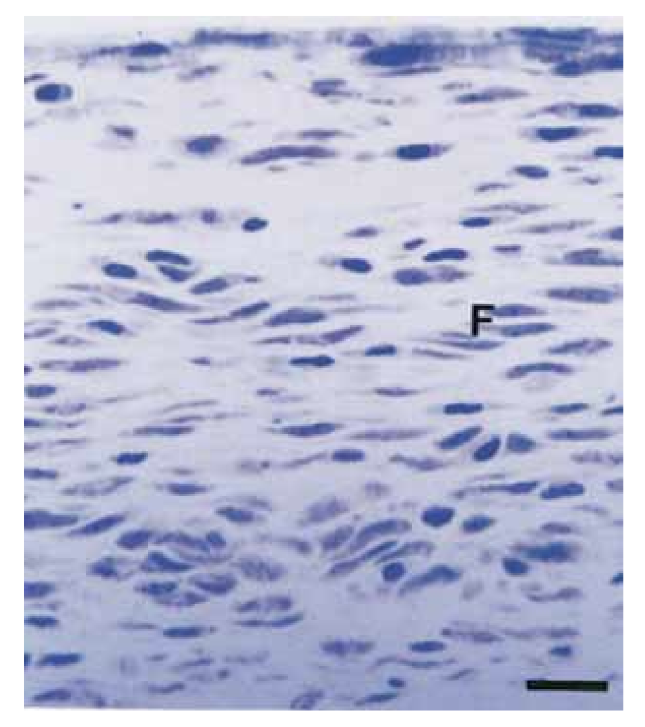
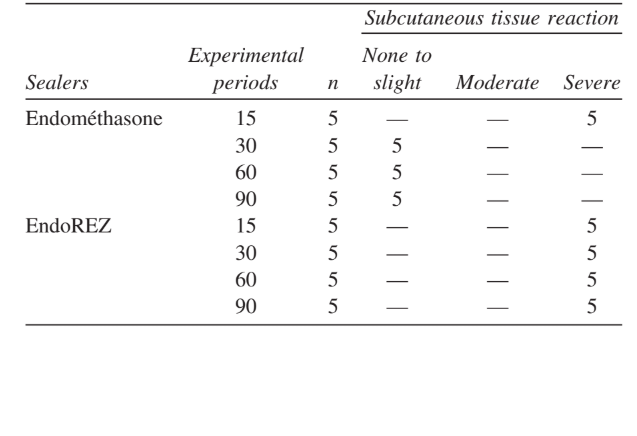
L'intensità della risposta infiammatoria in tutti i periodi sperimentali di entrambi i sigillanti è stata analizzata. La risposta del tessuto connettivo lungo la parete laterale esterna dei tubi in Teflon ha servito come controllo negativo per la tecnica e non ha mostrato reazione infiammatoria in tutti i periodi di sperimentazione (Fig. 1). I numeri dei campioni in ciascuna categoria infiammatoria nei diversi intervalli di tempo per i 2 tipi di sigillanti sono presentati nella Tabella II.
Endométhasone
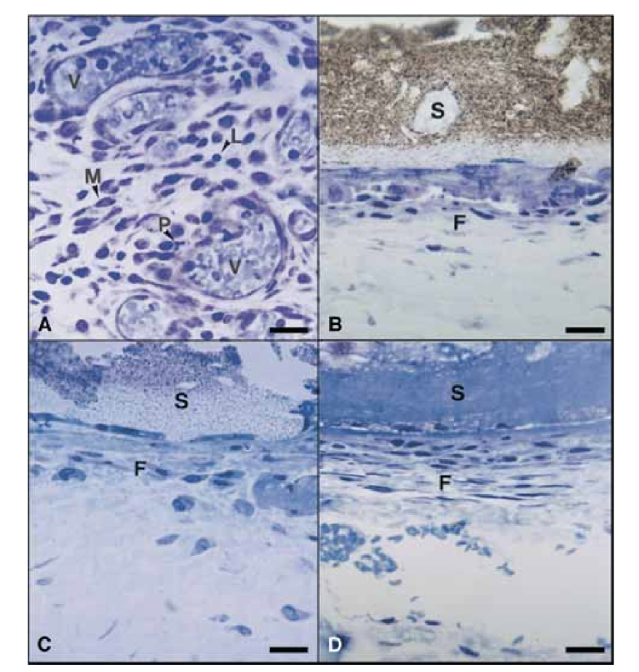
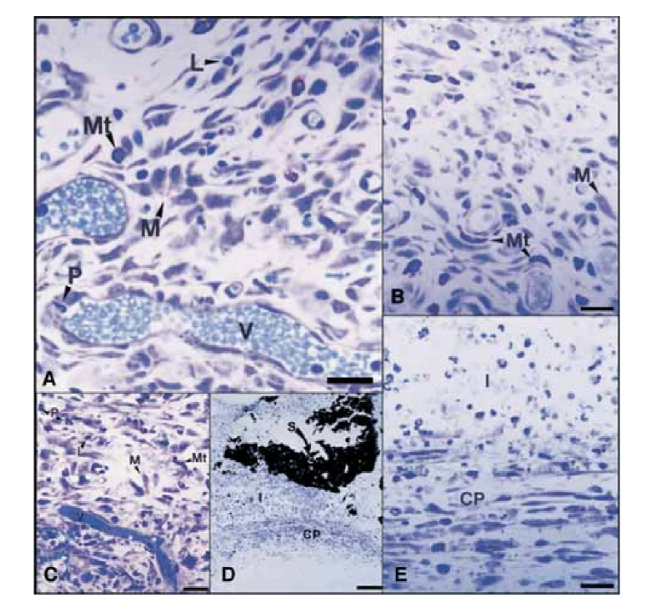
Il 15° giorno, è stata osservata una reazione infiammatoria da moderata a severa. Il tessuto era infiltrato prevalentemente da macrofagi e linfociti. È stata osservata anche la presenza di leucociti polimorfonucleati, iperemia e una matrice extracellulare morfologicamente alterata (Fig. 2, A). Nei giorni 30, 60 e 90, il tessuto connettivo non ha mostrato reazione infiammatoria (Fig. 2, B, C e D).
EndoREZ
Il 15° giorno è stata osservata una reazione infiammatoria da moderata a severa. Il tessuto era infiltrato prevalentemente da macrofagi, pochi leucociti polimorfonucleati e linfociti. Sono state osservate anche iperemia vascolare e una matrice extracellulare ridotta e morfologicamente alterata (Fig. 3, A). Dal 30° giorno, è stata osservata una reazione infiammatoria severa e un infiltrato infiammatorio composto prevalentemente da leucociti polimorfonucleati, linfociti e macrofagi sembrava invadere il lume dei tubi in Teflon. Inoltre, all'interfaccia tra il sigillante e il tessuto connettivo, sono stati osservati vasi sanguigni circondati da mastociti (Fig. 3, B). Al 60° giorno, persisteva ancora una reazione infiammatoria severa con macrofagi, linfociti e leucociti polimorfonucleati. All'apertura dei tubi in Teflon, il sigillante era sostituito da un infiltrato infiammatorio con prevalenza di macrofagi e linfociti. Sono stati osservati vasi sanguigni congesti circondati da mastociti (Fig. 3, C). È stata anche rilevata una proliferazione fibroblastica consistente che circondava il tessuto infiammatorio. Al 90° giorno, è stato osservato un infiltrato infiammatorio severo composto da macrofagi, linfociti, leucociti polimorfonucleati, globuli rossi e cellule morte invaginati nel lume dei tubi in Teflon, sostituendo il sigillante. All'estremità di apertura dei tubi, il tessuto granulomatoso era isolato da un'incapsulazione fibrosa (Fig. 3, D e E).
Discussione
Quando un nuovo materiale viene introdotto sul mercato, o un materiale esistente è proposto per un'applicazione diversa, le sue proprietà devono essere investigate e i risultati confrontati con quelli di altri autori. Negli Stati Uniti, la Food and Drug Administration (FDA) ha la responsabilità di valutare e analizzare gli effetti biologici di tutti i farmaci, materiali e dispositivi utilizzati negli esseri umani, compresi la maggior parte dei prodotti e dispositivi dentali. La FDA prevede anche il riconoscimento degli standard stabiliti da organizzazioni private, come l'ANSI/ADA. La revisione delle prime Pratiche Standard Raccomandate per la Valutazione Biologica dei Materiali Dentali è stata ritardata per incorporare gli elementi essenziali delle raccomandazioni della FDA. Questo nuovo documento non intendeva scoraggiare lo sviluppo industriale di nuovi e migliorati prodotti dentali richiedendo test biologici eccessivi, ma, in quest'era di preoccupazione per i rischi chimici, dovrebbe essere sviluppato un profilo di tossicità per tutti i nuovi e migliorati materiali per ottenere dati rilevanti sulla sicurezza e sull'efficacia. Sebbene nessuna quantità di studio sperimentale possa garantire una sicurezza assoluta per qualsiasi sostanza, le indagini tossicologiche forniscono dati dai quali possono essere fatte proiezioni e previsioni ragionevoli sulle condizioni sotto le quali l'agente può essere utilizzato in sicurezza.
Sebbene molti test, come la citotossicità, l'emolisi, il test di Ame, la trasformazione cellulare di Styles, le impiantazioni sottocutanee e ossee, la sensibilizzazione e l'uso endodontico, siano elencati per vari livelli di test, non sono tutti richiesti per ogni prodotto. Deve essere fatta una valutazione su quali test siano rilevanti. I test iniziali servono a fornire un profilo di tossicità in un sistema biologico, in modo che, su base comparativa, il produttore avrà un'idea generale e una realizzazione di dove si colloca il prodotto. Per la FDA, i dispositivi regolamentati rientrano in 3 classi, tuttavia, la maggior parte dei dispositivi e degli apparecchi dentali non sarebbe soggetta a standardizzazione per l'autorizzazione premarket. In altre parole, a volte anche i test di sicurezza di base non sono richiesti prima che i prodotti possano essere promossi per uso clinico.
La biocompatibilità dei materiali dentali è un requisito importante perché i componenti tossici presenti in questi materiali potrebbero produrre irritazione o addirittura degenerazione dei tessuti circostanti, specialmente quando vengono accidentalmente estrusi nei tessuti periradicolari. L'impianto di tessuto connettivo sottocutaneo negli animali è uno dei metodi più affidabili per valutare la biocompatibilità dei materiali dentali perché le reazioni infiammatorie sono una caratteristica comune a tutti i tessuti connettivi. Il roditore selvatico simile a un topo Calomys callosus è comunemente usato per indagare l'infezione sperimentale e la risposta immunitaria umorale ed è stato utilizzato nello studio presente grazie alla sua riproducibilità come modello stabilito ampiamente accettato nella letteratura.
I campioni sono stati incorporati in metacrilato di glicole grazie ai suoi vantaggi rispetto alla paraffina, come la produzione di minore distorsione, la fornitura di sezioni sottili che offrono una buona definizione cellulare, la possibilità di preparare sezioni senza rimuovere i tubi e la colorazione con buona qualità e pochi artefatti tecnici, favorendo una valutazione più precisa della reazione infiammatoria.
Nello studio attuale, il tessuto connettivo lungo la parete laterale ha servito come controllo negativo e non ha presentato reazioni infiammatorie (Fig. 1), dimostrando la biocompatibilità del Teflon e che la reazione infiammatoria all'apertura del tubo era correlata al materiale studiato.
Le proprietà biologiche dell'Endométhasone, un sigillante per canali radicolari a base di ossido di zinco–eugenolo (ZOE), sono state precedentemente studiate riguardo all'attività antibatterica, alla citotossicità e alla biocompatibilità dei tessuti. L'eugenolo (4-alleile-2-metossifenolo) è un estratto di olio di chiodi di garofano ampiamente utilizzato in odontoiatria come agente terapeutico, più comunemente come componente del cemento a base di ossido di zinco–eugenolo applicato come base o medicazione temporanea per la dentina o come sigillante per canali radicolari. Sono stati riportati diversi studi sull'influenza istopatologica dei sigillanti per canali radicolari a base di ZOE sui tessuti. L'eugenolo che fuoriesce dai sigillanti per canali radicolari a base di ZOE può partecipare allo sviluppo di infiammazione periapicale o alla continuazione di una lesione periapicale preesistente.
Nello studio attuale, le reazioni infiammatorie del tessuto sottocutaneo all'Endométhasone sono diminuite nel tempo, similmente ai risultati ottenuti da Kaplan et al., probabilmente a causa della neutralizzazione dell'eugenolo liberato all'inizio e dalla liberazione locale di corticoidi come il desametasone e l'idrocortisone. Molti ricercatori hanno suggerito che la capacità irritativa dei sigillanti a base di ZOE potrebbe essere attribuita principalmente all'eugenolo e secondariamente agli ioni di zinco. L'eugenolo può inibire la funzione dei macrofagi e può influenzare le reazioni infiammatorie nei tessuti periapicali. È stato dimostrato che il paraformaldeide provoca reazioni allergiche e necrosi del tessuto connettivo. Tuttavia, nonostante l'alta concentrazione di paraformaldeide nel sigillante Endométhasone, nello studio attuale tali risultati non sono stati osservati.
Recentemente, è stato introdotto un nuovo sigillante endodontico a base di metacrilato come sigillante per canali radicolari. EndoREZ è un materiale idrofilo, a 2 componenti, a indurimento chimico contenente ossido di zinco, solfato di bario, resine e pigmenti in una matrice di resina di dimetacrilato di urethane.
Le proprietà biologiche di EndoREZ sono state precedentemente investigate riguardo alla sua citotossicità e biocompatibilità tissutale. Gli studi riguardanti la biocompatibilità tissutale dei sigillanti a base di resina hanno mostrato reazioni infiammatorie da moderate a severe. Nello studio attuale, EndoREZ ha causato reazioni infiammatorie severe in tutti i periodi sperimentali. Poiché la vita media di un neutrofilo al di fuori del vaso sanguigno è di 7 giorni, la presenza di cellule polimorfonucleate in tutti i periodi sperimentali suggerisce un comportamento tossico di questo materiale. Utilizzando cellule coltivate, è stato dimostrato che EndoREZ diventava sempre più citotossico con il tempo di esposizione e presentava rischi citotossici significativi quando appena mescolato. La reazione del tessuto connettivo a tubi di silicone riempiti con EndoREZ impiantati nel tessuto sottocutaneo di ratti ha mostrato una reazione severa che ha cambiato significativamente il suo profilo dopo 30 giorni, con una reazione moderata dopo 3 mesi e assenza di infiammazione dopo 4 mesi. Tuttavia, è stato anche riportato che, in alcuni animali, la risposta infiammatoria è persistere in tutti i periodi sperimentali. Si è ritenuto che dopo l'impianto sottocutaneo di EndoREZ fresco, componenti come zinco e bario fossero in contatto diretto con il tessuto e causassero la severa reazione iniziale. In contrasto con i risultati della presente ricerca, Zmener et al. hanno dimostrato una risposta soddisfacente del tessuto osseo nel periodo di osservazione di 60 giorni di EndoREZ impiantato nelle tibie dei ratti. La lenta degradazione del sigillante EndoREZ, illustrata dal materiale disperso, e la successiva endocitosi da parte dei macrofagi, potrebbero essere state la causa di tale infiammazione cronica persistente. Inoltre, la terapia canalare eseguita con coni di gutta-percha condensati lateralmente in combinazione con EndoREZ sembra presentare un buon tasso di successo complessivo dopo una valutazione di richiamo di 14-24 mesi.
Inoltre, nello studio attuale è stata osservata la presenza di molte cellule mastocitarie nel tessuto connettivo, principalmente nell'area circostante i vasi sanguigni, nei periodi del 30°, 60° e 90° giorno, suggerendo una reazione ipersensibile tardiva ai componenti di EndoREZ. Sebbene la reazione ipersensibile tardiva ai materiali endodontici non sia frequentemente riportata, queste reazioni avverse sistemiche, che si verificano più frequentemente di quanto riportato in letteratura, non dovrebbero essere sottovalutate. Secondo Bratel et al., i materiali endodontici possono indurre una reazione ipersensibile tardiva anche in concentrazioni sub-tossiche.
Conclusione
Secondo i criteri FDI, i risultati ottenuti nello studio attuale hanno permesso di concludere che il sigillante per canali radicolari Endométhasone ha presentato biocompatibilità nei periodi analizzati, mentre EndoREZ non ha mostrato un comportamento biocompatibile e una suggestione di reazione ipersensibile tardiva.
Autori: Edilson José Zafalon, Marco Aurélio Versiani, Cássio José Alves de Souza, Camila Christian Gomes Moura, Paula Dechichi
Riferimenti:
- Bernath M, Szabo J. Reazione tissutale iniziata da diversi sigillanti. Int Endod J 2003;36:256-61.
- Bouillaguet S, Wataha JC, Lockwood PE, Galgano C, Golay A, Krejci I. Citotossicità e proprietà sigillanti di quattro classi di sigillanti endodontici valutati mediante attività della succinato deidrogenasi e microscopia confocale a scansione laser. Eur J Oral Sci 2004; 112:182-7.
- Kaplan AE, Ormaechea MF, Picca M, Canzobre MC, Ubios AM. Proprietà reologiche e biocompatibilità dei sigillanti endodontici. Int Endod J 2003;36:527-32.
- Hauman CH, Love RM. Biocompatibilità dei materiali dentali utilizzati nella terapia endodontica contemporanea: una revisione. Parte 2. Materiali per il riempimento dei canali radicolari. Int Endod J 2003;36:147-60.
- Gençoĝlu N, Turkmen C, Ahiskali R. Un nuovo sigillante per canali radicolari a base di silicio (Roekoseal-Automix). J Oral Rehabil 2003;30:753-7.
- Zmener O, Banegas G, Pameijer CH. Risposta del tessuto osseo a un sigillante endodontico a base di metacrilato: uno studio istologico e istometrico. J Endod 2005;31:457-9.
- Huang TH, Yang JJ, Li H, Kao CT. La valutazione della biocompatibilità dei sigillanti per canali radicolari a base di resina epossidica in vitro. Biomaterials 2002;23:77-83.
- Ozbas H, Yaltirik M, Bilgic B, Issever H. Reazioni del tessuto connettivo a compomeri, compositi e materiali di riempimento in amalgama. Int Endod J 2003;36:281-7.
- Ho Y-C, Huang F-M, Chang Y-C. Meccanismi di citotossicità dell'eugenolo nelle cellule osteoblastiche umane in vitro. Int Endod J 2006;39:389-93.
- Hauman CH, Love RM. Biocompatibilità dei materiali dentali utilizzati nella terapia endodontica contemporanea: una revisione. Parte 1. Farmaci e sostanze intracanalari. Int Endod J 2003;36:75-85.
- Sousa CJ, Loyola AM, Versiani MA, Biffi JC, Oliveira RP, Pascon EA. Una valutazione istologica comparativa della biocompatibilità dei materiali utilizzati nella chirurgia apicale. Int Endod J 2004;37:738-48.
- Tepel J, Darwisch el Sawaf M, Hoppe W. Reazione del tessuto periapicale infiammato a medicamenti intracanalari e sigillanti per canali radicolari. Endod Dent Traumatol 1994;10:233-8.
- Gerosa R, Menegazzi G, Borin M, Cavalleri G. Valutazione della citotossicità di 6 sigillanti per canali radicolari. J Endod 1995;21:446-8.
- Vajrabhaya L, Sithisarn P. Colture cellulari multilivello e monolivello in un saggio di citotossicità di sigillanti per canali radicolari. Int Endod J 1997;30:141-4.
- Bratel J, Jontell M, Dahlgren U, Bergenholtz G. Effetti dei sigillanti per canali radicolari sulle cellule immunocompetenti in vitro e in vivo. Int Endod J 1998;31:178-88.
- Serper A, Ucer O, Onur R, Etikan I. Effetti neurotossici comparativi dei materiali di riempimento dei canali radicolari sul nervo sciatico del ratto. J Endod 1998;24:592-4.
- Ersev H, Schmalz G, Bayirli G, Schweikl H. Potenzialità citotossiche e mutagene di vari materiali di riempimento dei canali radicolari in cellule eucariotiche e procariotiche in vitro. J Endod 1999;25:359-63.
- Telli C, Serper A, Dogan AL, Guc D. Valutazione della citotossicità dei sigillanti per canali radicolari a base di fosfato di calcio mediante saggio MTT. J Endod 1999;25:811-3.
- Huang FM, Tai KW, Chou MY, Chang YC. Citotossicità dei sigillanti per canali radicolari a base di resina, ossido di zinco-eugenolo e idrossido di calcio sulle cellule del legamento parodontal umano e sulle cellule V79 permanenti. Int Endod J 2002;35:153-8.
- Schwarze T, Fiedler I, Leyhausen G, Geurtsen W. La compatibilità cellulare di cinque sigillanti endodontici durante il periodo di indurimento. J Endod 2002;28:784-6.
- Schwarze T, Leyhausen G, Geurtsen W. Citocompatibilità a lungo termine di vari sigillanti endodontici utilizzando un nuovo modello di canale radicolare. J Endod 2002;28:749-53.
- Gomes BP, Pedroso JA, Jacinto RC, Vianna ME, Ferraz CC, Zaia, AA, et al. Valutazione in vitro dell'attività antimicrobica di 5 sigillanti per canali radicolari. Braz Dent J 2004;15:30-5.
- Perassi FT, Filho IB, Berbert FL, Carlos IZ, de Toledo Leonardo R. Secrezione di fattore di necrosi tumorale-alfa da parte dei macrofagi peritoneali di topo in presenza di sigillanti dentali, sealapex ed endométhasone. J Endod 2004;30:534-7.
- Pizzo G, Giammanco GM, Cumbo E, Nicolosi G, Gallina G. Attività antibatterica in vitro dei sigillanti endodontici. J Dent 2006; 34:35-40.
- Zmener O. Risposta tissutale a un nuovo sigillante per canali radicolari a base di metacrilato: osservazioni preliminari nel tessuto connettivo sottocutaneo dei ratti. J Endod 2004;30:348-51.
- Zmener O, Pameijer CH. Valutazione clinica e radiografica di un sigillante per canali radicolari a base di resina. Am J Dent 2004;17:19-22.
- Louw NP, Pameijer CH, Norval G. Valutazione istopatologica di un sigillante per canali radicolari in primati subumani [abstract]. J Dent Res 2001;80:654.
- Fédération Dentaire International, Commission of Dental Materials, Instruments, Equipment and Therapeutics. Pratiche standard raccomandate per la valutazione biologica dei materiali dentali. Int Dent J 1980;30:140-88.
- Istituti Nazionali di Salute. Politica del Servizio Sanitario Pubblico sulla cura e l'uso umano degli animali da laboratorio, 2006. Disponibile su: http://grants.nih.gov/grants/olaw/references/phspol.htm.
- Istituti Nazionali di Salute. Politica del Servizio Sanitario Pubblico sulla cura e l'uso umano degli animali da laboratorio chiarimento riguardo all'uso di anidride carbonica per l'eutanasia di piccoli animali da laboratorio, 2006. Disponibile su: http://grants.nih.gov/grants/olaw/ Compilation_of_Guidance.doc.
- Stanley HR. Test di tossicità dei materiali dentali. 1a ed. Miami: CRC Press; 1985.
- Sousa CJA, Montes CRM, Pascon EA, Loyola AM, Versiani MA. Confronto della biocompatibilità intraossea di sigillanti per canali radicolari AH Plus, Endo-REZ ed Epiphany. J Endod 2006;32:656-62.
- Huang FM, Tsai CH, Yang SF, Chang YC. Induzione dell'espressione genica di interleuchina-6 e interleuchina-8 da parte dei sigillanti per canali radicolari nelle cellule osteoblastiche umane. J Endod 2005;31:679-83.
- Olsson B, Sliwkowski A, Langeland K. Impianto sottocutaneo per la valutazione biologica dei materiali endodontici. J Endod 1981;7:355-67.
- de Oliveira L, Borges MM, Leal RC, Assreuy J, Kloetzel JK. Coinvolgimento dell'ossido nitrico nell'infezione sperimentale di Trypanosoma cruzi in Calomys callosus e topi svizzeri. Parasitol Res 1997;83:762-770.
- Tanisaki M, Ogawa K, Lapa SRC, Da Silva PMC, Watanabe I. Studio morfometrico e di microscopia elettronica a scansione ad alta risoluzione del nervo palatino maggiore di Calomys callosus. Int J Morphol 2005;23:13-8.
- Dost CK, Saraiva J, Zentgraf U, Monesi N, Engels W, Albuquerque S. È coinvolto l'ossido nitrico nella tolleranza di Calomys callosus come ospite serbatoio verso l'infezione da Trypanosoma cruzi? J Infect 2006;52:49-55.
- Taniwaki NN, Andreoli WK, Calabrese KS, da Silva S, Mortara RA. Disruzione delle proteine miofibrillari nel muscolo cardiaco di Calomys callosus infettato cronico con Trypanosoma cruzi e trattato con un agente immunosoppressivo. Parasitol Res 2005;97:323-31.
- Martinez M, Milton FA, de Oliveira SA, de Lima NF, Segatelli TM, Pinheiro PF, et al. Cambiamenti ultrastrutturali nella mucosa palatina dura di Calomys callosus dopo 120 giorni di alcolismo cronico sperimentale. J Submicrosc Cytol Pathol 2005;37:59-65.
- Carroll DS, Mills JN, Montgomery JM, Bausch DG, Blair PJ, Burans JP, et al. Sindrome polmonare da hantavirus in Bolivia centrale: relazioni tra ospiti serbatoi, habitat e genotipi virali. Am J Trop Med Hyg 2005;72:42-6.
- Gomes-Filho JE, Gomes BP, Zaia AA, Novaes PD, Souza-Filho FJ. Metacrilato di glicole: un metodo alternativo per l'incapsulamento di impianti sottocutanei. J Endod 2001;27:266-8.
- Pascon EA, Leonardo MR, Safavi K, Langeland K. Reazione tissutale ai materiali endodontici: metodi, criteri, valutazione e osservazioni. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 1991;72:222-37.
- Holland R, Otoboni Filho JA, Bernabé PF, Nery MJ, de Souza V, Berbert A. Effetto dello stato del canale radicolare sulla guarigione parodontale dopo un infortunio chirurgico nei cani. Endod Dent Traumatol 1994;10:77-82.
- Hume WR. Effetto dell'eugenolo sulla respirazione e divisione della polpa umana, fibroblasti di topo e cellule epatiche in vitro. J Dent Res 1984;63:1262-5.
- Gulati N, Chandra S, Aggarwal PK, Jaiswal JN, Singh M. Citotossicità dell'eugenolo in un sigillante contenente ossido di zinco. Endod Dent Traumatol 1991;7:181-5.
- Neff T, Layman D, Jeansonne BG. Valutazione della citotossicità in vitro dei sigillanti endodontici esposti al calore prima del saggio. J Endod 2002;28:811-4.
- Ioannis K, Nikolaos E. Confronto in vivo della biocompatibilità di 2 sigillanti per canali radicolari impiantati nel tessuto connettivo sottocutaneo dei ratti. J Endod 1998;24:82-5.
- Nikolaos E, Ioannis K. Studio sperimentale della biocompatibilità di quattro sigillanti per canali radicolari e della loro influenza sul contenuto di zinco e calcio di vari tessuti. J Endod 1995;21:122-7.
- Segura JJ, Jimenez-Rúbio A. Effetto dell'eugenolo sull'adesione dei macrofagi in vivo a superfici plastiche. Endod Dent Traumatol 1998;14:72-4.
- de Oliveira Mendes ST, Ribeiro Sobrinho AP, de Carvalho AT, de Souza Cortes MI, Vieira LQ. Valutazione in vitro della citotossicità di due sigillanti per canali radicolari sull'attività dei macrofagi. J Endod 2003;29:95-9.
- Di Felice R, Lombardi T. Necrosi gengivale e ossea mandibolare causata da una pasta contenente paraformaldeide. Endod Dent Traumatol 1998;14:196-198.
- Cotran RS, Kumar V, Robbins SL. Fondamenti patologici della malattia: eventi cellulari. 5a ed. Philadelphia: Saunders; 1994.
- el Sayed F, Seite-Bellezza D, Sans B, Bayle-Lebey P, Marguery MC, Bazex J. Urticaria da contatto da formaldeide in una pasta dentale per canali radicolari. Contact Dermatitis 1995;33:353.
- Ebner H, Kraft D. Anafilassi indotta da formaldeide dopo trattamento dentale? Contact Dermatitis 1991;24:307-9.
