Colonizzazione microbica all'interfaccia impianto-abutment e il suo possibile influsso sulla peri-implantite: una revisione sistematica e meta-analisi
Traduzione automatica
L'articolo originale è scritto in lingua EN (link per leggerlo) .
Abstract
Scopo: Lo scopo di questa revisione sistematica e meta-analisi era di valutare la colonizzazione microbica alle interfacce impianto-abutment (IAI) su impianti a livello osseo e di identificare possibili associazioni con condizioni peri-impiantari.
Selezione degli studi: La domanda principale mirava a rispondere se gli impianti osseointegrati a due pezzi, in funzione per almeno 1 anno, negli esseri umani, siano correlati a un conteggio batterico più elevato e all'insorgenza di peri-implantite, rispetto a condizioni peri-impiantari sane. La strategia di ricerca ha incluso la letteratura on-line (MedLine, Google scholar, Cochrane library) dal 1990 fino a marzo 2015 pubblicata in inglese utilizzando combinazioni di MeSH (Medical Subject Headings) e termini di ricerca. La valutazione della qualità degli articoli selezionati in testo completo è stata effettuata secondo le linee guida ARRIVE e CONSORT. Per l'analisi dei dati, il conteggio batterico totale di Porphyromonas gingivalis, Tannerella forsythia, Treponema denticola, Prevotella intermedia e Fusobacterium nucleatum è stato calcolato e confrontato con IAI con o senza patologia peri-impiantare.
Risultati: Un totale di 14 articoli, che riportano dati da 1126 impianti, ha soddisfatto i criteri di inclusione ed è stato sottoposto a valutazione della qualità. Gli studi selezionati hanno rivelato contaminazione dell'IAI, in pazienti che hanno ricevuto sistemi di impianto a due pezzi. La meta-analisi ha indicato una differenza significativa nel conteggio totale dei batteri tra impianti colpiti da peri-implantite rispetto ai tessuti peri-implantari sani (0.387 0.055; 95% CI 0.279–0.496). Sono stati identificati conteggi batterici inferiori nell'IAI sano per tutti i batteri gram-negativi investigati, tranne per T. forsythia.
Introduzione
Le microfessure all'interfaccia impianto-abutment (IAI) sono tipiche dei sistemi di impianto dentale osseointegrato a due pezzi e sembrano svolgere un ruolo significativo nella colonizzazione batterica nel solco peri-implantare. Questo, a sua volta, può portare a reazioni infiammatorie peri-implantari e successivamente alla perdita di osso di supporto. La perdita batterica all'IAI insieme agli assemblaggi delle viti di abutment che agiscono come serbatoi batterici può innescare una risposta dell'ospite con tessuti molli infiammati e possibile perdita marginale di osso peri-implantare.
La colonizzazione batterica dello spazio all'interno dell'IAI è stata anche implicata nell'establishment della larghezza biologica fisiologica. La maggior parte della perdita ossea marginale è stata riportata durante il primo anno dopo l'inserimento dell'impianto, dopodiché, nei pazienti con livelli adeguati di igiene orale, i livelli ossei marginali si sono stabilizzati nel corso degli anni. La micropermeabilità nello spazio tra l'impianto e l'abutment può consentire il passaggio di acidi, enzimi, batteri e/o i loro prodotti metabolici che influenzano direttamente il tessuto parodontale, causando sanguinamento, gonfiore e odore. Tuttavia, le connessioni a morse sono ritenute presentare livelli inferiori di micropermeabilità e perdita ossea marginale rispetto agli impianti a connessione esterna.
Una recente revisione della letteratura ha descritto Porphyromonas gingivalis, Treponema denticola e Tannerella forsythia, trovati nei campioni di biofilm subgengivale, come microrganismi con evidenze moderate di associazione con l'insorgenza della periimplantite. Al contrario, sono state trovate solo alcune evidenze per Prevotella intermedia e Campylobacter rectus. In condizioni anaerobiche, come quelle presenti all'interno dell'IAI, le figure microbiologiche potrebbero essere responsabili della selezione, nel medio-lungo termine, di specie microbiologiche in grado di innescare il processo di periimplantite.
Gli obiettivi di questa revisione sistematica e meta-analisi erano di valutare la colonizzazione microbiologica all'interfaccia impianto-abutment su impianti a due pezzi, a livello osseo, indipendentemente dalla configurazione della connessione, e indagare se ciò sia correlato all'insorgenza della periimplantite.
Selezione dello studio
Questa revisione sistematica ha rispettato le linee guida per la segnalazione preferita degli articoli per revisioni sistematiche e meta-analisi (PRISMA) (http://www.prisma-statement.org). Il protocollo di questa revisione sistematica è stato pubblicato nel registro internazionale prospettico delle revisioni sistematiche (PROSPERO, http://www.crd.york.ac.uk/PROSPERO/) con numero di registrazione CRD42016037481. La domanda focalizzata della revisione era identificare se ci sia una relazione tra la presenza di un conteggio batterico più elevato e l'insorgenza della periimplantite, rispetto a condizioni peri-implantari sane in pazienti con impianti osseointegrati a due pezzi dopo almeno 1 anno di funzionamento. La periimplantite è stata definita dalla presenza di una profondità di sondaggio peri-implantare ≥5mm associata a sanguinamento al sondaggio e/o suppurazione, e immagini radiografiche di perdita ossea ≥3 mm, rispetto alle radiografie iniziali al momento della consegna della riabilitazione protesica.
2.1. Fonti di informazione
Sono stati cercati articoli pubblicati solo in inglese che riportassero sulla colonizzazione microbica all'IAI e la sua relazione con l'insorgenza della periimplantite, pubblicati dal 1990 fino a marzo 2015 nel database PubMed della Biblioteca Nazionale di Medicina degli Stati Uniti (http://www.ncbi.nlm.nih.gov/pubmed/), Google Scholar (http://www.google.com) e la Cochrane Library (http://www.cochranelibrary.com/). Inoltre, le referenze degli articoli inclusi sono state controllate manualmente per trovare articoli aggiuntivi.
2.2. Strategia di ricerca
Inizialmente, la domanda PICOS (Popolazione (P), Intervento (I), Confronto (C), Risultati e Disegno dello Studio (O), Tipo di Studio (S)) ha definito la strategia di ricerca, dove P=Impianti osseointegrati a due pezzi con diagnosi di periimplantite dopo almeno 1 anno di funzionamento; I=Colonizzazione microbica all'IAI; C=Condizioni peri-implantari sane; O=Tasso di sopravvivenza; S=Studi clinici controllati randomizzati (RCT) e studi di follow-up clinico.
Le banche dati elettroniche sono state cercate utilizzando una combinazione di termini MeSH (Medical Subject Headings), termini di ricerca e le loro combinazioni: “impianti dentali” [MeSH] E “contaminazione batterica” O “presenza di batteri” O “perdita dentale/microbiologia” [MeSH] O “microperdita” O “risultati microbiologici” O “colonizzazione microbiologica” O “microbiota” O “microflora peri-implantare” E “peri-implantite” [MeSH] O “patologia peri-implantare” O “malattia peri-implantare” E “Abutment Dentali*/microbiologia” [MeSH] “connessione, impianto-abutment” O “design impianto-abutment” [MeSH] O “giunzione impianto-abutment” O “microgap impianto-abutment” O “spazio interno degli impianti dentali” O “parte interna degli impianti dentali”.
2.3. Selezione degli studi e criteri di idoneità
Tutti i titoli e gli abstract degli studi selezionati sono stati inizialmente valutati in base ai seguenti criteri di inclusione: (1) Articoli scritti in inglese; (2) studi con un esame clinico dei pazienti; (3) studi che valutano il conteggio di diverse specie batteriche (conteggio batterico, BC) a livello di IAI in pazienti che hanno ricevuto sistemi di impianto a livello osseo a due fasi, indipendentemente dalla configurazione della connessione; (4) studi clinici controllati randomizzati (RCT), studi di coorte prospettici o studi trasversali che riportano su impianti in funzione per almeno 1 anno.
Dopo aver valutato il testo completo degli articoli secondo i criteri di esclusione precedentemente definiti, gli articoli con le seguenti caratteristiche, senza restrizioni di lingua, non sono stati considerati idonei: (a) Lettere, revisioni narrative o storiche; (2) studi su animali e in vitro; (3) Rapporti su siti e/o condizioni compromessi localmente o sistemicamente (cioè difetto osseo maggiore prima dell'impianto, patologie ossee, radioterapia testa e collo, trattamento con bisfosfonati); (4) rapporti su pazienti che hanno ricevuto debridement meccanico nei 3 mesi precedenti o antibiotici negli ultimi 6 mesi prima dell'analisi.
2.4. Processo di raccolta dei dati
Due revisori calibrati (M.C. e L.C.) hanno esaminato e raccolto i dati dagli articoli selezionati su tabelle strutturate. I valori di Kappa di Cohen tra gli esaminatori sono stati calcolati sia nella prima che nella seconda fase della ricerca. Le discrepanze sono state risolte per consenso e un terzo esaminatore (M.T.) è stato consultato.
Articoli senza abstract ma con titoli correlati agli obiettivi di questa revisione sono stati selezionati e il loro testo completo è stato esaminato per l'idoneità. Le liste di riferimento degli articoli selezionati sono state ulteriormente esaminate per possibili articoli aggiuntivi. Inoltre, sono state condotte ricerche manuali delle bibliografie delle revisioni sistematiche selezionate limitate alle seguenti riviste: Clinical Implant Dentistry and Related Research; Clinical Oral Implants Research; International Journal of Oral and Maxillofacial Implants; Journal of Clinical Periodontology; Journal of Periodontology.
2.5. Valutazione della qualità, eterogeneità e rischio di bias degli studi individuali
Gli stessi revisori hanno valutato il rischio di bias nel campione incluso secondo le linee guida fornite dalla dichiarazione CONSORT per la valutazione degli studi controllati randomizzati (http://www.consort-statement.org), la dichiarazione STROBE per studi osservazionali (http://www.strobe-statement.org), così come gli elementi modificati dello strumento della Collaborazione Cochrane per la valutazione del rischio di bias (Tabella 1).
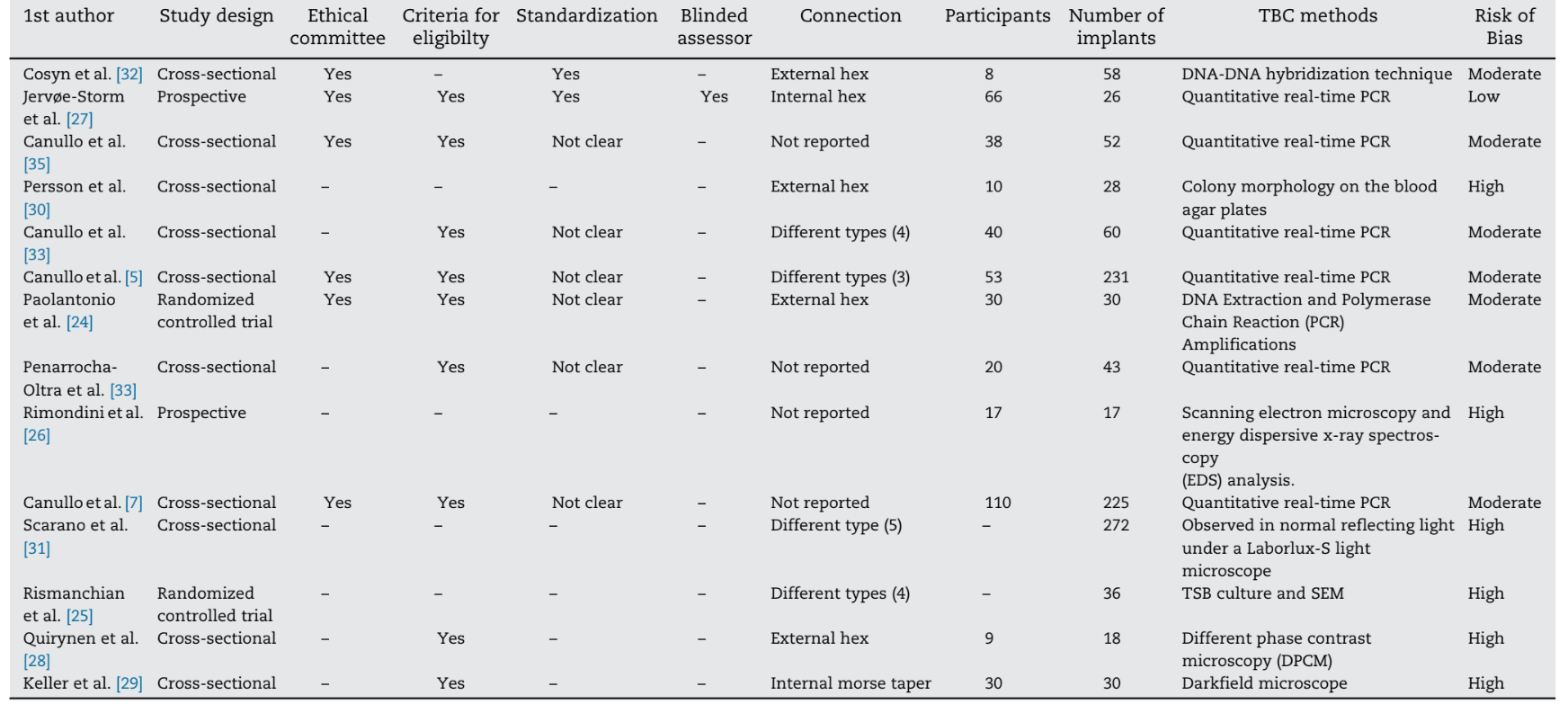
Considerando l'adeguatezza nei rispettivi studi, gli elementi sono stati valutati e la percentuale di elementi valutati positivamente è stata calcolata. La valutazione della qualità è stata eseguita in due fasi diverse, ovvero la fase I in cui la valutazione della qualità si basava sugli articoli pubblicati in testo completo eseguiti indipendentemente da entrambi i revisori e nella fase II in cui le discrepanze sono state risolte mediante discussione. Dopo aver raccolto i punteggi nella fase II della valutazione della qualità, è stata completata una stima complessiva del plausibile rischio di bias (basso, moderato o alto) per ciascun studio selezionato. Mentre un basso rischio di bias è stato stimato quando tutti i criteri erano soddisfatti, un rischio moderato è stato considerato quando uno o più criteri erano parzialmente soddisfatti e un alto rischio di bias è stato stimato quando uno o più criteri non erano soddisfatti (Cochrane Handbook for Systematic Reviews of Interventions, versione 5.1.0. http://www.cochrane.org/resources/handbook).
2.6. Misure e analisi dei risultati
Sono state eseguite statistiche descrittive, meta-regressione e meta-analisi, basate sugli studi comparabili che riportano le stesse misure di esito. Il microbiota presente all'IAI degli impianti in funzione per almeno 1 anno è stato considerato per l'analisi dei dati. I BC di batteri gram-negativi associati a parodontite cronica (P. gingivalis, T. forsythia, T. denticola, P. intermedia e Fusobacterium nucleatum) sono stati estratti e definiti come variabile di esito primaria. Il microbiota incluso per l'analisi è regolarmente rilevato nei siti di peri-implantite e si è dimostrato aumentare il rischio di perdita ossea peri-implantare e progressione della malattia. Le differenze medie sono state combinate utilizzando modelli a effetti casuali. L'eterogeneità tra gli studi, le analisi di sottogruppo, la meta-analisi e i grafici a foresta sono stati calcolati utilizzando un programma software (Comprehensive Meta-Analysis V3; Biostat, Englewood, NJ, USA).
Risultati
3.1. Selezione dello studio
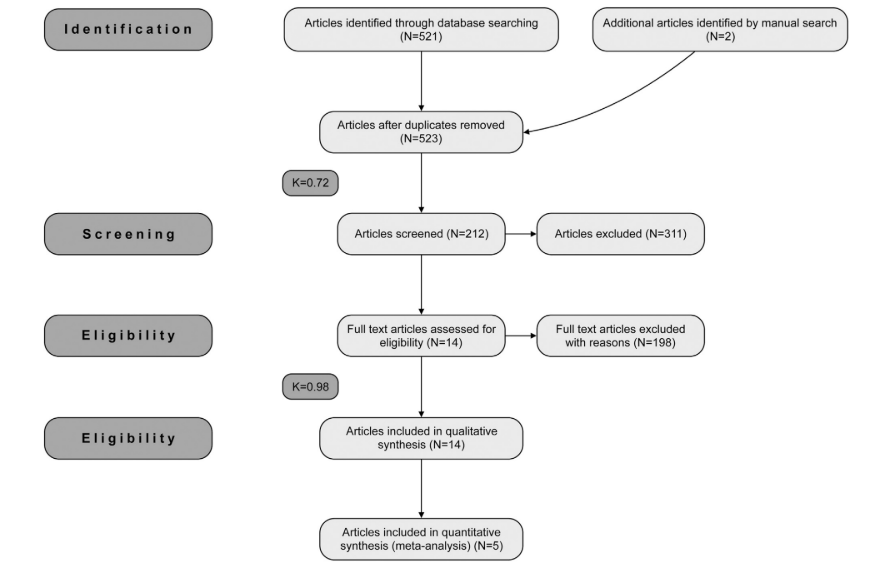
Un totale di 523 titoli e abstract potenzialmente rilevanti sono stati trovati dopo la ricerca elettronica e manuale. Durante la prima fase di selezione, 309 articoli sono stati esclusi sulla base dei titoli e degli abstract (k=0.72). Durante la seconda fase, sono stati valutati gli articoli completi delle rimanenti 212 pubblicazioni e 198 articoli sono stati esclusi poiché non soddisfacevano i criteri di inclusione (k=0.98). Infine, un totale di 14 articoli, che riportano dati da 1126 impianti, sono stati selezionati poiché soddisfacevano i criteri di inclusione e la valutazione della qualità richiesta per questa revisione sistematica (Fig. 1).
3.2. Caratteristiche dello studio
I 14 articoli selezionati sono stati pubblicati tra il 1993 e marzo 2015, di cui due erano RCT, due studi di coorte prospettici e dieci studi trasversali. Solo uno studio clinico prospettico è stato redatto seguendo la dichiarazione STROBE per studi osservazionali (http://www.strobe-statement.org). Pertanto, non è stata possibile una comparazione diretta tra gli articoli selezionati.
3.3. Rischio di bias all'interno degli studi
Nessuno degli studi retrospettivi è stato in grado di soddisfare tutti i requisiti. Una pubblicazione è stata associata a un basso rischio di bias, sette a un rischio moderato di bias e sei a un alto rischio di bias. Gli articoli inclusi hanno ricevuto una valutazione minima quando si è trattato di valutare la presentazione ai comitati etici (6/14), la presenza di valutatori ciechi (2/14), la standardizzazione delle procedure (1/14) e la presenza di criteri di idoneità (9/14) (Tabella 1).
3.4. Misure e analisi di meta-regressione
3.4.1. Perdita batterica all'IAI
Tutti gli studi selezionati hanno riportato contaminazione dell'IAI e della superficie dell'abutment in pazienti che ricevevano l'assemblaggio di un sistema implantare a due fasi. La reazione a catena della polimerasi in tempo reale quantitativa (PCR) è stata eseguita per BC in 7 dei 14 studi in cui sono stati analizzati i seguenti patogeni: Aggregatibacter actinomycetemcomitans, P. gingivalis, T. forsythia, T. denticola, P. intermedia, Parvimonas micra, F. nucleatum, C. rectus, Eikenella corrodens, Candida albicans, Enterococcus faecalis, e Porphyromonas aeruginosa. Mentre in uno studio è stata utilizzata la tecnica di ibridazione DNA-DNA a scacchiera, in altri sei studi sono state utilizzate diverse tecniche, tra cui la microscopia elettronica a scansione, per esaminare la morfologia delle colonie. In uno studio, è stata descritta la colonizzazione progressiva da parte di batteri patogeni parodontali nelle porzioni interne degli impianti a due pezzi. In un altro studio, i componenti intra-coronali delle restaurazioni fisse trattenute da vite erano pesantemente contaminati in tutti i campioni. La contaminazione delle viti di abutment è avvenuta molto probabilmente dal solco peri-implantare attraverso l'IAI e l'interfaccia abutment-protesi. Allo stesso modo, sono state osservate differenze significative nei batteri nosocomiali resistenti agli antibiotici (E. faecalis e P. aeruginosa) tra i componenti interni ed esterni dell'impianto tra solchi peri-implantari sani e impianti compromessi da peri-implantite. Riguardo all'assenza/presenza dei batteri analizzati, non sono state trovate differenze rilevanti tra l'analisi al solco peri-implantare e le connessioni all'interno delle superfici degli abutment. La composizione microbica nei denti adiacenti assomigliava a quella trovata nel solco peri-implantare con un'alta frequenza per P. gingivalis, T. forsythia, P. intermedia, P. micra e E. corrodens.
Due studi comparativi tra condizioni peri-implantari sane e impianti affetti da peri-implantite hanno riportato contaminazione batterica in entrambi i gruppi. Le specie del complesso arancione (P. intermedia, P. micra, F. nucleatum) erano le più prevalenti in tutti i siti analizzati per entrambi i gruppi. All'interno della connessione dell'impianto, la prevalenza delle specie analizzate era più predominante nel gruppo peri-implantite e variava dall'1,1% A. actinomycetemcomitans al 98,9% F. nucleatum. Le specie con ≥50% di prevalenza erano: P. gingivalis, T. denticola, P. intermedia, F. nucleatum, C. rectus, E. corrodens, T. forsythia e P. micra.
3.4.2. Perdite batteriche all'IAI in relazione al design della connessione dell'abutment
Il campione selezionato ha mostrato una maggiore eterogeneità riguardo al tipo di IAI. Quattro studi hanno riportato connessioni a esagono esterno e due studi su esagoni interni o connessioni a morse. Quattro studi hanno utilizzato diversi design di IAI, mentre il tipo di IAI non è stato riportato negli altri 4 manoscritti.
La valutazione di quattro diversi IAI ha implicato che tutte le connessioni analizzate presentavano contaminazione dopo 5 anni di carico funzionale. È emerso anche che il design della connessione potrebbe aver influenzato i livelli di BC qualitativamente e quantitativamente, specialmente all'interno delle connessioni implantari, mostrando risultati migliori per la connessione conica. Allo stesso modo, diversi tipi di pilastri hanno mostrato una variazione significativa nella dimensione media del microgap nelle prime 5 ore di carico. Tuttavia, non è stata trovata alcuna influenza significativa della microperdita a 24 ore, 48 ore e 14 giorni sui livelli di BC. Tuttavia, l'uso di pilastri standard ha ridotto significativamente la dimensione del microgap rispetto a quelli personalizzati. Lo studio ha concluso che la microperdita nell'area di connessione era comparabile per tutti i pilastri analizzati.
3.4.3. Meta-regressione e analisi dei sottogruppi
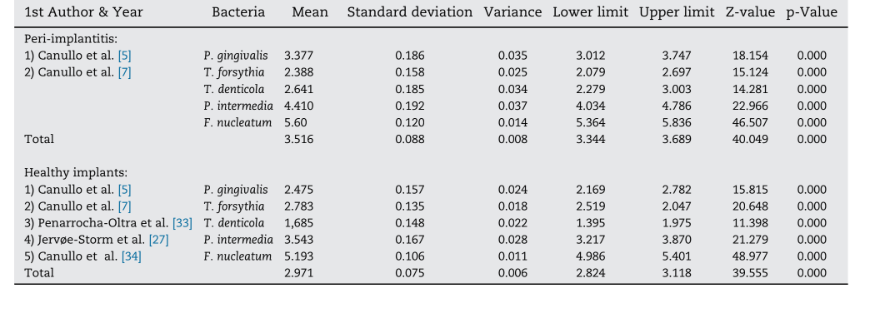
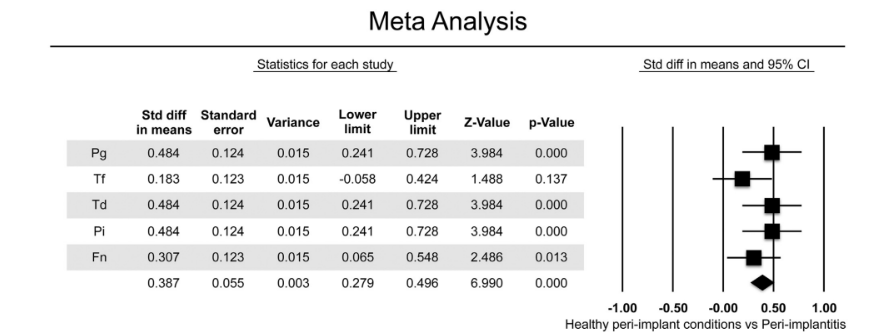
Cinque studi, che includevano un totale di 622 impianti (n=223 con periimplantite; n=399 con condizioni peri-implantari sane) in funzione per almeno 1 anno, sono stati inclusi nella meta-analisi. Il BC dei batteri anaerobici gram-negativi ha mostrato rilevanza per la parodontite cronica ed è stato trovato aumentare il rischio di perdita ossea peri-implantare e progressione della malattia a causa della presenza di patogeni parodontali (P. gingivalis, T. forsythia, T. denticola, P. intermedia, F. nucleatum) (Tabella 2)]. La meta-analisi ha considerato i batteri che sono stati valutati in tutti gli studi selezionati. Due dei cinque studi hanno confrontato il BC in condizioni peri-implantari sane rispetto agli impianti colpiti da periimplantite. La meta-analisi ha rivelato valori medi più elevati per il BC di tutti i batteri gram-negativi analizzati, tranne per T. forsythia negli impianti con periimplantite (Fig. 2). Complessivamente, le differenze medie nel BC erano statisticamente significative tra i due gruppi analizzati, con valori più elevati negli impianti con periimplantite (differenza: 0.387 ± 0.055; 95% CI 0.279–0.496, p=0.000).
Discussione
Questa revisione sistematica ha valutato la colonizzazione microbica all'IAI su impianti a livello osseo e l'ha correlata all'eventuale insorgenza di periimplantite. Gli impianti monoblocco sono stati esclusi dall'analisi a causa della posizione sopracrestale del loro IAJ: infatti, questa posizione, a causa dell'ambiente aerobiotico, porta a una composizione microbiologica completamente diversa.
Nella presente revisione, eccetto per T. forsythia, è stato identificato un BC significativamente più elevato negli impianti colpiti da periimplantite rispetto ai sulci peri-implantari sani per tutti i plausibili patogeni parodontali gram-negativi. Per T. forsythia, è stata rilevata solo una tendenza verso un BC più elevato.
Gli studi inclusi hanno valutato il microbiota a livello di IAI in pazienti che hanno ricevuto sistemi di impianti a livello osseo a due fasi con vari design di connessione impianto-abutment. Tuttavia, due studi hanno riportato la contaminazione dell'IAI indipendentemente dal design di connessione. Non è stata fatta alcuna distinzione tra restauri trattenuti a vite e cementati, assumendo che la giunzione corona-abutment si trovi più coronale e che lo spazio sia riempito di cemento. Inoltre, i manoscritti inclusi non hanno trovato differenze tra impianti sommersi e non sommersi nella colonizzazione microbica.
La presenza di contaminazione batterica all'IAI posizionato a livello dell'osso alveolare è stata dimostrata essere associata a un'infiltrazione significativa di cellule infiammatorie e perdita ossea. L'aumento dell'accumulo di cellule infiammatorie acute adiacenti all'IAI suggerisce la persistenza di stimoli chemiotattici da questa regione che sostengono un reclutamento continuo di granulociti neutrofili. Inoltre, la presenza di un'infiltrazione infiammatoria del tessuto peri-implantare agli interface fixture-abutment è stata anch'essa causata da contaminazione microbica interna.
Un certo numero di studi ha riportato che la contaminazione microbica potrebbe verificarsi a livello dell'IAI sia in impianti con condizioni tissutali sane che malate. Nonostante il fatto che non ci fossero segni clinici di peri-implantite, la presenza delle specie batteriche associate a questa condizione era chiaramente elevata. Quando sono state valutate le caratteristiche cliniche e microbiologiche in soggetti e impianti con condizioni tissutali sane o peri-implantite e i dati dei siti implantari sani e malati sono stati confrontati all'interno dello stesso soggetto (534 pazienti; 1507 impianti dentali), sono state osservate chiare tendenze. L'analisi microbica ottenuta da tre posizioni (sulco peri-implantare (PIS), parti interne delle connessioni dell'impianto (PI), sulco gengivale dei denti vicini) insieme ai parametri clinici (sanguinamento alla sondatura, profondità della tasca di sondaggio, indice di placca), la presenza di peri-implantite era evidente nel 10,3% dei pazienti e nel 7,3% degli impianti. L'analisi microbica all'interno dei 53 pazienti affetti da peri-implantite non ha rivelato differenze rilevanti tra l'analisi al PIS e al PI.
Il microgap all'IAI può anche portare a complicazioni meccaniche e biologiche, inclusi fratture delle viti di abutment e malattie peri-implantari. La dimensione del microgap e la perdita microbica in diversi momenti all'IAI di 4 diversi abutment per impianti Straumann hanno mostrato un effetto significativo sulla dimensione media del microgap (p<0.001) e sul numero medio di colonie batteriche (CFU/mL) che fuoriuscivano dall'IAI nelle prime 5 ore dell'esperimento (p=0.012). Tuttavia, la micro-perdita a 24 h, 48 h e 14 giorni non era più influenzata in modo significativo (p=0.145).
Le differenze cliniche e microbiche tra condizioni peri-implantari sane e peri-implantite hanno rivelato che la prevalenza microbica era più alta nel gruppo peri-implantite in tre posizioni e le differenze nella prevalenza tra i diversi tipi di batteri erano più marcate all'interno della connessione rispetto al PIS (57 pazienti; 122 impianti).
Quando i patogeni opportunistici (E. faecalis, P. aeruginosa) sono stati identificati in presenza di malattia peri-implantare a livello del PIS di ciascun impianto, del solco gengivale dei denti adiacenti e della connessione e dell'abutment nella porzione interna di ciascun impianto, sono state rilevate differenze significative sulla presenza e quantità di batteri nosocomiali attorno agli impianti malati. Questo potrebbe suggerire l'importanza della decontaminazione della connessione in caso di trattamento della peri-implantite.
Sono stati proposti diversi tentativi per ridurre la colonizzazione batterica all'IAI in caso di impianti sani. Tuttavia, l'applicazione di una soluzione di clorexidina allo 0,2% durante interventi chirurgici a due fasi è considerata una pratica più comune. Tuttavia, esistono opinioni contrastanti sull'efficacia della soluzione di clorexidina nel prevenire la colonizzazione microbica all'IAI. Gli endotossine batteriche penetrano tipicamente nell'IAJ, ma la soluzione di clorexidina allo 0,2% non è riuscita a eliminare significativamente la penetrazione, almeno a lungo termine. D'altra parte, non sono state fornite indicazioni nella letteratura nel caso di impianti affetti da periimplantite.
Non solo la perdita microbica attraverso il gap tra la sovrastruttura e l'abutment, ma anche i design e i materiali degli impianti possono influenzare il potenziale rischio di ospitare microrganismi orali. Tipicamente, le connessioni a morse hanno sviluppato meno batteri rispetto alla connessione conica interna a quattro scanalature. Allo stesso modo, le connessioni a morse hanno presentato risultati favorevoli in questo rispetto rispetto alla connessione cementata trilobata. D'altra parte, il microbiota batterico presente all'interno della connessione dell'impianto e nel fluido PIS di impianti con condizioni peri-implantari sane con quattro diversi sistemi di impianto dopo almeno 5 anni di carico funzionale, ha dimostrato contaminazione microbiologica in tutti i tipi di connessioni indipendentemente dal sito (sulco peri-implantare, porzione interna della connessione, superficie dell'abutment e sulco gengivale dei denti adiacenti).
Dal punto di vista clinico, le evidenze attuali possono suggerire la rimozione del complesso corona/abutment e la disinfezione/sterilizzazione delle unità di connessione sia negli aspetti dell'impianto che dell'abutment, in caso di malattia peri-implantare, come complemento ai regimi di manutenzione degli impianti dentali.
Conclusioni
Questa meta-analisi ha indicato che i batteri possono facilmente colonizzare l'interfaccia impianto-abutment. È evidente da un punto di vista clinico che le porzioni interne dell'IAI dovrebbero sempre essere considerate contaminate, anche in condizioni clinicamente sane.
Marco Tallarico, Luigi Canullo, Martina Caneva, Mutlu Özcan
Riferimenti
- Hermann JS, Buser D, Schenk RK, Schoolfield JD, Cochran DL. Larghezza biologica attorno a impianti in titanio a pezzo unico e a due pezzi. Clin Oral Implants Res 2001;12:559–71.
- Tsuge T, Hagiwara Y, Matsumura H. Adattamento marginale e microfessure dell'interfaccia impianto-abutment con configurazione interna anti-rotazione. Dent Mater J 2008;27:29–34.
- Schwarz F, Hegewald A, Becker J. Impatto della connessione impianto-abutment e posizionamento del collare lavorato/microfessura sui cambiamenti del livello osseo crestale: una revisione sistematica. Clin Oral Implants Res 2014;25:417–25.
- Weng D, Nagata MJH, Bell M, Bosco AF, de Melo LGN, Richter EJ. Influenza della posizione e configurazione della microfessura sulla morfologia ossea peri-implantare in impianti sommersi. Uno studio sperimentale su cani. Clin Oral Implants Res 2008;19:1141–7.
- Canullo L, Penarrocha-Oltra D, Covani U, Botticelli D, Serino G, Peñarrocha M. Risultati clinici e microbiologici in pazienti con periimplantite: uno studio trasversale. Clin Oral Implants Res 2015;27:376–82.
- Canullo L, Peñarrocha D, Clementini M, Iannello G, Micarelli C. Impatto del trattamento di pulizia con plasma di argon sugli abutment degli impianti in pazienti con una storia di malattia parodontale e biotipo sottile: risultati radiografici a 24 mesi di follow-up di un RCT. Clin Oral Implants Res 2015;26:8–14.
- Canullo L, Peñarrocha D, Covani U, Rossetti PHO. Risultati microbiologici e clinici di impianti in condizioni di salute e con periimplantite. J Oral Maxillofac Implants 2015;30:834–42.
- Quirynen M, Bollen CM, Eyssen H, van Steenberghe D. Penetrazione microbica lungo i componenti impiantari del sistema Brånemark. Uno studio in vitro. Clin Oral Implants Res 1994;5:239–44.
- Passos SP, Gressler May L, Faria R, Özcan M, Bottino MA. Gap impianto-abutment rispetto alla colonizzazione microbica: significato clinico basato su una revisione della letteratura. J Biomed Mater Res B Appl Biomater 2013;101:1321–8.
- Callan DP, Cobb CM, Williams KB. Identificazione di batteri che colonizzano le superfici interne dell'interfaccia impianto-abutment tramite sonda DNA: uno studio preliminare. J Periodontol 2005;76:115–20.
- Hermann JS, Schoolfield JD, Schenk RK, Buser D, Cochran DL. Influenza della dimensione della microfessura sui cambiamenti ossei crestali attorno agli impianti in titanio. Una valutazione istometrica di impianti non sommersi non caricati nella mandibola canina. J Periodontol 2001;72:1372–83.
- Piattelli A, Scarano A, Paolantonio M, Assenza B, Leghissa GC, Di Bonaventura G. Fluidi e penetrazione microbica nella parte interna delle connessioni impianto-abutment mantenute con cemento rispetto a quelle mantenute con vite. J Periodontol 2001;72:1146–50.
- Pérez-Chaparro PJ, Duarte PM, Shibli JA, Montenegro S, Lacerda Heluy S, Figueiredo LC, et al. Il peso attuale delle evidenze del profilo microbiologico associato alla periimplantite: una revisione sistematica. J Periodontol 2016;87:1295–304.
- Monje A, Suarez F, Galindo-Moreno P, García-Nogales A, Fu JH, Wang HL. Una revisione sistematica sulla perdita ossea marginale attorno a impianti dentali corti (<10mm) per protesi fisse supportate da impianti. Clin Oral Implants Res 2014;25:1119–24.
- Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group. Metodi di revisioni sistematiche e meta-analisi: elementi di reporting preferiti per revisioni sistematiche e meta-analisi: la dichiarazione PRISMA. J Clin Epidemiol 2009;62:1006–12.
- Lindhe J, Meyle J, Group D of European Workshop of Periodontology. Malattie peri-implantari: rapporto di consenso del sesto workshop europeo sulla parodontologia. J Clin Periodontol 2008;35:282–5.
- Lang NP, Berglundh T, Working Group 4 of the Seventh European Workshop on Periodontology. Malattie peri-implantari: dove siamo ora? Consenso del Settimo Workshop Europeo sulla Parodontologia. J Clin Periodontol 2001;38:178–81.
- Miller SA, Forrest JL. Migliorare la tua pratica attraverso decisioni basate su evidenze: PICO, imparare a porre buone domande. J Evid Based Dent Pract 2001;1:136–41.
- Graziani F, Figuero E, Herrera D. Revisione sistematica della qualità del reporting, misurazioni degli esiti e metodi per studiare l'efficacia degli approcci preventivi e terapeutici alle malattie peri-implantari. J Clin Periodontol 2012;39:224–44.
- Pjetursson BE, Zwahlen M, Lang NP. Qualità del reporting degli studi clinici per valutare e confrontare le prestazioni delle restaurazioni supportate da impianti. J Clin Periodontol 2012;39:139–59.
- Mombelli A, Décaillet F. Le caratteristiche dei biofilm nella malattia peri-implantare. J Clin Periodontol 2011;38:203–13.
- Mombelli A. Microbiologia e terapia antimicrobica della periimplantite. Periodontol 2000 2002;28:177–89.
- Leonhardt Å, Dahlén G, Renvert S. Risultati clinici, microbiologici e radiologici a cinque anni dopo il trattamento della periimplantite nell'uomo. J Periodontol 2003;74:1415–22.
- Paolantonio M, Perinetti G, D’Ercole S, Graziani F, Catamo G, Sammartino G. Decontaminazione interna degli impianti dentali: uno studio microbiologico randomizzato in vivo di 6 mesi sugli effetti di un gel di clorexidina. J Periodontol 2008;79:1419–25.
- Rismanchian M, Hatami M, Badrian H, Khalighinejad N, Goroohi H. Valutazione della dimensione della microfessura e della perdita microbica nell'area di connessione di 4 abutment con impianto Straumann (ITI). J Oral Implantol 2012;38:677–85.
- Rimondini L, Marin C, Brunella F, Fini M. Contaminazione interna di un sistema impiantare a 2 componenti dopo carico occlusale e ricostruzione provvisoriamente cementata con o senza dispositivo washer. J Periodontol 2001;72:1652–7.
- Jervøe-Storm PM, Jepsen S, Jöhren P, Mericske-Stern R, Enkling N. Colonizzazione batterica interna degli impianti: associazione con la perdita ossea peri-implantare. Clin Oral Implants Res 2015;26:957–63.
- Quirynen M, van Steenberghe D. Colonizzazione batterica della parte interna degli impianti a due stadi: uno studio in vivo. Clin Oral Implants Res 1993;4:158–61.
- Keller W, Brägger U, Mombelli A. Microflora peri-implantare di impianti con sovrastrutture cementate e mantenute a vite. Clin Oral Implants Res 1998;9:209–17.
- Persson LG, Lekholm U, Leonhardt A, Dahlén G, Lindhe J. Colonizzazione batterica sulle superfici interne dei componenti impiantari del sistema Brånemark. Clin Oral Implants 1996;7:90–5.
- Scarano A, Assenza B, Piattelli M, Iezzi G, Leghissa GC, Quaranta A. Uno studio di 16 anni sulla microfessura tra 272 impianti in titanio umani e i loro abutment. J Oral Implantol 2005;31:269–75.
- Cosyn J, Van Aelst L, Collaert B, Persson GR, De Bruyn H. Il solco peri-implantare confrontato con i componenti interni dell'impianto e della sovrastruttura: un'analisi microbiologica. Clin Implant Dent Relat Res 2009;13:286–95.
- Penarrocha-Oltra D, Rossetti PHO, Covani U, Galluccio F, Canullo L. Microperdita della connessione impianto/abutment a causa delle manovre di inserimento dell'impianto: analisi microbiologica trasversale in impianti dopo 5 anni di carico. J Oral Implantol 2014;41:e292–6.
- Canullo L, Penarrocha-Oltra D, Soldini C, Mazzocco F, Penarrocha M, Covani U. Valutazione microbiologica dell'interfaccia impianto-abutment in diverse connessioni: studio trasversale dopo 5 anni di carico funzionale. Clin Oral Implants res 2014;26:426–34.
- Canullo L, Rossetti PHO, Peñarrocha D. Identificazione di Enterococcus faecalis e Pseudomonas aeruginosa su e negli impianti in individui con malattia peri-implantare: uno studio trasversale. Int J Oral Maxillofac Implants 2015;30:583–7.
- Socransky SS, Haffajee AD, Ximenez-Fyvie LA, Feres M, Mager D. Considerazioni ecologiche nel trattamento delle infezioni parodontali da Actinobacillus actinomycetemcomitans e Porphyromonas gingivalis. Periodontol 2000 1999;20:341–62.
- Socransky SS, Haffajee AD, Smith C, Duff GW. Parametri microbiologici associati a polimorfismi del gene IL-1 in pazienti con parodontite. J Clin Periodontol 2000;27:810–8.
- Broggini N, McManus LM, Hermann JS, Medina R, Schenk RK, Buser D. Infiammazione peri-implantare definita dall'interfaccia impianto-abutment. J Dent Res 2006;85:473–8.
- Broggini N, McManus LM, Hermann JS, Medina RU, Oates TW, Schenk RK. Infiammazione acuta persistente all'interfaccia impianto-abutment. J Dent Res 2003;82:232–7.
- Cosyn J, Eghbali A, De Bruyn H, Collys K, Cleymaet R, De Rouck T. Impianti immediati a singolo dente nell'arcata anteriore: risultati a 3 anni di una serie di casi sulla risposta dei tessuti duri e molli e sull'estetica. J Clin Periodontol 2011;38:746–53.
- Tesmer M, Wallet S, Koutouzis T, Lundgren T. Colonizzazione batterica dell'interfaccia impianto-abutment: uno studio in vitro. J Periodontol 2009;80:1991–7.
- Nascimento CD, Pita MS, Fernandes FHNC, Pedrazzi V, de Albuquerque Junior RF, Ribeiro RF. Adesione batterica sulle superfici degli abutment in titanio e zirconia. Clin Oral Implants Res 2014;25:337–43.
- Koutouzis T, Wallet S, Calderon N, Lundgren T. Colonizzazione batterica dell'interfaccia impianto-abutment utilizzando un modello di carico dinamico in vitro. J Periodontol 2011;82:613–8.
- Assenza B, Tripodi D, Scarano A, Perrotti V, Piattelli A, Lezzi G. Perdita batterica in impianti con diverse connessioni impianto-abutment: uno studio in vitro. J Periodontol 2012;83:491–7.
- Paolantonio M, Perinetti G, D’Ercole S, Graziani F, Catamo G, Sammartino G, et al. Decontaminazione interna degli impianti dentali: uno studio microbiologico randomizzato in vivo di 6 mesi sugli effetti di un gel di clorexidina. J Periodontol 2008;79:1419–25.
- Romanos GE, Biltucci MT, Kokaras A, Paster BJ. Composizione batterica alla connessione impianto-abutment sotto carico in vivo. Clin Implant Dent Relat Res 2016;18:138–45.
